高一化学试题
下列说法不正确的是:( )
A.分子为C3H8与C6H14的两种有机物一定互为同系物
B.具有相同通式的有机物不一定互为同系物
C.属于同分异构体的物质,其分子式相同,相对分子质量相同;但相对分子质量相同的不同物质不一定是同分异构体
D.分子组成相差一个或几个CH2原子团的化合物必定互为同系物
X、Y是元素周期表中ⅦA族的两种元素。下列叙述能说明X的非金属性比Y强的是
A.X原子的电子层数比Y原子的电子层数多
B.X的氢化物的沸点比Y的氢化物的沸点低
C.Y的单质能将X从NaX的溶液中置换出来
D.X的气态氢化物比Y的气态氢化物稳定
三硫化四磷用于制造火柴及火柴盒摩擦面,分子结构如图所示.下列有关三硫化四磷的说法中正确的是( )
 A.该物质中磷元素的化合价为+3
A.该物质中磷元素的化合价为+3
B.该物质22 g含硫原子的数目约为1.806×1023
C.该物质分子结构中S、P最外层电子数均不为8
D.该物质分子中不含非极性共价键
在密闭容器中进行的可逆反应2X2(g)+Y2(g)⇌2Z(g),已知X2、Y2、Z的起始浓度分别0.1mol•L﹣1、0.2mol•L﹣1、0.2mol•L﹣1,在一定条件下,当反应达到平衡时,各物质的浓度可能( )
A. Z为0.3 mol•L﹣1
B. Y2为0.1 mol•L﹣1
C. X2为0.2 mol•L﹣1
D. Z为0.4 mol•L﹣1
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.标准状况下,22.4 L H2O含有分子数为NA
B.分子总数为NA的N2、CO![]() 混合气体体积约为22.4 L,质量为28 g
混合气体体积约为22.4 L,质量为28 g
C.4 g金属钙变成钙离子时失去的电子数目为0.1 NA
D.常温常压下,1.6 g CH4含原子数为0.5NA
控制适合的条件,将反应![]() 设计成如图所示的原电池。下列判断正确的是
设计成如图所示的原电池。下列判断正确的是

A. 反应开始时,甲中石墨电极上发生氧化反应
B. 反应开始时,乙中石墨电极上![]() 被还原
被还原
C. 电流计读数为零时,反应达到化学平衡状态,但反应还在进行
D. 电流计读数为零后,在甲中溶入![]() 固体,甲中石墨电极为正极
固体,甲中石墨电极为正极
用98%的浓H2SO4(密度为1.84 g/mL)配制1 mol·L-1的稀H2SO4 100mL,配制过程中可能用到下列仪器:
①100mL量筒;②10mL量筒;③50mL烧杯;④托盘天平;⑤100mL容量瓶;⑥胶头滴管;⑦玻璃棒。按使用出现的先后顺序排列正确的是
A. ②⑥③⑦⑤ B. ④③⑤⑦⑥ C. ①③⑦⑤⑥ D. ②⑤⑦⑥
己知某纯碱(Na2CO3)试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。

主要实验步骤如下:
①按图组装仪器,并检查装置的气密性;
②将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;
③称量盛有碱石灰(CaO与NaOH固体混合物)的U型管的质量,称得为bg;
④从分液漏斗滴入6mol·L-1的硫酸;直到不再产生气体时为止;
⑤从导管A处缓缓鼓入一定量的空气;
⑥再次称量盛有碱石灰的U型管的质量;
⑦重复步骤⑤和⑥的操作,直到U型管的质量基本不变,最终称得为cg;
请填空和回答问题:
(1)装置中干燥管B的作用是_______________
(2)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果将 (填偏高、偏低或不变)
(3)步骤⑤的目的是
(4)步骤⑦的目的是
(5)该试样中纯碱的质量分数的计算式为
对于可逆反应2SO2+O2 ![]() 2SO3达到平衡的标志是
2SO3达到平衡的标志是
A. SO2的反应速率和SO3的生成速率相等 B. SO2的物质的量等于SO3的物质的量
C. SO2的物质的量不再变化 D. SO2的百分含量是O2百分含量的2倍
下列化学用语表示不正确的是
A. 葡萄糖的分子式:C6H12O6 B. H2O的结构式:H-O-H
C. 乙醇的结构简式:CH3CH2OH D. 氯原子的结构示意图:![]()
.下列操作能达到目的的是( )
| 选项 | 目的 | 操作 |
| A | 配制20% CuSO4溶液 | 将20 g CuSO4·5H2O溶于80 mL蒸馏水中 |
| B | 除去NaCl中少量KNO3 | 将混合物制成热的饱和溶液,冷却结晶,过滤 |
| C | 除去KNO3溶液中的Ca2+ | 向溶液中加入Na2CO3溶液 |
| D | 确定NaCl溶液中是否混有Na2CO3 | 取少量溶液滴加CaCl2溶液,观察是否出现白色浑浊 |
同温同压下的氧气和氢气,两种气体的密度比为 ;若质量相等时,两种气体的体积比 ;如果a g 某气体中含有的分子数为b,则c g 该气体在标准状况下的体积约是 。
下列各组数据中,前者刚好是后者两倍的是( )
A.2 mol水的摩尔质量和1 mol水的摩尔质量
B.200 mL 1 mol/L氯化钙溶液中c(Cl-)和100 mL 2 mol/L氯化钾溶液中c(Cl-)
C.64 g二氧化硫中氧原子数和标准状况下22.4 L一氧化碳中氧原子数
D.20% NaOH溶液中NaOH的物质的量浓度和10% NaOH溶液中NaOH的物质的量浓度
水热法制备Fe3O4纳米颗粒的反应为3Fe2+ + 2S2O32-+ O2 +xOH-=Fe3O4 + S4O62- + 2H2O,
下列说法中不正确的是( )
A. 每生成1 mol Fe3O4,反应转移的电子总数为4 mol
B. Fe2+和S2O32-都是还原剂
C. 1 mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1/3 mol
D. x=4
下图是部分短周期元素的常见化合价与原子序数的关系:
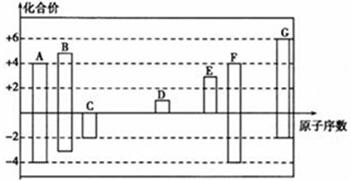
(1)元素A在周期表中的位置。C2﹣、D+、G2﹣离子半径大小顺序是____________(填离子符号)。
(2)用电子式表示D2G2的形成过程________________________。
(3)C、G的氢化物中沸点较低的是____________(填化学式)。
(4)C与D形成的具有强氧化性的化合物的电子式为____________。
四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物是生活中一种常用调味品.下列说法正确的是( )
A.简单离子半径:W<X<Z B.W与X形成的化合物溶于水后溶液呈碱性
C.气态氢化物的热稳定性:W<Y D.最高价氧化物的水化物的酸性:Y>Z
下列实验操作中正确的是 ( )
A. 蒸发操作时,应使混合物中的水分完全蒸干后才能停止加热
B. 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶支管口处
C. 分液操作时,分液漏斗中下层液体从下口放出后,上层液体从下口放出到另一烧杯
D. 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
下列说法或表示方法不正确的是( )
A. 盖斯定律实质上是能量守恒定律的体现
B. 在稀溶液中:H+(aq)+OH-(aq)=H2O(l);△H = –57.3kJ/mol,若将含0.5mol H2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ
C. 由C(石墨)→C(金刚石);△H = +73 kJ/mol,可知石墨比金刚石稳定
D. 在101kPa时,1molH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l);△H = –285.8kJ/mol
下列物质在一定条件下可与CH4发生化学反应的是( )
A. 氯水 B. 氧气 C. 溴水 D. 酸性KMnO4溶液
氢气在氯气中燃烧时产生苍白色火焰,在反应过程中,断裂1molH2中的化学键消耗的能量为Q1kJ,断裂1molCl2中的化学键消耗的能量为Q2 kJ,形成1molHCl中的化学键释放的能量为Q3kJ,下列关系式正确的是( )
A. Q1 + Q2 >Q3 B. Q1+ Q2 > 2Q3 C. Q1 + Q2 < Q3 D. Q1 + Q2 < 2Q3
- 符合东半球、北半球的地点是( ) A.25°N,25°W B.25°S,25°E C.4
- Who is the man teacher_______? A. you spoke to B. spok
- 细胞分裂后新细胞的遗传物质( ) A.比原细胞少一半 B.比原细胞多
- 已知p:{1}{0,1},q:{1}∈{1,2,3},由它们构成的新命题“p∧q”“p∨q”“p”中真命题的个数为()
- (4分)如图所示,有人对“利用频闪照相研究平抛运动规律”装置进行了改变,在装置两侧都装上完全相同的斜槽A、B,但位置有一
- 右图示某哺乳动物某一时期细胞中染色体组成及其上的部分基因。下列叙述不正确的是 A.该细胞含同源染色体,是处于有丝分
- 新华社报道,国家工商行政管理总局要求各地工商部门对辖区所有食品经营者建立食品安全信用档案,实行信用分类监管,切实提高监管
- 下图显示了人类发展史上经济发展阶段与环境质量之间的关系。据图回答:根据这种关系,发展中国家应认识到( )
- 恩格斯指出:国家是一种“特殊的公共权力,构成这种权力的,不仅有武装的人,而且还有物质的附属物,如监狱和各种强制机关”。中
- 读图,回答问题。若x轴表示南半球的纬度数值,y轴表示夜长,则 ( )
- (10分)旅游地理 阅读图文资料,完成下列要求。 材料一 中国、哈萨克斯坦、吉尔吉斯斯坦三国于2012年4月15日前正式
- 下列是日常生活中发生的变化,其中都属于化学变化的是() A.冰雪融化 白磷自燃 B.桂花飘香 钢铁生锈 C.粮
- 下列反应在通常情况下可以发生:①2FeCl3+Cu====2FeCl2+CuCl2 ②Fe+CuSO4====FeSO4
- A few years after Mom died, Dad handed me a plastic bag. Tha
- 函数在下列哪个区间上为增函数 A. B. C. D.
- (2a+b)(2a-b)+b(2a+b)-4a2b÷b,其中a=-,b=2
- 呼吸运动的完成依赖于( ) A.肺泡的弹性 B.氧气和二氧化碳的交换 C.膈肌、肋间
- 阅读下面的小说,完成小题。 掀起帷幔 【美国】戴维·兰勃纳 从老板的办公室出来,看着乱七八糟的办公桌,我气得七窍生烟。已
- 欲鉴别一株高茎豌豆是否是纯合子,最简便易行的方法是( ) A.杂交 B.观察
- 下列有关说法中正确的是() A.20℃时,20g某固态物质能溶解在100g水中,所以20℃时该物质的溶解度为20g B.



