高一化学试题
Na、Mg、Al三种金属各2mol分别跟1L 1mol∙L﹣1的盐酸反应时,相同条件下放出氢气体积最大的是( )
A . Al
B . Mg
C . Na
D . 三者产生的氢气一样多
合成氨工业是重要的化工基础。欲用N2和H2合成6800gNH3 , 请利用化学方程式计算参加反应的N2的体积(标准状况下)。
已知某原子的结构示意图为  ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )
A . 该元素位于第2周期第ⅡA族
B . 该元素位于第2周期第Ⅷ族
C . 该元素位于第3周期第ⅡA族
D . 该元素位于第3周期0族
根据下列几种粒子的结构示意图,回答问题:(填编号)

-
(1) 其中属于阴离子的是,
-
(2) 属于金属元素的是,
-
(3) 具有相似化学性质的是.
某研究性学习小组欲用化学方法测量一个不规则的容器的体积,取14.3g Na2CO3•10H2O放入100mL烧杯中,加入50mL水配成溶液,将溶液转移到该容器中,用蒸馏水稀释到完全充满该容器,从中取出10mL该溶液,然后逐滴滴入质量分数为3.65%(密度为1g/cm3)的稀盐酸直至没有气体放出为止,用去该稀盐酸10mL.求:
-
(1) 该容器的容积.
-
(2) 所得CO2在标况下的体积.
1993年8月国际原子量委员会确认我国张青莲教授测定的锑原子量(127.760)为标准原子量,已知锑有两种以上天然同位素,则127.760是()
A . 按照锑的各种天然同位素的质量数与这些同位素所占的原子百分比计算出来的平均值
B . 按照锑的各种天然同位素的相对原子质量与这些同位素所占的原子百分比计算出来的平均值
C . 一个锑原子的质量与12C原子的质量的的比值
D . 锑元素的质量与12C原子质量的 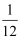 的比值
的比值
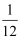 的比值
的比值
用试管收集60mL NO和NO2的混合气体,倒立于盛有水的水槽中,并缓慢通入O2 . 当分别通入VmL或40mL(V<40)O2时,均剩余20mL气体(均为标准状况).
①当通入40mL O2时剩余的气体是
②混合气体中NO2的体积是mL
③V的值是
④当恰好没有气体剩余时,所得溶液的物质的量浓度为(假设溶液不扩散)mol/L(保留到小数点后第三位)
下列有关化学用语表示正确的是( )
A . 钠离子的结构示意图:  B . 乙烯的比例模型:
B . 乙烯的比例模型:  C . 中子数为18 的氯原子
C . 中子数为18 的氯原子  Cl
D . 苯的结构简式:C6H6
Cl
D . 苯的结构简式:C6H6
 C . 中子数为18 的氯原子
C . 中子数为18 的氯原子  Cl
D . 苯的结构简式:C6H6
Cl
D . 苯的结构简式:C6H6
化学反应的实质就是旧键的断裂和新键的生成,欲探讨发生化学反应时分子中化学键在何处断裂的问题,近代科技常使用同位素示踪原子法,如有下列方法:
2R﹣14CH=CH﹣R′ R﹣14CH=CH﹣R+R′﹣14CH=CH﹣R′
R﹣14CH=CH﹣R+R′﹣14CH=CH﹣R′
由此可以推知:化合物 反应时断裂的化学键是( )
反应时断裂的化学键是( )
A . ①③
B . ①④
C . ②
D . ②③
乙烯、乙炔、甲苯、苯乙烯(  )4种有机物分别在一定条件下与H2充分反应.
)4种有机物分别在一定条件下与H2充分反应.
①若烃与H2完全加成反应时的物质的量之比为1:3,它是.
②若烃与H2完全加成反应时的物质的量之比为1:2,它是.
③苯乙烯与H2完全加成的物质的量之比为.
在100mLNaOH溶液中加入NH4NO3 和(NH4)2SO4 的固体混合物,加热使之充分反应,如图表示加入固体的质量与产生气体的体积(标准状况)的关系.试计算:

-
(1) NaOH溶液的物质的量浓度是 mol•L﹣1
-
(2) 当NaOH溶液为140mL,固体为51.6g时,充分反应产生的气体为 L(标准状况)
-
(3) 当NaOH溶液为180mL,固体仍为51.6g时,充分反应产生的气体为L(标准状况).
3He在月球上储量丰富,3He主要来源于宇宙射线的初级粒子,下列关于3He和4He的叙述正确的是( )
A . 两者互为同位素
B . 两者互为同素异形体
C . 两者为同一种核素
D . 两者具有相同的中子数
实验室常用KMnO4与浓盐酸反应制取氯气:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O,某同学将一定质量的KMnO4溶解在100mL 过量浓盐酸(右图为该浓盐酸试剂瓶标签上的有关数据)中,收集到4.48L 氯气(标准状况).请计算:


-
(1) 此浓盐酸的物质的量浓度是多少?
-
(2) 反应耗用KMnO4的质量是多少?
有相同质量的两份NaHCO3粉末,第一份加入足量盐酸,第二份先加热使其完全分解再加足量同质量分数的盐酸,则两者所消耗的盐酸中氯化氢的质量比为( )
A . 2:1
B . 1:1
C . 1:2
D . 3:2
一定温度下,在密闭容器中充入4moIX,当反应4X(g)⇌3Y(g)+Z(g)达到平衡状态时,有30%的X发生分解,则达到平衡状态时混合气体的总物质的量是( )
A . 4mol
B . 3.4mol
C . 2.8mol
D . 1.2mol
下列化学用语正确的是( )
A . 氢元素的同位素:1H2、2H2、3H2
B . N2的结构式:N≡N
C . 硼元素的元素符号:Be
D . 乙酸乙酯的结构简式:C4H8O2
《学习强国》学习平台说“最基本的生命分子中都有碳原子”。  常用于测定文物的年代,
常用于测定文物的年代,  作为示踪原子对研究有机化学反应和生物化学反应更为方便。
作为示踪原子对研究有机化学反应和生物化学反应更为方便。  被用来作为阿伏加德罗常数的标准。关于
被用来作为阿伏加德罗常数的标准。关于  、
、  、
、  说法正确的是( )
说法正确的是( )
 常用于测定文物的年代,
常用于测定文物的年代,  作为示踪原子对研究有机化学反应和生物化学反应更为方便。
作为示踪原子对研究有机化学反应和生物化学反应更为方便。  被用来作为阿伏加德罗常数的标准。关于
被用来作为阿伏加德罗常数的标准。关于  、
、  、
、  说法正确的是( )
说法正确的是( )
A . 质子数与质量数相同
B . 化学性质相似
C . 互为同素异形体
D . 质子数与中子数相等
铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各种性能的不锈钢,CrO3大量地用于电镀工业中。
-
(1) CrO3具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火,若该过程中乙醇被氧化成乙酸,CrO3被还原成绿色的硫酸铬[Cr2(SO4)3]。则该反应的化学方程式为:
。
-
(2) CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如下图所示。

①A 点时剩余固体的成分是(填化学式)。B 点时剩余固体的成分是(填化学式)
②从开始加热到 750K时总反应方程式为。
-
(3) CrO3和 K2Cr2O7均易溶于水,这是工业上造成铬污染的主要原因。净化处理方法之一是将含+6价 Cr 的废水放入电解槽内,用铁作阳极,加入适量的NaCl进行电解:阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成 Fe(OH)3 和Cr(OH)3沉淀除去[已知 KspFe(OH)3=4.0×10-38 , KspCr(OH)3=6.0×10-31]。
①电解过程中 NaCl 的作用是。
②已知电解后的溶液中c(Fe3+)为2.0×10-13 mol·L-1 , 则溶液中c(Cr3+)为mol·L-1。
一定质量的液态化合物XY2与标准状况下的一定质量的O2恰好完全反应,化学方程式为:XY2(l)+3O2(g)=XO2(g)+2YO2(g),冷却后,在标准状况下测得生成物的体积是672 mL,密度是2.56g/L,则:
-
(1) 反应前O2的体积是。
-
(2) 化合物XY2的摩尔质量是。
将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L.请回答:
-
(1) NO的体积为 L,NO2的体积为 L.
-
(2) 待产生的气体全部释放后,向溶液加入VmLamol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为 mol/L.
-
(3) 欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3 , 至少需要30%的双氧水 g.
最近更新
- 下图表示细胞膜的亚显微结构,下列对细胞膜结构和功能的叙述,正确的是 A.不同物种的细胞中①B.器官移植的成功率受③影响
- 图中属于费力杠杆的是:
- 豌豆灰种皮对白种皮是显性,黄子叶对绿子叶为显性.每对性状的杂合子(F1)自交后代(F2)均表现3:1的性状分离比.则下列
- 由于亚欧板块和印度洋板块挤压碰撞而形成的地形是( ) A.东非大裂谷 B.喜马拉雅山 C.亚洲东部的
- 下列有关化学变化中的能量关系的说法中,错误的是() A. 任何一个化学变化的过程中都包含着能量的变化 B
- 三角形的内角和等于() A.90° B.180° C.300° D.360°
- 节能减排,建设生态文明——2008年8月25日,国家发改委、科技部等部门发出关于贯彻实施《中华人民共和国节约能源法》的通
- 在公比q>1的等比数列{an}中,已知a2+a6=34,a3·a5=64,则数列{an}的前5项的和S5等于( )
- 我国城市建设中“南方北方一个样,大城小城一个样,城里城外一个样”,这种“千城一面”现象 A.体现了文化具有普遍性的特点
- β-胡萝卜素可以利用微生物的发酵生产,经过科研人员的努力,此种方法已取得了突破性进展: (1)生产β-胡萝卜素的工程菌是
- 下列物质的用途,主要是由其物理性质决定的是() A.氧气可用于医疗急救 B.澄清石灰水可用于检验二氧化碳 C.天然气可用
- 下列实验事故的处理方法正确的是( ) A. 实验桌上的酒精灯倾翻燃烧,马上用湿布扑灭 B. 不慎将酸(碱)溶液溅入
- 阅读下面这首宋诗,完成下题。 题西溪无相院① 张先 积水涵虚上下清,几家门静岸痕平。 浮萍破处见山影,小艇归时闻草声。
- 为检验浓硫酸与木炭在加热条件下反应产生的SO2和CO2气体,设计了如图所示实验装置,a、b、c为止水夹,B是用于储气的气
- 已知扇形的周长是6cm,面积是2cm2,则扇形的中心角的弧度数是( ) A.、1 B
- 氧气是一种化学性质比较活泼的气体,它可以和许多物质发生化学反应,如右图所示,关于三个反应的叙述中不正确的是 A.都是化
- 某物质只含一种元素,则该物质不可能是( ) A.化合物 B、纯净物 C、混合物
- 在一定条件下,发生CO + NO2CO2 + NO 的反应,达到化学平衡后,降低温度,混合物的颜色变浅,下列有关该反应的
- 北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬 燃料是丙烯(C3H6)。 (1)丙烷脱氢可得丙烯。 已
- 一幅地图,图上20厘米表示实际距离10千米,求这幅地图的比例尺 。



