高一化学试题
重水(D2O)是重要的核工业原料,下列说法不正确的是( )
A . 氘(D)原子核外有 1 个电子
B . H2O 与 D2O 互称同素异形体
C . 1H 与 D 互称同位素
D .  与
与  的相对分子质量相同
的相对分子质量相同
 与
与  的相对分子质量相同
的相对分子质量相同
成都市近年来常常发生“毒奶粉”事件.劣质奶粉制造商为牟取暴利,大大降低了奶粉中蛋白质的含量,导致食用这种奶粉的众多婴幼儿严重营养不良乃至死亡.为了测定某牛奶样品中蛋白质的含量,现采用“盖尔达法”分解其中的蛋白质.其原理是把蛋白质中的氮元素完全转化为氨气(化学式为NH3),再用稀硫酸吸收氨气,反应的化学方程式为:2NH3+H2SO4=(NH4)2 SO4现取该奶粉样品100g,用“盖尔达法”分解其中的蛋白质,产生的氨气用7.5g溶质质量分数为19.6%的稀硫酸恰好完全吸收.
计算并回答下列问题:
-
(1) 产生氨气的质量是多少?(计算结果精确到0.01,下同)
-
(2) 含氮元素的质量多少?
-
(3) 该奶粉中氮的含量是否达到了国家规定的标准.(奶粉中蛋白质的含量国家标准为:每100g婴幼儿奶粉中含12g~25g.蛋白质含氮元素的质量分数为16%)
最新科技报道,美国夏威夷联合天文中心的科学家发现了新型氢粒子,这种新粒子是由3个氢原子核(只有质子)和 2个电子构成,对于这种粒子,下列说法中正确的是( )
A . 是氢的一种新的同分异构体
B . 是氢的一种新的同位素
C . 它的组成可用 H3表示
D . 它比一个普通H2分子多一个氢原子核
下列说法错误的是( )
A .  H、
H、 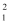 H、H+和H2是氢元素的四种不同粒子
B . 石墨和金刚石互称为同位素
C .
H、H+和H2是氢元素的四种不同粒子
B . 石墨和金刚石互称为同位素
C .  Ca和
Ca和  Ca互称为同位素
D . 12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同
Ca互称为同位素
D . 12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同
 H、
H、 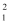 H、H+和H2是氢元素的四种不同粒子
B . 石墨和金刚石互称为同位素
C .
H、H+和H2是氢元素的四种不同粒子
B . 石墨和金刚石互称为同位素
C .  Ca和
Ca和  Ca互称为同位素
D . 12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同
Ca互称为同位素
D . 12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同
化合物甲(由氮和另一种常见的主族元素组成)是一种新型无机材料.将8.2g甲溶于足量的氢氧化钠溶液,可产生标准状况下为4.48L的气体,该气体可作制冷剂.向反应后的溶液中逐滴加入稀盐酸,产生白色沉淀质量最大为15.6g,继续滴加沉淀消失.则甲溶于氢氧化钠的化学方程式为
已知碳元素有12C、14C两种核素,氧元素有16O、18O两种核素,则它们所形成的二氧化碳分子共有( )
A . 2种
B . 4种
C . 6种
D . 12种
已知氧的相对原子质量为16,用氢气还原氧化铜法测定铜的相对原子质量,实验数据如下:
空硬质玻璃管 | 硬质玻璃管+氧化铜 | 硬质玻璃管+铜 | |
质量(g) | w | m | n |
则铜的相对原子质量为( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
等物质的量的下列物质在一定条件下与足量浓硝酸反应生成NO2 , 消耗硝酸的物质的量最多的是( )
A . Ag
B . FeI2
C . SO2
D . C
在1L溶液中含有Fe(NO3)3和H2SO4两种溶质,其浓度分别为0.2mol/L和1.5mol/L,现向该溶液中加入39.2g铁粉使其充分反应.下列有关说法正确的是( )
A . 反应后溶液中Fe3+物质的量为0.8mol
B . 反应后产生13.44L H2(标准状况)
C . 反应后溶液中Fe2+和Fe3+物质的量之和为0.9mol
D . 由于氧化性Fe3+>H+ , 故反应中先没有气体产生后产生气体
若某阴离子的结构示意图如图所示,则该元素在元素周期表中的位置可能是( )

A . 第四周期IA
B . 第三周期0族
C . 第二周期VIIA
D . 第三周期VIIA族
下列化学用语正确的是( )
A . 质子数为17、中子数为20的氯原子:  Cl
B . 氟原子的结构示意图:
Cl
B . 氟原子的结构示意图:  C . 明矾的化学式:KAlSO4•12H2O
D . 次氯酸的电离方程式:HClO=H++ClO﹣
C . 明矾的化学式:KAlSO4•12H2O
D . 次氯酸的电离方程式:HClO=H++ClO﹣
 Cl
B . 氟原子的结构示意图:
Cl
B . 氟原子的结构示意图:  C . 明矾的化学式:KAlSO4•12H2O
D . 次氯酸的电离方程式:HClO=H++ClO﹣
C . 明矾的化学式:KAlSO4•12H2O
D . 次氯酸的电离方程式:HClO=H++ClO﹣
完成下面各题:
-
(1) 向30毫升1mol/L的AlCl3溶液中逐渐加入浓度为2mol/L的NaOH溶液,若产生0.78克白色沉淀,则加入的NaOH溶液的体积可能为.
-
(2) 某溶液中有①NH4+、②Mg2+、③Fe2+、④Al3+四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是 .A . ①② B . ②③ C . ①③ D . ③④
-
(3) 把Ba(OH)2溶液滴入明矾溶液中,使SO42﹣全部转化成BaSO4沉淀,此时铝元素的主要存在形式是.
将9.6g铜单质置于200mL一定浓度的稀硝酸中,两者恰好完全反应.假定溶液体积不变,请回答下列问题:(要求写出计算过程)

-
(1) 反应生成的气体的体积(标况下);
-
(2) 反应过程中转移电子的物质的量;
-
(3) 参加反应的稀硝酸的物质的量浓度.
据科学家预测,月球的土壤中吸附着数百万吨的32He,每百吨32He核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以42He的形式存在。下列说法正确的是 ( )
A . 42He原子核内含有4个质子
B . 32He原子核内含有2个中子
C . 32He和42He互为同位素
D . 42He的性质很活泼
将9.75g锌加入到100ml 2mol/L 的盐酸中.当反应结束后求:
-
(1) 生成的ZnCl2的物质的量
-
(2) 生成的氢气在标况下的体积.
下列微观粒子中,互为同位素的是( )
A . 40Ar和40Ca
B . D和T
C . H2O和D2O
D . O2和O3
实验室用MnO2与浓盐酸共热制Cl2 , 当有14.6HCl被氧化时,将Cl2全部用消石灰吸收,可得漂白粉
A . 14.3g
B . 25.4g
C . 28.6g
D . 50.6g
下列说法正确的是( )
A . 钠原子失去一个电子后,它的电子数与氖原子相同,所以变成氖原子
B . 任何元素的原子都是由核外电子和核内中子、质子组成的
C . 核素指一种原子,而元素是指一类原子;核素间互称同位素,元素包含同位素
D . 40 18Ar、40 19K、40 20Ca的质量数相同,所以它们是互为同位素
二氧化硫、氮气、二氧化碳组成的混合气体在同温、同压下与笑气(N 2O)的密度相同,则该 混合气体中二氧化硫、氮气、二氧化碳的质量比为( )
A . 4:5:6
B . 22:1:14
C . 64:35:13
D . 29:8:13
测定水中溶解氧的方法:量取20mL水样,迅速加入MnSO4和KOH的混合溶液,再加入KI,立即塞好塞子,振荡使其完全反应.打开塞子,迅速加入适量硫酸溶液,此时有碘单质生成,6.0mLNa2S2O3溶液(每毫升含溶质1×10﹣5mol)与生成的碘恰好完全反应.上述过程发生反应的化学方程式为:
①2MnSO4+4KOH+O2→2MnO(OH)2+2K2SO4;
②MnO(OH)2+2KI+2H2SO4→I2+MnSO4+K2SO4+3H2O;
③I2+2Na2S2O3→2NaI+Na2S4O6
该样品中溶解氧量为( )
A . 0.75mg/L
B . 48mg/L
C . 24mg/L
D . 12mg/L
最近更新
- . The breakdown of the machine brought the work into
- .1921年8月,在莫斯科市民惊异的目光注视下,一位23岁的美国青年走进了克里姆林宫,他的名字叫阿曼德·哈默。在列宁的支
- 3.下列各句中,加横线的成语使用恰当的一项是( ) A.该产品的试用效果非常好,相信它大量投产后将不孚众望,公司
- 如图4-3-4所示,用一本书托着黑板擦在竖直平面内做匀速圆周运动(平动),先后经过A、B、C、D四点,A、B和C、D处于
- 推导动能定理的表达式(要求做图写出必要的过程)
- 在室温下,1升某气体分别与4升氧气混和,在引燃后将气体通过浓硫酸,剩余气体回复至室温时体积变为2升,则该气体是: ①乙烷
- —Where shall we gofor the holiday,to thebeach or into the mo
- ________ the plan has been made, let’s get down to ________
- 李强的家里养了一盆观赏植物——肾蕨,为了使它长得好,你认为他应该怎样做( ) A.放在向阳的地方,多浇水
- 完形填空 Television hasnow come to nearly every family. It has
- 下列各种饮料中,依靠生物发酵技术生产的是( )A.鲜榨果汁B.矿泉水C.鲜牛奶D.酸奶
- 天然色素的提取往往应用到萃取操作,现在有用大量水提取的天然色素,下列溶剂不能用来萃取富集这些天然色素的是 A.乙醇
- 如图所示,A、B两点固定两上等量正点电荷,在A、B连线的中点C处放一点电荷(不计重力),若给该点电荷一个初速度v0,v0
- 下列各组中的两种有机物,无论以何种比例混合,只要混合物总质量不变,完全燃烧时生成水的质量就不变,符合这一条件的组合是()
- 读我国某地气候资料表,回答下面试题。一月均温 七月均温 6-8月 降水量 12月至次年2月降水量 年降水量 主导风向 -
- (08年安徽皖南八校联考文) (本小题满分12分)如图,在平面直角坐标系中,(4,-3),点在第一象限内,交 轴于点,°
- 阅读下面诗词,完成后面题目。 永遇乐·京口北固亭怀古 辛弃疾 千古江山,英雄无觅孙仲谋处。舞榭歌台,风流总被雨打风
- 棉布开始成为民众的主要衣被原料是在 A. 两汉时期 B. 隋唐时期 C. 宋元时期 D
- 给全世界无产阶级的战歌──《国际歌》谱曲的音乐家是() A.欧仁·鲍狄埃B.狄盖特 C.瓦尔兰 D.贝多芬
- Are they still for holiday in Beijing now?They should have c



