高一化学试题
在浓度均为3mol/L的盐酸和硫酸各100mL溶液中,分别加入等质量的铁粉,充分反应后生成气体质量之比为3:4.则加入铁粉的质量是( )
A . 1.8 g
B . 11.2 g
C . 5.6 g
D . 8.4 g
下列属于同位素的一组是( )
A . O2、O3
B . Na2O、Na2O2
C .  K、
K、  Ca
D .
Ca
D .  H
H 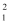 H
H  H
H
 K、
K、  Ca
D .
Ca
D .  H
H 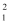 H
H  H
H
2.16g X2O5中含有0.1mol氧原子,则X的相对原子质量为( )
A . 28 g•mol﹣1
B . 28
C . 14 g•mol﹣1
D . 14
把氢氧化钠滴入相同物质的量浓度的硫酸铜溶液中有沉淀生成,由实验可知,氢氧化钠溶液和硫酸铜的体积比3∶2时,残留在溶液中的Cu2+的量极小(可以认为Cu2+全部沉淀)此时生成的沉淀的化学式可能是 ( )
A . Cu(OH)2
B . Cu2(OH)2SO4
C . CuSO4•5H2O
D . Cu4(OH)6SO4
天然铊有两种稳定同位素,  Tl和
Tl和  Tl.下列有关铊的同位素说法中,不正确的是( )
Tl.下列有关铊的同位素说法中,不正确的是( )
 Tl和
Tl和  Tl.下列有关铊的同位素说法中,不正确的是( )
Tl.下列有关铊的同位素说法中,不正确的是( )
A .  Tl 和
Tl 和  Tl 质子数相同
B .
Tl 质子数相同
B .  Tl 和
Tl 和  Tl互为同素异形体
C .
Tl互为同素异形体
C .  Tl 和
Tl 和  Tl中子数之差为2
D .
Tl中子数之差为2
D .  Tl 原子核内中子数与核外电子数之差为43
Tl 原子核内中子数与核外电子数之差为43
 Tl 和
Tl 和  Tl 质子数相同
B .
Tl 质子数相同
B .  Tl 和
Tl 和  Tl互为同素异形体
C .
Tl互为同素异形体
C .  Tl 和
Tl 和  Tl中子数之差为2
D .
Tl中子数之差为2
D .  Tl 原子核内中子数与核外电子数之差为43
Tl 原子核内中子数与核外电子数之差为43
下列各组物质中,互为同位素的是( )
A . T2O与D2O
B .  K与
K与  Ca
C . O2和O3
D .
Ca
C . O2和O3
D . 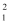 H和
H和  H
H
 K与
K与  Ca
C . O2和O3
D .
Ca
C . O2和O3
D . 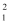 H和
H和  H
H
(1)某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的原子结构示意图是 .
(2)已知某粒子的结构示意图为: 
试回答:
①当x﹣y=10时,该粒子为 (填“原子”、“阳离子”或“阴离子”).
②当y=8时,粒子可能为(填名称) 、
③写出y=3与y=7的元素最高价氧化物对应水化物发生反应的离子方程式
下列有关化学用语表示正确的是( )
A . 次氯酸的结构式:H—Cl—O
B . 质子数为53、中子数为72的碘原子: C . 对硝基苯酚的结构简式:
C . 对硝基苯酚的结构简式: D . Na+的结构示意图:
D . Na+的结构示意图:
 C . 对硝基苯酚的结构简式:
C . 对硝基苯酚的结构简式: D . Na+的结构示意图:
D . Na+的结构示意图:
一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和H2O的总质量为41克,若水的质量为16.2克,求CO2的质量.
根据下列叙述,写出元素名称并画出原子结构示意图。
-
(1) A元素原子核外M层电子数是L层电子数的一半:。
-
(2) B元素原子的最外层电子数是次外层电子数的1.5倍:。
-
(3) C元素的单质在常温下可与水剧烈反应,产生的气体能使带火星的木条复燃: 。
-
(4) D元素原子的次外层电子数是最外层电子数的:。
盛有O2和NO2的混合气体的量筒倒立在盛有水的水槽中,过一段时间后,量筒内的气体体积减小为原来的一半.则原混合气体中O2和NO2的体积比是( )
A . 3:1
B . 3:2
C . 2:1
D . 1:2
在常温常压下,①CH4②C2H6③C3H8④C4H10 .
-
(1) 取等物质的量的下列四种气态烃,分别在足量的氧气中燃烧,消耗氧气最多的是(填分子式).
-
(2) 取等质量的量的下列四种气态烃,分别在足量的氧气中燃烧,消耗氧气最多的是(填分子式).
下列有关化学用语使用正确的是( )
A . 次氯酸的结构式:H-Cl–O
B . 乙烯的结构简式CH2CH2
C . 硫离子的结构示意图:  D . 丙烷分子的球棍模型:
D . 丙烷分子的球棍模型: 
 D . 丙烷分子的球棍模型:
D . 丙烷分子的球棍模型: 
将钠、镁、铝各0.3 mol分别放入100 mL 1 mol·L-1的盐酸中,同温同压下产生的气体的体积比为( )
A . 1∶2∶3
B . 6∶3∶2
C . 3∶1∶1
D . 1∶1∶1
钙和钠相似,也能形成含O22-离子的过氧化物,下列叙述错误的是 ( )
A . 过氧化钙的化学式是CaO2
B . 1 mol过氧化钙或过氯化钠跟足量的水反应都生成1mol氧气
C . O22-离子的电子式为  D . 过氧化钙或过氯化钠都是强氧化剂
D . 过氧化钙或过氯化钠都是强氧化剂
将51.2gCu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.6mol,这些气体恰好能被500mL 2mol/LNaOH溶液完全吸收,生成含NaNO3和NaNO2的盐溶液,其中NaNO3的物质的量为( )
A . 0.2mol
B . 0.6mol
C . 0.8mol
D . 1.0mol
氯只有  和
和  两各稳定同位素,它们在氯气中的原子数之比
两各稳定同位素,它们在氯气中的原子数之比  :
:  为3:1.则相对分子质量为70、72、74、的氯气分子数之比可能是( )
为3:1.则相对分子质量为70、72、74、的氯气分子数之比可能是( )
 和
和  两各稳定同位素,它们在氯气中的原子数之比
两各稳定同位素,它们在氯气中的原子数之比  :
:  为3:1.则相对分子质量为70、72、74、的氯气分子数之比可能是( )
为3:1.则相对分子质量为70、72、74、的氯气分子数之比可能是( )
A . 5:2:1
B . 5:2:2
C . 9:3:1
D . 9:3:2
将10.6 g由Mg、Al、Si组成的合金投入足量的NaOH溶液中,在标准状况下产生气体11.2L;另取等质量的合金溶于过量稀H2SO4中,合金质量减少了7.8g。则合金中Mg、Al、Si的物质的量之比为( )
A . 1:2:1
B . 2:1:1
C . 1:3:2
D . 1:1:2
1.2gRSO4中含0.01molR2+ , 则RSO4的摩尔质量是 ;R的相对原子质量是
用KMnO4氧化一定体积密度为1.19g/cm3 , 溶质质量分数为36.5%的 盐酸.反应方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
-
(1) 用双线桥法分析该反应(只需标出电子得失的方向和数目)
-
(2) 15.8g KMnO4参加反应能消耗多少摩尔HCl?
-
(3) 产生的Cl2在标准状况下的体积为多少升?
最近更新
- 某政协委员公开展示了一幅包括103种常用证件、长达3.8米的“人在证途”图,并由衷感叹:中国人不是在办证,就是在去办证的
- 把过量的稀盐酸加入盛有少量镁粉、铁粉、铜粉、氢氧化钾的混合物的小烧杯中,经充分反应后,加水稀释并过滤,在滤纸上剩下的物质
- 下图是地球公转示意图,回答地球从①公转到③期间,正午屋内的光照面积将A 越来越大 B 由小变大,再由大变小 C 越
- 25 ℃时,用浓度为0.100 0 mol·L-1的NaOH溶液分别滴定20.00mL浓度均为0.100 0 mol·L
- A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的
- 在实验中得到小车做直线运动的s-t关系如图所示。(1)由图可以确定,小车在AC段和DE段的运动分别为
- 右图是某研究性学习小组设计的示意图,最适合作为其标题的是 A.《多样性的政治文明》 B.《典型的民主政治制度》 C.《中
- 下列各句中,加点的成语使用恰当的一项是 A.在一些触景生情的场合,往事历历,那风雨不蚀的记忆,实在是人性一种根深蒂固的表
- 含苯酚的工业废水处理的流程图如图所示:(1)上述流程里,设备Ⅰ中进行的是_________操作(填写操作名称)。实验室里
- 能说明苯分子中的碳碳键不是单双键交替,而是所有碳碳键都完全相同的事实是( )A.苯的一元取代物没有同分异构体
- 氢气是理想的高能燃料。若充分燃烧8g氢气,最少需要氧气多少克?
- 在全国农运会上,其中女子45kg级举重冠军被某省运动员获得,成绩是95kg。电视屏幕上的加入展示了她的举重全过程:她用力
- 上海师大附中等六校2011届高三联考英语试题 The fashion designer makes frequent t
- 郑州市跌贴正式开通方便了人们的 生活,修建地铁需要大量钢铁制品.现代工业利用磁铁矿的主要原理 (用化学方程式表示).
- The ______on his face told me that he was angry. A. impre
- 新中国成立后,为了解决民族问题而制定的基本政策是 A.人民代表大会制度 B.多党合作制 C.按劳分配制度 D.
- 下列选项中不属于免疫的正常功能的是() A.抵抗病原体的入侵 B.清除体内死亡细
- 如图,已知的面积为,. 如果,那么向量与的夹角的取值范围是 .
- 盛浓硫酸和浓盐酸的两个试剂瓶敞口放置一段时间,则两瓶溶液( ) A. 质量都增加了
- 某烃的结构简式为,它可能具有的性质是 A.它能使溴水褪色,但不能使酸性高锰酸钾溶液褪色 B.它既能使溴水褪色



