高一化学试题
PM2.5是指大气中直径小于或等于2.5微米(1微米=10-6米)的可入肺的有害颗粒。下列有关说法中不正确的是( )
A. 研制开发燃料电池汽车,降低机动车尾气污染,某种程度可以减少PM2.5污染
B. PM2.5表面积大,能吸附大量的有毒、有害物质
C. PM2.5在空气中形成了胶体
D. PM2.5主要来自工业生产、汽车尾气排放等过程中经过燃烧而排放的残留物,大多含有重金属等有毒物质
下列反应中,铁元素被氧化的是( )
A.FeS+2HCl9FeCl2+2H2S↑ B.Fe+H2S049FeS04+H2↑
C.FeO+2HCl9FeCl2+H20 D.Fe203+3CO92Fe+3C02↑
下列说法正确的是( )
A.氢氟酸、浓硝酸、硅酸钠溶液依次保存在棕色玻璃瓶、无色细口瓶、带胶塞细口瓶中
B.钠着火时不能用泡沫灭火器灭火
C.用饱和碳酸钠溶液除去CO2中混有的HCl
D.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
已知某溶液中存在较多的H+、SO42+ 、NO3- ,则溶液中还可能大量存在的离子组成( )
A.Al3+、CH3COO-、Cl- B.Na+、NH4+、Cl-
C.Mg2+、Cl-、Fe2+ D.Mg2+、Ba2+、Br-
(1)实验室常用下图所示装置制取并收集氨气。
 |
①实验室制取氨气反应的化学方程式为 ;
②图中方框内收集氨气的装置可选用 (填字母序号);
③尾气处理装置中使用倒扣漏斗的作用是 。
(2)在盛有一定量浓硝酸的试管中加入6.4g的铜片发生反应。请回答下列问题:
①开始阶段,反应的化学方程式为 ,若该反应共产生标准状况下气体2.24L,则反应过程中被还原的HNO3的物质的量为 。
②反应结束后铜片有剩余,再加入少量20%的稀硫酸,这时铜片上又有气泡产生,反应的离子方程式为 。
引起环境污染的原因不正确的是
A. 重金属、农药和难分解有机物、含N、P的污水等会造成水体污染
B. 装饰材料中的甲醛、芳香烃及氡等会造成居室污染
C. SO2、NO2和CO2都会导致酸雨的形成
D. CO2的大量排放会造成温室效应的加剧
合金A由四种单质组成,已知:①合金A中不含K、Ca、Na;②气体B可燃;③气体G为人体新陈代谢的主要产物之一,请据图回答以下问题:
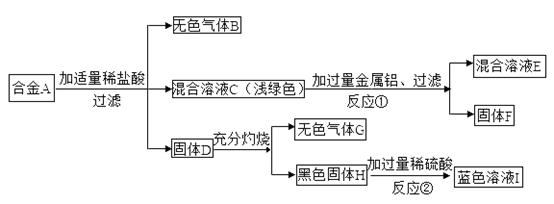
(1)合金A由哪些单质组成(用化学式表示):_____、_______、________、________;
(2)写出反应①的化学方程式:______________;
(3)写出反应②的化学方程式:__________________。
下列关于铝及其化合物叙述中,正确的是
A.不能用铝制的器皿来盛放酸梅汤或碱水是因为铝会和酸或碱反应
B.铝制品在空气中有很强的抗腐蚀性是因为铝的化学性质很稳定
C.氯化铝溶液与NaOH溶液互滴现象完全相同
D.纯铝比铝合金的硬度更大、熔点更低
德国化学家凯库勒研究提出的苯分子结构模型如图所示:

(1)请根据苯的分子结构模型,写出苯的分子式_______,结构式____________,结构简式________________。
(2)向试管中加入3 mL酸性高锰酸钾溶液,再加入1 mL苯,振荡试管。观察到的实验现象是_______________。
(3)向试管中加入1 mL溴水,再加入3 mL苯,振荡试管。观察到的实验现象是_____________。
(4)你认为凯库勒提出的苯的分子结构符合实验事实吗?________,理由是_____________。
1 mol/L的NaCl溶液表示( ).
A、溶液中含有1 mol NaCl B、1 L溶液里含有NaCl 58.5克
C、58.5 g NaCl溶于941.5 g水中 D、1 mol NaCl溶于1 L水中
主族元素在周期表中的位置,取决于该元素的( )
A、最外层电子数和原子量 B、原子量和核外电子数
C、 次外层电子数和电子层数 D、电子层数和最外层电子数
下列有关原电池的应用原理和有机物的结构及其性质说法中,不正确的是( )
A.铜锌硫酸组成的原电池中,电子是从锌经过导线流向铜
B.把Zn片放入盛有盐酸的试管中,加入几滴CuCl2溶液,形成原电池加快了产H2速率
C.乙烯能使溴水和酸性KMnO4溶液褪色,乙烯使两者褪色的化学原理相同
D.C5H10不属于烷烃,C5H12属于烷烃且有3种同分异构体
NA代表阿伏加德常数,下列说法中正确的是( )
A.在同温同压时,相同体积的任何气体单质所含的原子数目相同
B.标准状况下,22.4 L水所含的水分子数为NA
C.在常温常压下,11. 2 L氮气所含的原子数目为NA
D.34g氨气所含质子数目为20 NA
下列反应中,属于氧化还原反应同时又是放热反应的是( )
A. Ba(OH)2·8H2O与NH4Cl反应 B. 铝与稀盐酸
C. 灼热的炭与水蒸气生成一氧化碳和氢气的反应 D. 氧化铁和稀盐酸的反应
CO与O2反应生成CO2的历程如图(部分微粒未画出):下列分析不正确的是( )

A.CO2的电子式为![]()
B.在该过程中,断裂了非极性共价键
C.CO和O生成了具有极性共价键的CO2
D.CO和O生成CO2的过程涉及了电子转移
下列物质中属于混合物的是__________(填序号,以下同)属于电解质的是__________,属于非电解质的是__________,能导电的是__________。
①CH3COOH②氨气③酒精④氯化钠固体⑤盐酸⑥BaSO4⑦CO2⑧液态氯化氢
Na与硫酸铜溶液反应的实验现象是( )
A、置换出金属铜 B、产生气体、置换出金属铜
C、生成蓝色沉淀 D、产生气体、生成蓝色沉淀
19.6克铁粉和8克硫粉混合后放入密闭容器中加热,充分反应后冷却,再加入250毫升一定物质的量浓度的盐酸恰好完全反应。试求:
(1)反应后可生成标准状况下的气体多少升? (2)所加盐酸的物质的量浓度为多大?
由淀粉发酵最终可制得有机化合物A,某同学为研究A的化学组成,进行如下实验:
(1)称取0.9g有机物A,在一定条件下使其完全气化。已知相同条件下同体积的H2为0.02g,则有机物A的相对分子质量为 。
(2)若将![]() 上述有机物A蒸汽在O2中完全燃烧只生成CO2和H2O(g), 产物全部被碱石灰吸收,碱石灰增重1.86g;若通入过量石灰水中产生3.0g沉淀,则A的分子式 。
上述有机物A蒸汽在O2中完全燃烧只生成CO2和H2O(g), 产物全部被碱石灰吸收,碱石灰增重1.86g;若通入过量石灰水中产生3.0g沉淀,则A的分子式 。
(3)另取0.9g的有机物A跟足最金属钠反应,生成H2224mL(标况);若与足最NaHCO3反应,生成224mLCO2(标况)。通过化学分析知A结构中含有一个“-CH3”则A的结构简式是 。
欲配制0.1 mol/L的Na2CO3溶液240 mL,完成下列步骤:
(1)用托盘天平称取Na2CO3·10H2O(摩尔质量为286g/mol)固体 克。
(2)配制过程中需要用到托盘天平、烧杯、玻璃棒、药匙,还需要什么仪器?
、 (2种)
(3)下列实验操作中,按先后顺序排列为________ 。
A.将溶解好的Na2CO3溶液沿玻璃棒注入容量瓶中,
B.将洗涤液也注入容量瓶中,轻轻摇动容量瓶,使溶液混合均匀,
C.将称量好的固体放入烧杯中,
D.向烧杯中加入适量蒸馏水,用玻璃棒搅拌并冷却至室温,
E.用适量蒸馏水洗涤烧杯2~3次,
F.向容量瓶中加蒸馏水到液面接近刻度1 cm~2 cm处,
G.盖上瓶塞,并反复倒转摇匀,
H.用胶头滴管加蒸馏水到瓶颈刻度处,
(4)在配制过程中,如果出现下列情况,将对所配溶液的物质的量浓度有何影响?(填“偏高”、“偏低”或“无影响”)
A.洗涤时,未将洗涤液注入容量瓶中________________;
B.转移溶液时,容量瓶中有少量蒸馏水_________________;
C.称取Na2CO3·10H2O晶体时,晶体已经部分风化了_______________;
D.定容时,仰视观察容量瓶刻度线_________________。
(5)若配制时不小心加水超过了刻度线,用胶头滴管把多余的水吸出来,会导致所配溶液浓度_________,此时应该怎么办? 。
- 如图,在同一竖直面内,小球、b从高度不同的两点,分别以初速和沿水平方向抛出,经时间和后落到与两抛出点水平距离相等的P点,
- 中国上海世界博览会,于2010年5月1日~10月31日举办。上海世博会的门票为:平日普通票价格为160元人民币、指定日普
- 下图为一段纬线,P点以东是海洋,Q点以西是海洋,S和T之间为某一海域,其余为陆地,回答下题。S—T之间的海域的洋流是(
- 右图是某化肥包装袋上的部分说明,该化肥属于 A.氮肥 B.磷肥
- 39. Is this the reason ____ at the meeting for his carelessn
- 函数 自变量x的取值范围是 .
- 对右边漫画《节能减排“死任务”,百姓冷暖谁人管》中某市的做法,认识正确的是( )A.符合科学发展观的要求B.违背了
- 食品安全与人体健康密切相关。下列做法不会损害人体健康的是 A.吃变蛋(或松花蛋)时,为消除蛋中所含碱性物
- The law requires governments to increase investment in publi
- 某原电池装置如图所示,电池总反应为下列说法正确的是( ) A.正极反应为 B.放电时,交换膜右侧溶液中有大量白色沉淀生
- 设a,b是两个非零向量. A.若|a+b|=|a|-|b|,则a⊥b B.若a⊥b,则|a+b|=|a|-|b| C.若
- 《化学教育》报道了数起因食用有“瘦肉精”的猪肉和内脏,而发生急性中毒的恶性事件。这足以说明,目前由于奸商的违法经营,已使
- 在一次射击比赛中,8个泥制的靶子挂成三列,其中两列各挂3个,一列挂两个,如图所示.一射手按照下列规则去击碎靶子:先挑选一
- 除去下列物质中的少量杂质,所选用的试剂正确的是选项 物质 杂质 试剂 A CO2 HCl 氢氧化钠溶液 B Cu CuO
- 下列关于物质跨膜运输的叙述正确的是 A.线粒体DNA上的基因所表达的酶与线粒体的功能有关,若线粒体DNA受损伤,对神经细
- Drama is a huge part of British culture and has been________
- .下列各项加点字读音全都正确的一项是 A.贿赂(lù) 瑰(guī)怪 荫(yīn)庇 哺(
- 对下列现象或事实的解释中,不正确的是选项 事 实 解 释A 二氧化碳吸入过多,会使人窒息死亡 二氧化碳有
- 依次填入下面的一段文字横线处的语句,衔接最恰当的一组是 真正精致的石头虽则应该暗示雄伟或出尘超俗的感觉,然而线条
- 下列不属于“长大”的内涵是 ( )A.懂得自我约束和自我控制,老师家长在与不在时都一个样B.懂得自立自强,尊重理解他



