高一化学上学期上册试题
下列叙述正确的是( )
A. 金属单质在氧化还原反应中只能作还原剂
B. 非金属单质在氧化还原反应中只能作氧化剂
C. 钠原子在反应中失去1个电子,而铝原子失去3个电子,所以钠的还原性小于铝
D. 金属元素被还原时一定生成金属单质
仪器名称为“容量瓶”的是
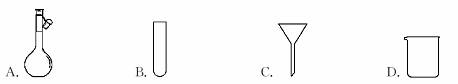
下列化学名称及化学用语书写正确的是( )
A.崔化剂 B.一氧化碳 C.硝酸安 D.粹取
某实验需要480ml 0.5mol/L的NaOH溶液,请回答下列问题:
(1)应称取NaOH的质量______g,应选用容量瓶的规格是_______ml。
(2)除容量瓶外还需要的其它玻璃仪器是________、________及玻璃棒
(3)配制时,其正确的操作顺序是(用字母表示,每个操作只能用一次)________。
A.将容量瓶盖紧,振荡,摇匀
B.用托盘天平准确称量所需的NaOH质量,倒入烧杯中,再加入适量水,用玻璃棒慢慢搅动,使其溶解(必要时可加热)
C.用适量水洗涤烧杯2-3次,洗涤液均注入容量瓶中,振荡
D.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
E. 将已冷却的溶液沿玻璃棒注入容量瓶中
F.继续往容量瓶内小心加水,直到液面接近刻度1-2cm 处
(4)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)没有进行C操作________;配制溶液时,定容时仰视刻度线 ________;容量瓶未干燥________。
某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图所示的变化。

请回答下列问题。
(1) 图中涉及分离溶液与沉淀的方法是__________________。
(2) B、C、D、E 4种物质的化学式为:
B_________、C_________、D_________、E_________。
(3) 沉淀F与NaOH溶液反应的离子方程式为
沉淀E与稀硫酸反应的离子方程式为
溶液G与过量稀氨水反应的化学方程式为
溶液.胶体和浊液这三种分散系的根本区别是 ( )
A.是否大量分子或离子的集合体 B.分散质粒子直径的大小
C.是否能通过滤纸或半透膜 D.是否均一.稳定.透明
下列检验方法和结论都正确的是( )
A.加人AgNO3溶液有白色沉淀生成,证明原溶液中一定有Cl-
B.加入稀盐酸酸化的BaCl2溶液,有白色沉淀生成,证明原溶液中一定有SO![]()
C.加入盐酸后加热,放出能使澄清石灰水变浑浊的无色无味气体,证明原溶液中一定有CO32-
D.加入浓的氢氧化钠溶液后加热,放出能使湿润的红色石蕊试纸变蓝的气体,证明原溶液中一定有NH4+
下列有关碳酸钠和碳酸氢钠的说法不正确的是
A.热稳定性:碳酸钠>碳酸氢钠
B.相同温度下的溶解度:碳酸钠>碳酸氢钠
C.等质量的碳酸钠和碳酸氢钠分别与足量的盐酸反应,前者产生二氧化碳少
D.足量的碳酸钠和碳酸氢钠分别与等物质的量的盐酸反应,两者产生二氧化碳一样多。
设NA表示阿伏加德罗常数的值,下列叙述正确的是
A.标准状况下,22.4L H2O含有的原子数为3NA
B.常温常压下,1.06g Na2CO3含有的Na+数目为0.02NA
C.5.6g铁粉放入足量稀硫酸中转移的电子数为0.3NA
D.0.5mol·L-1的MgCl2溶液中,含有Cl-个数为NA
下列除杂质的方法不正确的是()
A.铜粉中混有铁粉:加入过量盐酸充分反应,过滤
B.CO2中混有HCl:将其通入NaOH溶液,洗气
C.NaHCO3溶液中混有少量Na2CO3:往该溶液中通入过量CO2气体
D.FeCl2溶液中混有少量FeCl3:加入Fe粉
对下列实验过程的评价,正确的是:
A.X溶液与NaOH混合加热产生使湿润的红色石蕊试纸变蓝的气体,则X一定含NH4+
B.Y溶液中滴加BaCl2溶液,生成不溶于稀HNO3的白色沉淀,则Y一定含SO42-
C.Z的无色溶液滴入紫色石蕊试液显蓝色,则Z溶液一定含有大量的H+
D.W固体中加入稀盐酸,产生了无色气体,证明W固体中一定含有CO32-
在自来水的生产中,常通入适量氯气进行杀菌消毒,氯气与水反应的产物之一是盐酸。
市场上有些不法商贩为牟取暴利,利用自来水冒充纯净水桶装出售。为辨别真伪,可用以鉴别的一种试剂是
A.氢氧化钠溶液 B.酚酞试液 C.硝酸银溶液 D.氯化钡溶液
X、Y、Z、W四种物质有如下相互转化关系(其中X、W为单质,Y、Z为化合物,未列出反应条件)。
 ⑴若Z是生活中常用的调味品,W遇淀粉溶液变蓝,则X单质在常温下的颜色为 ▲ 。
⑴若Z是生活中常用的调味品,W遇淀粉溶液变蓝,则X单质在常温下的颜色为 ▲ 。
⑵若X是常温下密度最小的气体,Y由两种非金属元素组成,,其中一种在地壳中的含量仅次于氧,另一种在海水中的含量仅次于氢和氧,则Z的化学式为 ▲ 。
⑶若X原子的质子数是W原子质子数的2倍,且X原子最外层电子数为2。则W的原子结构示意图为 ▲ 。
有一种微型钮扣电池——银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn + 2OH--2e-=ZnO + H2O,Ag2O+H2O+2e―=2Ag +2OH-,总反应为Ag2O + Zn = 2Ag + ZnO。根据上述反应式,判断下列叙述中正确的是( )
A.在使用过程中,电池负极区溶液pH增大
B.在使用过程中,电子由Ag2O极经外电路流向Zn极
C.在使用过程中,Zn电极发生还原反应,Ag2O电极发生氧化反应
D.外电路中每通过0.2mol电子,正极质量理论上减小1.6g
下列物质属于纯净物的是
A.液氯 B.合金 C.水玻璃 D.漂白粉
取50.0mLNa2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到14.51g白色沉淀,用过量稀硝酸处理后沉淀量减少到4.66g,并有气体放出。试计算:
(1)原混合溶液中Na2CO3和Na2SO4的物质的量浓度分别为____________、___________;
(2)产生的气体在标准状况下的体积_____________。
(3)已知t℃时Na2CO3的溶解度为Sg,该温度![]() 下Na2CO3饱和溶液溶质的物质的量浓度是c mol/L,则此饱和溶液的密度为(用S、c表示)_______________g/mL。
下Na2CO3饱和溶液溶质的物质的量浓度是c mol/L,则此饱和溶液的密度为(用S、c表示)_______________g/mL。
下列关于氯水的叙述不正确的是
A.新制氯水长期放置后颜色会逐渐褪为无色
B.长期放置的氯水也能使有色布条褪色
C.长期放置的氯水中含有的H+多于新制氯水
D.新制氯水中含有的阳离子只有 H+
下列变化中需加入氧化剂才能实现的是
A.S→SO2 B.Na2O2→O2 C.HNO3→NO D.2H+→H2
下列各组中的两种物质相互作用时,反应条件(温度、反应物用量比)改变,不会引起产物的种类改变的是()
A.![]() 和
和![]() B.
B.![]() 溶液和
溶液和![]() 溶液
溶液
C.![]() 和
和![]() D.
D.![]() 溶液和
溶液和![]()
下列变化过程中,加入氧化剂才能实现的是
A.Cl2→Clˉ B.Iˉ→I2 C.SO2→SO![]() D.CuO→Cu
D.CuO→Cu
- 下列在现代生物科技的应用中,需要进行检测与筛选的是()① 对植物的愈伤组织进行诱变处理,培育作物新品种;② 将鼠的骨髓瘤
- 关于澳大利亚城市的叙述正确的是A.首都堪培拉是全国人口最多的城市 B.墨尔本是澳大利亚太平洋沿岸最大港口C.珀斯是
- 如图所示,一根轻绳跨过定滑轮,两端分别系着质量为m1、m2的小物块,m1放在地面上,m2离地面有一定高度。当m2的质量发
- 两个所受重力大小分别为GA和GB的小球A和B,用轻杆连接,放置在光滑的半球形碗内。小球A、B与碗的球心O在同一竖直平面内
- 细胞衰老是一种正常的生命现象。人的细胞在衰老过程中不会出现的变化是( ) A.细胞内有些酶活性降低
- 下列描述的运动中,不属于机械运动的是:( ) A.一个巨大的星系正在吞噬一个小星系 B.大城市里滚滚的车流 C.桂花
- 下列关于常用消毒剂的叙述中,正确的是A.高锰酸钾(KMnO4)是氧化物B.H2O2中氢元素的质量分数为11.1%C.次氯
- 竖直绝缘墙壁的Q处有一固定的小球A,在Q的正上方的P点用绝缘丝线悬挂另一小球B,A、B两小球因带电而相互排斥,致使悬线与
- 烹鱼时加入少量食醋和料酒可以使烹制的鱼具有特殊的香味,这种香味来自于 A.食盐 B.食醋中的乙酸
- 作为中国公民,依法行使政治权利,依法履行政治性义务,是我们政治生活的基本内容。对公民权利理解正确的是 ①公民的权利是法定
- 9、默写题(共9分,每空1分)(1)闻道有先后, ,如是而已。(韩愈《师说》) (2)故木受绳则直,
- (多选)细胞作为生命活动的基本单位,其结构和功能高度统一。下列有关叙述正确的是
- 3.根据图中农作物分布图分析影响南北农作物分布差异的主要因素是 (原创) A.降水 B.土壤 C.热量
- 下列说法中能体现唯物主义和唯心主义根本分歧的是 A.“气者,理之依也”与“人病则忧惧,忧惧则见鬼出” B.“天地之变,阴
- 1914年,夫兰克和赫兹在实验中用电子碰撞静止原子的方法,使原子从基态跃迁到激发态,来证明玻尔提出的原子能级存在的假设。
- 我们所使用的电冰箱、电扇、洗衣机等家用电器,其主要部件都是用电动机来工作的,那么电动机是根据下列哪种现象制成的
- 将正比例函数的图象向上平移3个单位,所得的直线不经过第 象限.
- The result was not the same ___they had expected , _____was
- (二)阅读下面这首诗,完成第7、8两小题。 霜天晓角·题采石蛾眉亭① 韩元吉② 倚天绝壁,直下江千尺。天际两蛾凝黛,愁与
- 你能在日历中圈出一个正方形,使正方形所圈出的4个数和为78吗?如果能,那么这4天分别是几号?如果不能,请说明理由。



