高一化学上学期上册试题
海洋中有丰富的资源,下图为海水利用的部分过程。下列有关说法正确的是

A.由反应①可知:相同温度下,NaHCO3的溶解度大于Na2CO3
B.通过电解MgCl2·6H2O晶体可以获得Mg单质
C.反应②的离子方程式为:Br2+SO2+2H2O=SO![]() +2Br—+4H+
+2Br—+4H+
D.粗盐中含有的Mg2+、SO![]() 等杂质离子,可通过依次加入BaCl2溶液、NaOH溶液、盐酸等试剂加以去除
等杂质离子,可通过依次加入BaCl2溶液、NaOH溶液、盐酸等试剂加以去除
如果你家里的食用花生油混有水份,你将采用下列何种方法分离( )
A、过滤 B、蒸馏 C、分液 D、萃取
在一密闭的2L容器里装有4 mol SO2和2 mol O2,在一定条件下开始反应生成SO3。2 min末测得容器中有3.6 mol SO2,试计算:
(1)2 min末SO3的浓度。
(2)2 min内SO2的平均反应速率。
(3)O2的转化率。
下列有关物质鉴别与除杂的方法描述错误的是
A.用稀盐酸除去铜粉中混有少量铁粉
B.只用一种试剂可以鉴别CuO粉末、炭粉、铁粉三种黑色粉末
C.用滤纸过滤除去溶液中的胶体粒子
D.用水可以鉴别四氯化碳和苯两种无色液体
工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2.下列说法错误的是( )
A.硫元素既被氧化,又被还原
B.氧化剂与还原剂的物质的量之比为2:1
C.相同条件下,每吸收10m3SO2就会放出2.5m3CO2
D.若生成2.24LCO2,则转移0.8mol电子
设NA为阿伏加德罗常数的值,下列说法正确的是
A.0.5mol Na2O2中阳离子数为NA,则阴离子数也为NA
B.1.0 mol·L-1的NaOH溶液中OH-的数目为NA
C.1molNa2O2与足量的CO2反应转移电子数为2 NA
D.标准状况下,18g H2O所含的分子数为NA
硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,制取硝酸铜现有三种设计方案可供选用:
①Cu与稀硝酸反应制取:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
②Cu与浓硝酸反应制取:Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O
③通氧气于铜屑与稀硝酸的体系中制取:2Cu+4HNO3+O2=2Cu(NO3)2+2H2O
下列说法正确的是( )
| A.制取相同量的硝酸铜需硝酸的量③最多 |
| B.制取相同量的硝酸铜①产生的有毒气体比②多 |
| C.三种方案中硝酸的利用率③>①>② |
| D.三种方案的反应都可以在铁制容器中进行 |
将一定体积的密度为1.19g /cm3,HCl的质量分数为36.5%的浓盐酸稀释到50mL,使溶液中HCl的物质的量浓度为1.19mol /L。计算所用浓盐酸的体积。
实验中的下列操作正确的是( )
A.取用试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中
B.把NaOH固体放在托盘天平左盘的滤纸上称量
C.用蒸发的方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干
D.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
取一定物质的量浓度的NaOH溶液100mL,然后向其通入一定量的CO2气体,得到溶液A,向A中逐滴缓慢加入0.1 mol•L-1的HCl溶液,产生的CO2气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示,通过计算回答:

(1)A溶液中的溶质为_________(化学式),其物质的量之比是_______。
(2)通入CO2气体体积__________________(标准状况)。
(3)NaOH溶液的物质的量浓度______________________。
四种基本反应类型与氧化还原反应的关系表述错误的是( )
A、化合反应不一定是氧化还原反应
B、分解反应不一定是氧化还原反应
C、置换反应一定是氧化还原反应
D、复分解反应一定是氧化还原反应
下列离子方程式正确的是
A.NaHSO4溶液中加入Ba(OH)2溶液至沉淀完全:SO42﹣+ H++ Ba2++ OH﹣═ BaSO4↓+ H2O
B.NaHCO3溶液中加入过量石灰水:2HCO3﹣+ Ca2++ 2OH﹣═ CaCO3↓ + 2H2O + CO32﹣
C.NaAlO2溶液中通入少量CO2:AlO2﹣+ CO2 + 2H2O ═ Al(OH)3↓ + HCO3﹣
D.Na2CO3溶液与醋酸溶液混合:2H+ + CO32﹣═ CO2↑ +H2O
已知铜片与浓硝酸可以发生如下反应:Cu+4HNO3=Cu(NO3)2+2X↑+2H2O对该反应的下列说法中正确的是( )
A.生成物X的化学式为H2
B.反应中N元素化合价改变的原子与N元素化合价不变的原子的个数比为1:1
C.浓硝酸属于纯净物
D.反应物Cu与生成物H2O的质量比为32:9
下列说法中正确的是
A.1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol·L-1
B.从1 L 2 mol·L-1的H2SO4溶液中取出0.5 L,该溶液的浓度为1 mol·L-1
C.配制500 mL 0.5 mol·L-1的CuSO4溶液,需62.5 g胆矾
D.中和100 mL 1 mol·L-1的H2SO4溶液,需NaOH 4 g
在2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O反应中
A. 氧化剂与还原剂的物质的量之比为1∶8
B. 氧化剂与还原剂的物质的量之比为5∶1
C. 氧化产物与还原产物的物质的量之比为5∶2
D. 氧化产物与还原产物的物质的量之比为2∶5
我国明代《本草纲目》中收载药物1892种,其中“烧酒”条目下写道:“自元时始创其法,用浓酒和糟入甑, 蒸
令气上……其清如水,味极浓烈,盖酒露也。”这里所用的“法”是指( )
A.萃取 B.过滤 C.蒸馏 D.分液
工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下,下列叙述正确的是( )
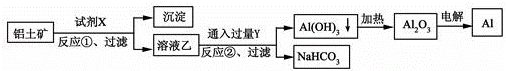
A.试剂X氢氧化钠溶液
B.反应①、过滤后所得沉淀为红褐色Fe2O3
C.图中所示转化反应都不是氧化还原反应
D.反应②的化学方程式为2NaAlO2+CO2+3H2O=2Al(OH)3↓+Na2CO3
下列电离方程式错误的是( )
A.KClO3![]() K++Cl-+3O2- B.H2SO4
K++Cl-+3O2- B.H2SO4![]() 2H++SO42-
2H++SO42-
C.Mg(NO3)2![]() Mg2++2NO3- D.Na2SO4
Mg2++2NO3- D.Na2SO4![]() 2Na++SO42-
2Na++SO42-
中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700℃时制造出纳米级金刚石粉末和氯化钠。该成果发表在世界权威的《科学》杂志上,立刻被科学家们高度评价为“稻草变黄金”。同学们对此有下列一些理解,其中错误的是( )
A.金刚石属于金属单质 B.制造过程中元素种类没有改变
C.CCl4是一种化合物 D.这个反应是置换反应
下列离子方程式书写正确的是( )
A.澄清石灰水与过量的小苏打溶液反应:Ca2++OH-+HCO![]() ===CaCO3↓+H2O
===CaCO3↓+H2O
B.明矾( KAl(SO4)2·12H2O )溶液中滴加Ba(OH)2溶液至SO![]() 恰好完全沉淀:
恰好完全沉淀:
Al3++Ba2++SO![]() +3OH-===BaSO4↓+Al(OH)3↓
+3OH-===BaSO4↓+Al(OH)3↓
C.将过量SO2通入冷氨水中:SO2+NH3·H2O===HSO![]() +NH
+NH![]()
D.小苏打溶液中加入醋酸溶液:HCO![]() +H+===CO2↑+H2O
+H+===CO2↑+H2O
- 电磁打点计时器是一种使用交流电源记录运动物体在一定时间间隔内位移的仪器,当电源频率为50 Hz时,振针每隔_______
- 下列有关实验原理或实验操作正确的是( ) A. 用广泛pH试纸测得饱和氯水的pH约为2 B. 用量筒量取7.60 mL
- 实验室需要0.80 mol·L-1 NaOH溶液475 mL 和0. 40mol·L-1硫酸500 mL。根据这两种溶液
- 正常情况下,甲胎蛋白(AFP)主要来自胚胎的肝细胞,胎儿出生后约两周AFP从血液中消失,但慢性肝炎、肝硬化患者的肝细胞再
- 写出下列名篇命局中的空缺部分 15.--------------------,月涌大江流。 16.出师一表真名世,---
- 将羧酸的碱金属盐溶液电解可得到烃类化合物。例如: 2CH3COOK(溶液)+2H2O 根据下列转化关系回答有关问题: C
- 适应经济全球化和加入世贸组织的新形势,在更大范围、更广领域和更高的层次上参与国际资源配置,拓宽发展空间,以开放促进改革和
- 12.名句名篇默写 (1)茕茕孑立,______________________。(《陈情表》) (2)本图宦达,___
- 15......
- 假定英语课上老师要求同桌之间交换修改作文,请你修改你同桌写的短文。短文中共有10处错误,每句中最多有两处。错误涉及一个单
- 读“南极图”,下列说法正确的是( )A.A为长城站,C是中山站,其中中山站在极圈内,有极昼极夜现象 B.E在印度洋
- 下列关于原电池的叙述中,正确的是( ) A.把电能转化为化学能,使溶液发生氧化还原反应 B.电子从活泼金属流向不活
- The map was drawn to the standard _____ of 1/100,000, so the
- 2010年春节前后,某市羊肉价格是每千克17元,西红柿价格虽比平时上涨,但每千克只有6元。羊肉之所以比西红柿贵,根本原因
- It is oftensaid that you cannot “teach an old dog new tricks
- 根据装置图回答问题.(1)图中标示①仪器的名称是 _________ . (2)实验室中既可以用来制取O2,又可以用来制
- 用伏安法测电阻时采用图14-7-7(a)和(b)两种线路,当用图(a)测量时,电压表和电流表的示数分别为U 1=5 V、
- 比较下列各组数的大小: (1)(2).
- 小明家冰箱冷冻室的温度为℃,调高4℃后的温度为A.4℃B.9℃C.℃D.℃
- 有媒体报道称,2009年,上海等地出现了类似豪华月饼的天价粽子。粽子以鲍鱼、鱼翅等为馅料,搭配名茶名酒,价格最高的一款粽



