高一化学上学期上册试题
某无色溶液中可能含有Na+、Ba2+、Cu2+、CO32-、Cl-、Mg2+中的一种或几种离子。
①向此溶液中滴加足量稀盐酸无明显现象。
②取少许①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生。
③取②的上层清液并加入足量的NaOH溶液,有白色沉淀产生。
(1)原溶液中一定含有的离子是________,一定不含有的离子是________,不能确定是否含有的离子是________。
(2)②中反应的离子方程式为___________________。
(3)若另取10mL①的溶液于锥形瓶中,然后向此溶液中逐滴加入NaOH溶液(如图甲所示)。滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示。

①OA段反应的离子方程式为_____________________。
②AB段反应的离子方程式为_______________________。
下图是某儿童微量元素体检报告单的部分数据:

根据上表![]() 数据,回答下列问题:
数据,回答下列问题:
(1)该儿童 元素含量偏低。
(2)报告单中“μmol/L”是 (填“质量”、“体积”或“浓度”)的单位。
(3)服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中体现维生素C的 (填“氧化性”或“还原性”)。
(4)缺铁性贫血患者应补充Fe2+。一些补铁剂以硫酸亚铁为主要成分,用硫酸亚铁制成药片时外表包有一层特殊的糖衣,推测糖衣的作用是 。
2.3g纯净的金属钠在干燥的空气中被氧化后得到3.5g固体,由此可判断其氧化产物是
A. 只有Na2O B. 只有Na2O2 C. Na2O和Na2O2 D. 无法确定
下列化学用语不正确的是
A.核素37Cl的中子数是20
B.16O和18O互为同位素
C.Na+的结构示意图: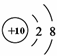
D.硫酸的电离方程式:H2SO4=2H+ + SO42-
由中学化学常见元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有下图所示
转化关系,A是由地壳中含量最多的金属元素组成的。请回答:

(1)写出下列物质的化学式:乙_______、丁_______、戊_______。
(2)写出甲物质在工业上的一种主要用途:______________________________。
(3)写出甲→乙+丙反应的离子方程式:______________________________________;
丁→戊反应的离子方程式:___________________________________________;
A→乙+C反应的化学方程式_____________________________________________。
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.1mol 铁和高温水蒸气完全反应转移的电子数为3NA
B.常温常压下,1mol 氦气含有的原子数为NA
C.标准状况下,11. 2 L 乙醇含有的分子数目为0. 5NA
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA
(1)483 g Na2SO4·10H2O中含O的物质的量为______mol,质量为_______g。
(2)9.8 g H2SO4的物质的量为________。
(3)0.25 mol CaCO3的质量为________。
(4)6.02×1022个H2O分子的质量为________。
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.强碱性溶液中:K+、Na+、CO32-、NO3-
B.加铝粉能产生大量H2的溶液中:Na+、NH4+、NO3-、Cl-
C.能使紫色石蕊变红的溶液中:Na+、A13+、SO42-、HCO3-
D.1.0 mol/LKNO3溶液:H+、Fe2+、Cl-、SO42-
下列各组中的两种物质作用时,反应条件(温度、反应物用量、反应物浓度等)改变,不会引起产物改变的是( )
A.Na2O2和CO2 B. NaOH和CO2 C.Na和O2 D.Cu和HNO3
铁及其化合物在日常生产生活中应用广泛,研究铁及其化合物的应用意义重大。
(1)所含铁元素只有还原性的物质是_________。
A.Fe B.FeCl2 C.FeCl3 D.Fe2O3
(2)当人体缺铁时,往往要吃补铁保健品。人体能够吸收的是+2价的铁,但是+2价的铁很容易被氧化。
①如何检验某固体补铁剂中铁元素已被氧化?写出操作过程、现![]() 象及结论。
象及结论。
答:_________________________________________________________________![]() ___。
___。![]()
②服用维生素C,可使食物中的三价铁离子转化为二价铁离子。由此可推知,维生素C具有________________(填化学性质)。
(3)工业上用氯化铁腐蚀铜箔、制造电路板。某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:

回答下列问题:
①试剂a是___________,操作I用到的玻璃仪器有烧杯、玻璃棒和___________。
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为___________。
③上述流程中操作III包括________________、________________、过滤、洗涤。
下列现象或事实不能用同一原理解释的是( )
A.SO2既能使氯水褪色,又能使酸性KMnO4溶液褪色
B.Cl2、SO2分别通入品红溶液中,品红均褪色
C.食盐水和氯水中滴加AgNO3溶液均产生沉淀
D.稀盐酸和氯水中加入小块CaCO3均产生气泡
下列金属的冶炼不适宜用热还原剂来冶炼的是( )
A.铁 B.铜 C. 钠 D.铅
某课外小组准备在实验室配制100mL1.0mol·L-1的硝酸溶液,然后再研究金属铜与硝酸的反应情况。
(1)配制100mL1.0mol·L-1的硝酸溶液,需要的仪器除烧杯、玻璃棒、量筒、胶头滴管外,还需要的玻璃仪器是 。
(2)若用10 mol·L-1的浓硝酸来配制上述溶液,需要量取浓硝酸的体积是 mL。
(3)配制过程中,若其他操作都正确,下列操作会引起浓度偏小的是 。
A.定容摇匀后发现液面低于刻度线,再加水至刻度线
B.定容时俯视容量瓶的刻度线
C.将溶液转入容量瓶后,没有洗涤烧杯和玻璃棒,就进行定容操作
D.容量瓶用蒸馏水洗涤后未烘干
(4)课外小组同学将制得的硝酸与铜片在下列装置中反应,反应初期观察到大试管中的液体a逐渐变为蓝色,试管上方有浅红棕色气体出现。

① 反应初期液体a逐渐变为蓝色是由于反应生成了 (填化学式)。
② 导致红棕色气体在试管c中颜色消失的反应方程式为 。
③ 你能否通过该实验初期现象得出1.0mol·L-1的硝酸与铜片反应直接生成红棕色NO2的结论? (填“能”或“不能”),理由是 。
下列各组物质不能实现直接转化的是( )
A. Mg→MgO→MgCl2→Mg(OH)2 B. Cu→CuCl2→Cu(NO3)2→Cu(OH)2
C. Fe→Fe3O4→Fe(OH)3→Fe2O3 D. Na→Na2O2→Na2CO3→NaCl
一只试管中NO、NO2、O2以不同的体积比混合,将试管倒立于一盛有足量水的水槽中,水能充满试管的是( )
A.1:1:2 B.9:6:1 C.8:4:7 D.4:2:3
将足量澄清石灰水加入250mL碳酸钠溶液中,过滤、干燥后得到10g沉淀。求此碳酸钠溶液的物质的量浓度。
某胶囊是一种常用的治疗胃酸过多的药品,其主要成分为一种两性氢氧化物。某同学欲对该胶囊内的白色固体的主要成分进行检验,设计了如下实验步骤:

(1) 操作Ⅱ所需要的玻璃仪器有_________、_________、________。
(2) 写出下列反应的方程式:
③的化学方程式:____________________________________________________,
④的离子方程式:______________________________________________________。
(3) 根据实验推测,该胃药的主要成分为_________________________________________。
(4) 该同学通过阅读课外读物了解到:常用胃药中除了上述实验已检出的物质外,还有NaHCO3,请你帮助该同学完成对滤液C中主要成分的探究实验(简要描述操作步骤):_____________________。
需要加入氧化剂才能实现下列反应的是( )
A.Cl2→Cl- B.H+→H2
C.MnO2→Mn2+ D.Zn→Zn2+
下列实验操作合理的是
A.称量 NaOH 固体时,将 NaOH 直接放在托盘里的纸上
B.用10 mL量筒量取5.2 mL盐酸
C.用托盘天平称取25.20 g 碳酸钠
D.用100 mL容量瓶配制50 mL 0.10 mol·L-1氯化钠溶液
人体中的钙主要以羟基磷酸钙[Ca10(PO4)6(OH)2]形式存在于牙齿和骨骼中,使牙齿和骨骼具有坚硬的结构支架。下列关于羟基磷酸钙的说法正确的是
A.羟基磷酸钙是一种碱 B.羟基磷酸钙是一种有机高分子化合物
C.羟基磷酸钙由5种元素组成 D.羟基磷酸钙中磷元素的化合价为+5价
- 下表为一台冷暖空调名牌上的有关数据,关于这台空调,下列说法正确的是[ ]A.若连续制冷半小时,空调消耗的电能为1
- 现代科技证明,适量饮用葡萄酒有助人体健康,葡萄酒中含有的白藜芦醇具有美容养颜之功效.下列关于白藜芦醇(C14H12O3)
- 党和政府的重大决策都要从人民群众的实践中吸取智慧、经受检验,都要依靠人民群众付诸实践、取得实效。这体现了: ①人
- 下列被称为“异端”思想家是( ) A、程颢 B、朱熹 C、李贽
- 已知函数是偶函数,其定义域为,则点的轨迹是
- 下列命题中正确的命题是……………………………………… ()A.若点P(a,2a)(a≠0)为角α终边上一点,则sinα=
- 河床沉积物经过漫长的地质作用,会逐渐变成沉积岩,这类沉积岩往往以砂岩为主,砂岩的抗侵蚀能力与其颗粒有关,颗粒越小,抗侵蚀
- 下列各句,没有语病的一句是 ( ) A.通过参加社会实践活动,使我们亲身体验到改革大潮的汹涌澎湃。 B.我想,卓
- 已知f(x)=,定义正数数列{an},a1=,=2anf(an)(n∈N*)(Ⅰ)证明数列{}是等比数列;(Ⅱ)令bn=
- 否定经典力学的绝对时空论,从本质上修正由狭隘经验建立起来的时空观,深刻揭示时间和空间的本质属性的是: A.狭义相对论
- 若室温下0.1mol·L-1NaX溶液中pH=9,则该溶液中发生水解反应的X-占全部X-的() A.0.01%
- 设NA表示阿伏加德罗常数,数值约为6.02×1023。下列说法正确的是 ( )A.2.4 g金属镁变成镁离子时
- 2011年12月10日晚,近10年来我国观测条件最好的一次月全食现身天宇。这是一次最美的月全食,我们可以看到一轮红彤彤的
- PM2.5是指大气中直径小于或等于2.5微米的颗粒物,PM2.5漂浮在空气中容易造成雾霾天气.为了减少PM2.5的排放,
- (09年东城区二模文)在总体为N的一批零件中抽取一个容量为30的样本,若每个零件被抽取的可能性为25%,则N的值为___
- 下列叙述正确的是()A.分子式相同,元素各百分含量也相同的物质是同种物质B.通式相同的不同物质一定属于同系物C.分子式相
- 一氢气球下系一小重物G,重物只在重力和绳的拉力F作用下做匀速直线运动,不计空气阻力和风力的影响,而重物匀速运动的方向如下
- 目前旅游已经成为中国家庭重要的休闲方式和消费方式。2012年十一期间,西安的王先生到海南旅游,按照消费目的分,旅游消费
- 如图2所示.下列说法正确的是 A.小鸟受到的重力与小鸟对树枝的压力是一对平衡力 B.小鸟对树枝的压力与树枝对
- 如图所示为一种质谱仪示意图,由加速电场、静电分析器和磁分析器组成。若静电分析器通道中心线的半径为R,通道内均匀辐射电场在



