硝酸的化学性质 知识点题库
将铜粉放入稀硫酸中,加热无明显现象发生,当加入下列一种物质后,铜粉的质量减小,溶液呈蓝色,同时有气体逸出,该物质是( )
A . Fe2(SO4)3
B . KNO3
C . Na2SO4
D . FeSO4
下列金属能跟酸反应生成氢气的是( )
A . Fe+H2SO4(稀)
B . Al+H2SO4(浓)
C . Ag+HCl(稀)
D . Zn+HNO3(稀)
在下列反应中,HNO3既表现出氧化性,又表现出酸性的是( )
A . H2S+2HNO3═S↓+2NO2↑十2H2O
B . CuO+2HNO3═Cu (NO3)2十H2O
C . 4HNO3  4NO2↑十O2↑十2H2O
D . 3Cu+8HNO3═3Cu (NO3) 2+2NO↑十4H2O
4NO2↑十O2↑十2H2O
D . 3Cu+8HNO3═3Cu (NO3) 2+2NO↑十4H2O
 4NO2↑十O2↑十2H2O
D . 3Cu+8HNO3═3Cu (NO3) 2+2NO↑十4H2O
4NO2↑十O2↑十2H2O
D . 3Cu+8HNO3═3Cu (NO3) 2+2NO↑十4H2O
类比是研究物质性质的常用方法之一,可预测许多物质的性质.但类比是相对的,不能违背客观实际.下列各说法中,正确的是( )
A . IVA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3
B . CH4是正四面体结构,则SiH4也是正四面体结构
C . 锂与氧气反应:4Li+O2═2 Li2O,则钠与氧气反应:4Na+O2═2Na2O
D . CaCO3与稀硝酸反应生成CO2 , 则CaSO3与稀硝酸反应生成SO2
常温下,下列溶液可用铁制或铝制容器盛装的是( )
A . 浓盐酸
B . 浓硝酸
C . 稀硫酸
D . 稀盐酸
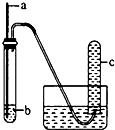
用如图装置实验,下列实验现象预期及相应结论均正确的是( )
a | b | 实验现象预期 | 结论 | |
A | 铜丝 | 浓硝酸 | 试管c中有大量红棕色气体 | 硝酸有强氧化性 |
B | 木条 | 18.4mol/L硫酸 | 木条变黑 | 浓硫酸有酸性及氧化性 |
C | 生铁 | NaCl溶液 | 导管处发生倒吸 | 生铁发生吸氧腐蚀 |
D | 铁丝 | 含少量HCl的H2O2溶液 | 试管c中有大量无色气体 | 该反应中铁作催化剂 |
A . A
B . B
C . C
D . D
在某100mL混酸中,硝酸的物质的量浓度为0.4mol•L﹣1 , 硫酸的物质的量浓度为0.2mol•L﹣1 . 向其中加入2.56g铜粉,微热,待充分反应后,溶液中Cu2+的物质的量浓度为( )
A . 0.15 mol•L﹣1
B . 0.3 mol•L﹣1
C . 0.225 mol•L﹣1
D . 无法计算
根据问题填空:
-
(1) 在浓硝酸中放入铜片,开始时反应的化学方程式为;待反应停止后,再加入少量质量分数为25%的稀硫酸,这时铜片上又有气泡产生,其原因是(用离子方程式表示).
-
(2) 常温下,将铁棒置于浓硫酸中,无明显现象,课本上解释为发生了钝化,但有人认为未发生反应.为验证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于CuSO4溶液中,若铁棒表面,则发生了钝化;若铁棒表面,则未发生反应.
-
(3) 制取硫酸铜有两种方法:方法一:2Cu+O2
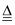 2CuO,CuO+H2SO4═CuSO4+H2O,方法二:Cu+2H2SO4(浓)
2CuO,CuO+H2SO4═CuSO4+H2O,方法二:Cu+2H2SO4(浓) 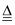 CuSO4+SO2↑+2H2O,方法一与方法二相比,其优点是(至少答两点):.
CuSO4+SO2↑+2H2O,方法一与方法二相比,其优点是(至少答两点):.
下列关于硝酸的认识中,正确的是( )
A . 浓、稀硝酸光照和受热都会分解
B . 浓硝酸与金属反应不放出氢气,而稀硝酸与金属反应可置换出氢气
C . 常温下,因为铝和铁不与浓硝酸反应,所以浓硝酸可盛放在铝制或铁制容器中
D . 铜分别与浓硝酸、稀硝酸反应生成NO2和NO,故稀硝酸的氧化性大于浓硝酸
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是( )
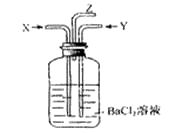
A . 洗气瓶中产生的沉淀是BaCO3
B . 在Z导管出来的气体中无CO2
C . 洗气瓶中产生的沉淀是BaSO3
D . 在Z导管口有红棕色气体出现
某小组对碳与浓硝酸的反应进行探究,已知:2NaOH+2NO2=NaNO3+NaNO2+H2O,2NaOH+NO2+NO=2NaNO2+H2O。请回答下列可题:
I.甲同学设计 如图所示装置制备并收集NO
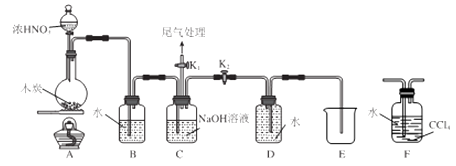
-
(1) 碳与浓硝酸反应的化学方程式为。
-
(2) C的作用为。
-
(3) 乙同学认为用装置F代替B更合理,理由为。
-
(4) 乙同学用改进后的装置进行实验。
①将浓HNO3滴入圆底烧瓶中的操作为。
②点燃A处酒精灯开始反应后,圆底烧瓶中的现象为。
-
(5) II.探究NO与Na2O2反应
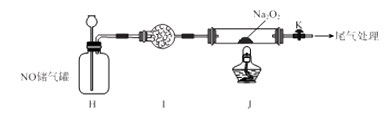
已知NaNO2既有氧化性,又有还原性;J 处硬质玻璃管中制得的NaNO2中含有少量NaNO3。
检验上图装置气密性的方法为。
-
(6) 实验结束后,设计实验证明J 处硬质玻璃管中有NaNO2生成。
供选试剂:蒸馏水KI-淀粉溶液,KMnO4溶液、NaOH溶液.BaCl2溶液、稀硫酸
聚合硫酸铁是一种新型高效净水剂。以黄铁矿(主要成分:FeS2,铁的化合价为+2价)烧渣(主要成分为Fe2O3、FeO、SiO2等)为原料制取聚合硫酸铁(铁的化合价为+3价)的实验步骤如下:
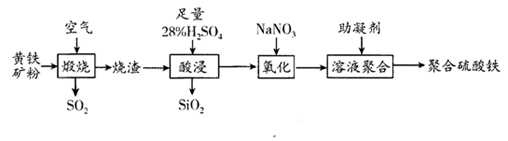
回答下列问题:
-
(1) “煅烧”过程发生反应的氧化产物是。
-
(2) 写出“酸浸”过程中发生反应的离子方程式。
-
(3) “氧化”过程中先产生无色气体,最终变成红棕色气体,写出加入NaNO3产生无色气体反应的离子方程式,若用H2O2代替NaNO3达到相同氧化效果,消耗H2O2和NaNO3的物质的量之比。
-
(4) 为确定产品是否合格,需测定聚合硫酸铁中Fe3+和SO42-的物质的量之比,测定时需要的试剂为___________ (填写序号)。A . FeSO4 B . BaCl2 C . NaOH D . NaCl
根据下列实验操作和现象所得到的结论正确的是 ( )
选项 | 实验操作和现象 | 结论 |
A | 向K2MnO4溶液(墨绿色)中加入醋酸,溶液逐渐变为紫色且有黑色沉淀 | 醋酸具有氧化性 |
B | 向Fe(NO3)2溶液中滴入HI和淀粉混合溶液,溶液变蓝 | 氧化性:Fe2+>I2 |
C | 向苯酚钠溶液中通入CO2 , 溶液变浑浊 | 结合H+能力: C6H5O->CO32- >HCO3- |
D | 将K2CrO4滴入AgNO3溶液至不再产生沉淀,再滴加相同浓度的Na2S溶液,沉淀由红棕色转化为黑色 | Ksp(Ag2CrO4)>Ksp(Ag2S) |
A . A
B . B
C . C
D . D
向100mL3mol/L的硫酸溶液中加入过量的锌粉发生反应,为了加快化学反应速率但又不影响生成氢气的总量,可向反应物中加入适量的( )
①K2SO4溶液 ②Na2CO3固体 ③水 ④NaNO3固体 ⑤CuSO4粉末 ⑥6mol/L的硫酸
A . ①② ③
B . ④⑤⑥
C . ③④⑤
D . 只有⑤
下列叙述错误的是( )
A . NH3易液化,液氨常用作制冷剂
B . 与金属反应时,稀HNO3可能被还原为更低价态,则稀HNO3氧化性强于浓HNO3
C . 铵盐受热易分解,因此贮存铵态氮肥时要密封保存,并放在阴凉通风处
D . 稀HNO3和活泼金属反应时得不到氢气
将Mg、Cu组成的2.64 g混合物投入到100 mL稀硝酸中完全溶解,并收集还原产物NO气体(还原产物只有一种)。然后向反应后的溶液中逐滴加入2 mol·L-1NaOH溶液,下图是生成沉淀的质量与滴入NaOH溶液体积间的关系图。以下说法错误的是( )
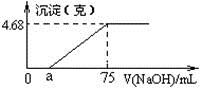
A . 稀硝酸的浓度为1.9 mol/L
B . 生成的NO在标况下的体积为0.896 L
C . a的值为15
D . Cu的物质的量为0.02 mol
对下列事实的解释错误的是( )
A . 高纯硅可制成计算机芯片,是利用其半导体性能
B . 浓硝酸在光照下颜色变黄,说明浓硝酸不稳定
C . 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有氧化性
D . 反应 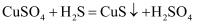 能进行,说明CuS既不溶于水也不溶于稀
能进行,说明CuS既不溶于水也不溶于稀 
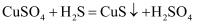 能进行,说明CuS既不溶于水也不溶于稀
能进行,说明CuS既不溶于水也不溶于稀 
下列说法不正确的是( )
A .  能导致“光化学烟雾”的形成
B . 浓硝酸可用铝槽车运输
C . 石灰石在高温下可用于消除燃煤烟气中的
能导致“光化学烟雾”的形成
B . 浓硝酸可用铝槽车运输
C . 石灰石在高温下可用于消除燃煤烟气中的  D . 氮气化学性质稳定,可将炽热的镁粉放在氮气中冷却
D . 氮气化学性质稳定,可将炽热的镁粉放在氮气中冷却
 能导致“光化学烟雾”的形成
B . 浓硝酸可用铝槽车运输
C . 石灰石在高温下可用于消除燃煤烟气中的
能导致“光化学烟雾”的形成
B . 浓硝酸可用铝槽车运输
C . 石灰石在高温下可用于消除燃煤烟气中的  D . 氮气化学性质稳定,可将炽热的镁粉放在氮气中冷却
D . 氮气化学性质稳定,可将炽热的镁粉放在氮气中冷却
下列反应既表现硝酸的氧化性,又表现硝酸的酸性的是( )
A .  B .
B .  C .
C . 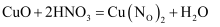 D .
D . 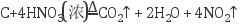
 B .
B .  C .
C . 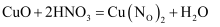 D .
D . 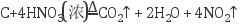
有某硫酸和硝酸的混合溶液20 mL,其中含硫酸的浓度为2mol·L-1 , 含硝酸的浓度为1mol·L-1 , 现向其中加入0.96 g铜粉,充分反应后(假设只生成NO气体),最多可收集到标准状况下的气体的体积为( )
A . 224 mL
B . 166 ml
C . 112 mL
D . 89.5mL
最近更新
- 已知定义在上的函数.则下列结论中,错误的是 (A)(B)函数的值域为 (C)对任意的,不等式恒成立 (D)将函数的极值由
- 一般人都是习惯于用右手写字,他们使用显微镜观察的正确做法为 ( ) A.双眼睁开注视镜筒
- 维生素C(化学式:C6H8O6)对人体皮肤和牙龈健康有重要作用,缺乏维生素C,会引起坏血病,中学生每天需要补充60mg维
- 若函数是偶函数,则的递减区间是 .
- 句型转换1. That is her new watch. (改为一般疑问句) _____ _____ her new
- 四种常见统计图名称 优点 条形图 能清楚地表示每个项目的具体⑨ . 扇形图 能直观地反映部分占总体的⑩
- 下列有关物质水解的说法正确的是 A.蛋白质水解的最终产物是多肽 B.淀粉水解的最终产物是葡萄糖 C.纤维素不能水解成
- 下表为长式周期表的一部分,其中的编号代表对应的元素。① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨ ⑩请回答下列问题: (1)表中属
- 关于加速度,下列说法正确的是 A.加速度表示物体运动
- 如图5-7-5所示,物体从高为h的斜面上的A点由静止滑下,恰好停在水平面上的B点.若使其从B点开始运动且能回到斜面上的A
- (16届湖南省长沙市麓山国际实验学校九年级上学期第一次限时训练)有关传统文化常识,下列说法错误的一项是( ) A.元
- 一块直角三角板放在两平行直线上,如图所示,∠1+∠2=___________度;
- 20世纪90年代初,某品牌移动电话每部售价1万多元人民币,年销售量不足1000部;随着信息技术的发展,移动电话功能日益完
- 下列词语中加点字读音正确的一组是 A.纰漏(pī) 同仇敌忾(kài) 审时度(duó
- 有关细胞中的有机物下列说法正确的是( ) A.含有元素C、H、0、N的物质是核酸、酶、果糖、脂肪 B.花生种子中没有
- 布袋中装有2个红球,3个白球,5个黑球,它们除颜色外均相同,则从袋中任意摸出一个球是白球的概率是__________.
- 在下列常用词语中字形完全正确的一项是 A.莫衷一是 意气用事 一衣戴水 不共戴天 B.通宵达旦 气冲霄汉 和言悦色 貌合
- 1948年、1962年美国与西欧在自由世界的黄金所占份额如下图,造成这种情况的原因是 A.经济危机导致美国经济实力下降
- .实验室内有一电压表〇mV ,量程为150mV,内阻约为 150Ω。现要将其改装成量程为10mA的电流表,并进行校准。为
- (16分) X、Y、Z、M、R、Q是短周期主族元素,部分信息如下表所示: X Y Z M R Q 原子半径/nm



