硝酸的化学性质 知识点题库
-
(1) 美蓝是亚硝酸盐中毒的有效解毒剂,下列说法正确的是 .(选填编号)
a.解毒时美蓝表现氧化性b.中毒时亚硝酸盐发生氧化反应
c.解毒时高铁血红蛋白被还原d.中毒过程中血红蛋白显氧化性
-
(2) NaNO2中钠离子核外有 种不同能级的电子,三种元素对应的简单离子半径由大到小的顺序为
-
(3) Na、N、O分别与H形成的简单化合物中熔点最高的是 (填化合物化学式),试解释原因
-
(4) 已知NaNO2能发生如下反应(未配平):NaNO2+HI→NO+I2+NaI+H2O当有0.75mol HI被氧化时,在标准状况下产生气体的体积是 L.
-
(5) 有人将26中反应产生的NO收集到一个固定容积的密闭容器中,并在常温下将其压缩到1.01×107Pa,然后加热至50℃时,发现气体的压力迅速下降.当温度恢复到常温,压强降至略小于1.01×107Pa的
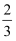 时,就不再改变.已知此过程中有一种产物是N2O.请写出生成N2O的反应方程式: .解释最后的气体压强略小于1.01×107Pa的
时,就不再改变.已知此过程中有一种产物是N2O.请写出生成N2O的反应方程式: .解释最后的气体压强略小于1.01×107Pa的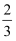 原因:
原因:
-
(6) 某工厂的废液中含有2%~5%的NaNO2直接排放会造成污染,下列试剂中①NaCl、②NH4Cl、③HNO3、④浓H2SO4 , 能使NaNO2转化为N2的是 .(选填编号)
-
(1) 写出下列反应的化学方程式:
①工业制漂白粉:;
②氯化亚铁溶液中通入氯气:.
-
(2) 写出下列反应的离子方程式:
③铁粉溶于稀硫酸:;
④稀硝酸与铜片的反应:.
①浓硝酸中滴入石蕊试液并微热
②氧化亚铁与浓硝酸反应
③氢氧化铝与浓硝酸反应
④碳与浓硝酸.
-
(1) 写出硝酸工业生产中相关的三个化学方程式:,,;
-
(2) 铝片与氢氧化钠溶液反应的离子方程式;
-
(3) 明矾溶液与过量氢氧化钡溶液反应的离子方程式;
-
(4) 在偏铝酸钠溶液中通入足量二氧化碳气体的离子方程式.
-
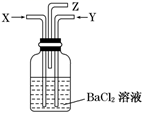
(1) 甲同学欲探究铜与稀硝酸反应产生的气体主要是NO,设计装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹(处于关闭状态),F是含有一半空气的注射器。
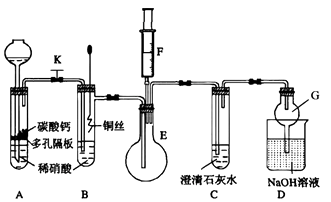
请回答有关问题:
①装置A中进行反应时打开止水夹K,当装置C中时,关闭止水夹K,试分析这样操作的目的是,A中反应的离子方程式为。
②在完成①中的“操作”后,将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是,B中反应的离子方程式为。
③为进一步证明产物是NO,将注射器F中的空气推入E中,看到的现象是。
④装置G的作用是。
-
(2) 同学们发现铜与稀、浓硝酸反应所得溶液的颜色不同,并记录如下:
将1 g细铜丝放入盛有10 mL的1 mol·L-1 HNO3溶液的试管中加热
铜丝表面有无色气体逸出,溶液变为天蓝色
将1 g细铜丝放入盛有10 mL的14 mol·L-1HNO3溶液的试管中
产生大量红棕色气体,溶液变为绿色,绿色由深到浅,未见到蓝色
有同学认为是铜与浓硝酸反应的溶液中溶解了生成的气体,也有同学认为是溶液中剩余硝酸浓度较大所致,同学们分别设计了以下4个实验来判断该看法是否正确,以下方案中可行的是(选填序号字母)。
a. 向上述绿色溶液中通入氮气,观察颜色变化
b. 加水稀释上述绿色溶液,观察颜色变化
c. 向饱和的硝酸铜溶液中不断滴加14 mol·L-1HNO3溶液
d. 向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化
 Cu(NO3)2
B . Cu
Cu(NO3)2
B . Cu 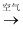 CuO
CuO 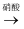 Cu(NO3)2
C . Cu
Cu(NO3)2
C . Cu 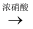 Cu(NO3)2
D . Cu
Cu(NO3)2
D . Cu 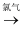 CuCl2
CuCl2  Cu(NO3)2
Cu(NO3)2
| 选项 | 实验操作 | 实验现象 | 实验推论 |
| A | 向某溶液中加入 | 未产生能使湿润红色石蕊试纸变蓝的气体 | 原溶液中不含有 |
| B | 测定饱和 | 前者 | |
| C | 向红热的木炭滴加浓硝酸 | 产生大量的红棕色气体 | 木炭和浓硝酸反应生成 |
| D | 向 | 有白色沉淀生成,四氯化碳层呈紫色 | 白色沉淀可能为 |
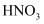 说法错误的是( )
说法错误的是( )
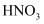 分解产生的
分解产生的  会溶解在其中
B . 将
会溶解在其中
B . 将 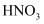 分解产生
分解产生  与
与  ,比值为
,比值为 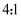 ,若将带火星的木条伸入该混合气体内,木条复燃,说明
,若将带火星的木条伸入该混合气体内,木条复燃,说明  也支持燃烧
C . 常温下,
也支持燃烧
C . 常温下,  和
和 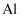 遇到浓硝酸会发生“钝化”,因此可以用
遇到浓硝酸会发生“钝化”,因此可以用  制容器来储存浓硝酸
D . 浓盐酸和浓硝酸体积按
制容器来储存浓硝酸
D . 浓盐酸和浓硝酸体积按 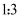 混合,可以得到“王水”
混合,可以得到“王水”
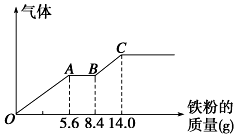
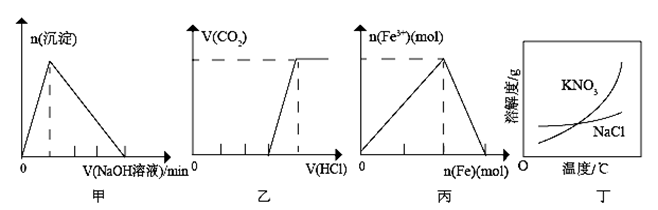
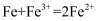 C . C点之后的溶液中溶质只有
C . C点之后的溶液中溶质只有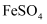 D . 原混合溶液中
D . 原混合溶液中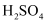 的浓度为1.5mol/L
的浓度为1.5mol/L
- 下列说法不正确的是( )。A.用石灰水可以区别Na2CO3和NaHCO3B.Na2CO3比NaHCO3易溶于水
- 读我国部分地区春季某时天气系统图,完成 8~10 题。8.图中甲、乙、丙、丁四条线中,能形成暖锋的是 A.甲、丙
- 如图6所示,两个底面积不同的圆柱形容器A和B(SA>SB),容器足够高,分别盛有甲、乙两种液体,且两种液体对容器底部的压
- 发射“神舟六号”飞船的火箭所用燃料燃烧时的化学方程式为 ,则R的化学式为 (
- 杜牧《上李太尉论江贼书》载:“凡江淮草市,尽近水际,富室大户,多居其间。自十五年来,江南江北,凡名草市,劫杀皆遍,只有三
- 后人哀之而不鉴之, (《阿房宫赋》)
- 下列哪个函数的图象不是中心对称图形 A、 B、 C、 D、
- 阅读下面这首诗,完成小题。 蝶恋花·别范南伯 宋·杨炎正 离恨做成春夜雨。添得春江,刬地东流去。弱柳系船都不住,为君愁
- “欲平天下者必先治其国,欲治国者必先齐其家,欲先齐家者必先修其身,欲修身者必先正其心”。《大学》中的这一观点告诉我们(
- 实验室需配制一定浓度的硝酸钾溶液。 (1)查阅硝酸钾溶解性。由右图可知,20 ℃时,硝酸钾的 溶解度为 g
- 有一条多肽链,分子式为CxHyOpNqS,将它彻底水解后,只得到下列四种氨基酸:分析推算可知,水解得到氨基酸个数为 A.
- 阅读下面的文言文,完成5~9题。 (高)允好切谏,朝廷事有不便,允辄求见,帝常屏左右以待之。或自朝至暮,或连日不出;群臣
- 已知方程的两根为,且,则的值为( ) (A) (B)
- Some language experts think we learn languages in the same
- It’s a fine day. Let’s go swimming, _____? A.won’t we B.
- 读下图回答C、D周边地区农业生产共同的有利区位条件是①地势平坦,耕地集中连片 ②热量充足 ③工业基础好 ④地
- 下列关于细胞衰老的叙述中,错误的是() A.细胞的衰老是一种正常的生命现象 B.衰老细胞的体积缩小,核体积增大 C.衰老
- ---________arethese cars made by? ---Tom A.Where B
- 上右图是菜粉蝶发育过程中的四个时期的示意图:请分析回答:(9分)(1)、图中数字代码1是 ,2是
- 若则在上的投影是 .
 溶液
溶液
 溶液和饱和
溶液和饱和  溶液的
溶液的  值
值 的水解程度小于
的水解程度小于 
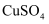 溶液中加入
溶液中加入  溶液,再加入四氯化碳振荡
溶液,再加入四氯化碳振荡