硝酸的化学性质 知识点题库
据各地报纸报导,在一些建筑工地的食堂里,常发生将工业用盐当作食盐用,引起工人食物中毒的现象,该工业用盐对人有致癌作用.这种盐的化学式是( )
A . MgCl2
B . NaCl
C . NaNO2
D . NaNO3
对人体健康不会造成危害的是( )
A . 用工业盐(NaNO2)作咸味调味品
B . 用富尔马林(35%~40%甲醛水溶液)浸泡海产品,防腐保鲜
C . 食盐中加入一定量的碘酸钾(KIO3)制食用含碘盐
D . 将含有甲醇(CH3OH)的工业酒精兑制成饮用白酒
下列物质误食后不会引起中毒的是( )
A . BaSO4
B . NaNO2
C . CH3OH
D . P4
氢气还原氧化铜所得的红色固体可能是铜与氧化亚铜的混合物,已知Cu2O在酸性溶液中可发生自身氧化还原反应,生成Cu2+和单质铜.
-
(1) 现有8克氧化铜被氢气还原后,得到红色固体6.8克,其中含单质铜与氧化亚铜的物质的量之比是
-
(2) 若将6.8克上述混合物与足量的稀硫酸充分反应后过滤,可得到固体 克
-
(3) 若将6.8克上述混合物与一定量的浓硝酸充分反应,
①生成标准状况下1.568升的气体(不考虑NO2的溶解,也不考虑NO2与N2O4的转化),则该气体的成分是 ,其物质的量之比是 ;
②把得到的溶液小心蒸发浓缩,把析出的晶体过滤,得晶体23.68.经分析,原溶液中的Cu2+有20%残留在母液中.求所得晶体的化学式为
常温下,下列物质可以用铝制容器盛装的是( )
A . 氢氧化钠溶液
B . 稀硫酸
C . 浓盐酸
D . 浓硝酸
某化学兴趣小组进行了有关Cu、硝酸、硫酸化学性质的实验,实验过程如图所示.下列有关说法正确的是( )
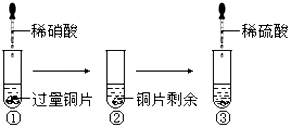
A . 实验①中溶液呈蓝色,试管口有红棕色气体产生,说明稀硝酸被Cu还原为NO2
B . 实验③中滴加稀硫酸,铜片继续溶解,说明稀硫酸的氧化性比稀硝酸强
C . 实验③发生反应的化学方程式为:3Cu+Cu(NO3)2+4H2SO4═4CuSO4+2NO↑+4H2O
D . 由上述实验可得出结论:Cu在常温下既可以和稀硝酸反应,也可以和稀硫酸反应
某固体物质和某溶液在一定条件下反应,产生气体的相对分子质量(平均相对分子质量)为45,则发生反应的物质一定不可能是( )
A . Zn和浓H2SO4
B . C和浓HNO3
C . Cu和浓HNO3
D . Na2O2和NH4Cl浓溶液
在浓硝酸中放入铜片:
①开始反应的化学方程式为.
②若铜有剩余,则反应将要结束时的反应的离子方程是:
③待反应停止后,再加入少量的25%的稀硫酸,这时铜片上又有气泡产生,其原因是.
下列叙述不正确的是( )
A . NH3易液化,液氨常用作制冷剂
B . 稀HNO3氧化能力弱于浓HNO3
C . 贮存铵态氮肥时要密封保存,并放在阴凉处
D . 硝酸只能被Zn、Fe等金属还原成H2
简要回答下列问题.
-
(1) 浓硝酸需保存在棕色试剂瓶中,原因是
-
(2) 可以用食醋除热水瓶胆内的水垢[主要成分CaCO3、Mg( OH)2 , 原因是
-
(3) 3月22日是“世界水日”,保护水环境,珍爱水资源是每个公民的责任和义务.请你提出一种有利于保护水资源的措施.
下列试剂中,标签上应标注  和
和  的是( )
的是( )
 和
和  的是( )
的是( )
A . C2H5OH
B . HNO3
C . NaOH
D . HCl
向200 mL 2 mol·L-1 HNO3溶液中,逐渐加入铁粉至过量(假设生成的气体只有一种),在此过程中,n(Fe2+)随n(Fe)变化如右图所示。下列有关说法正确的是( )
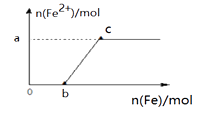
A . 当0<n(Fe)≤b时,向所得的溶液中加入KSCN溶液没有血红色出现
B . 向c点处的反应液中加入稀盐酸后无明显现象
C . 当加入铁粉n mol时(0.1<n<0.15),溶液中n(Fe3+)=(0.3-2n)mol
D . 图中a=0.15 、b =0.15
将铜粉放入稀硫酸中,加热后无明显现象,但当加入某物质后,铜粉质量减少,溶液呈蓝色且有气体逸出,此物质是( )
A . Na2CO3
B . KNO3
C . NaOH
D . HCl
在稀硫酸中加入铜粉,铜粉不溶解,再加入下列固体粉末,铜粉可以溶解的是( )
A . Fe
B . Na2SO4
C . KNO3
D . FeCl2
下列现象或事实能够用相同的原理解释的是( )
A . NaOH、FeSO4在空气中放置变质
B . 氯水、Agl密封保存在棕色试剂瓶中
C . SO2使品红和酸性KMnO4液褪色
D . 常温下浓硝酸不能溶解Al和Au(金)
下列说法错误的是( )
A . 蓝色的CoCl2溶液加浓盐酸可以变为红色
B . 含苯环的蛋白质与浓硝酸作用会产生黄色固体
C . 加热MgCl2·6H2O可以制得Mg(OH)Cl
D . 纤维素溶解在铜氨溶液中,然后压入稀酸可得铜氨纤维
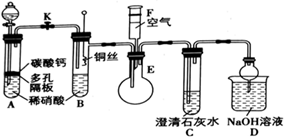
某校课外活动小组为了探究铜与稀硝酸反应产生的气体是否为NO,设计了如下实验。实验装置如图所示(已知NO、NO2能与NaOH溶液反应):
-
(1) 设计装置A的目的是:,写出试管A中发生的离子方程式:。
-
(2) 在(1)中的操作后将装置B中铜丝插入稀硝酸,并微热,观察到装置B中的现象是:;B中反应的离子方程式是:;
-
(3) 将注射器F中的空气推入E中,E中的气体变为红棕色,此时发生的化学方程式:;
-
(4) D装置的作用是:。
下列实验操作、现象及结论均正确的是( )
| 实验操作和现象 | 实验结论 | |
| A | 将惰性电极插入氢氧化铁胶体中,通电一段时间后,阴极区红褐色加深 | 氢氧化铁胶体带正电荷 |
| B | 向饱和食盐水中依次通入足量 | 该条件下溶解度: |
| C | 将苯加入到橙色的溴水中,充分振荡后静置,下层液体几乎无色 | 苯与 |
| D | 铜片投入到稀硫酸中,加热无明显现象;再加入少量硝酸钾固体,溶液变蓝色 | 硝酸钾起催化作用 |
A . A
B . B
C . C
D . D
将32.0g的Cu片投入到150mL某浓度的HNO3溶液中,恰好完全反应,共收集到11.2L(标准状况下)NO2和NO的混合气体,则该HNO3的物质的量浓度为( )
A . 10.0moL/L
B . 6.70mol/L
C . 13.3mol/L
D . 8.60mol/L
硫酸和硝酸都是重要的化工原料,具有广泛的用途。
-
(1) 蔗糖中加入浓硫酸后,蔗糖变黑且体积膨胀,同时有刺激性气味的气体产生。该变化过程中体现了浓硫酸的,产生气体的化学方程式为。
-
(2) 某同学进行有关铜的化学性质的实验,如图所示:
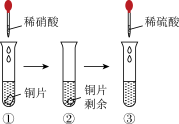
实验①可观察到的现象为(尽可能描叙完整);实验③中铜片逐渐溶解至消失,该同学认为铜与稀硫酸和稀硝酸均能反应,这种看法(填“合理”或“不合理”);试剂药品不变,请补充一个实验加以证明:(画出图示并写出预期现象)。根据补充实验的结论,写出③中铜片溶解的离子方程式。
-
(3) 如图所示,A是能使湿润的红色石蕊试纸变蓝的气体;C、D均为空气的主要成分;E是一种有毒气体能与血红蛋白结合,反应II在三元催化器催化作用下常用于汽车尾气的转化。
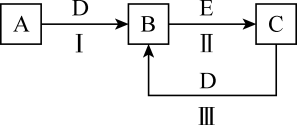
①写出实验室制A的化学方程式:。A在生产生活中有广泛的用途,写出其中的一个用途:。
②写出反应I的化学方程式;
③写出反应II的化学方程式。
最近更新
- 下列有关生物固氮的描述错误的是 A.豆科植物的根瘤是发生固氮作用的部位 B.土壤中独立生活的根瘤菌也能固氮 C.不同的根
- Are yousure ________ Mr. Li will come to your birthday
- I want to leave now; I can’t ____ nothing useful here. A. st
- 广东首部非遗主题微电影《鹤无双》上映,该剧以国家级非物质文化遗产三灶鹤舞为题材,讲述了爷孙两间的鹤舞传承故事,将历史与个
- 金属铜与人体分泌物中的盐酸以及子宫内的空气反应可生成超氧酸:Cu+HCl+O2=CuCl+HO2 HO2 (超氧酸)不
- 下面加点词语的读音全都正确的一项是() A. 荫(yìn)凉 熨(yù)帖 逢场(chǎng) 嘈(cāo)
- 形成地形雨、锋面雨和对流雨都需要具备的三个条件是: ①空气中有足够水汽 ②空气中有足够凝结核 ③空气中的水平运动
- 下列做法不会对人体健康造成损害的是 A、多吃水果和蔬菜 B、食用甲醛浸泡过的水产品 C、食用
- 函数y=log(x2-6x+17)的值域是
- 在光滑的绝缘水平面上放着带电小球甲和乙 ,若它们带电量的关系是q甲 = 4q乙,质量的关系是m甲=3m乙,则它们在库仑力
- 盐城市大丰裕华是闻名的“大蒜之乡”。大蒜是常见的调味品之一,大蒜中主要成分大蒜素具有消毒杀菌作用。大蒜素的化学式为C6H
- 从一副扑克牌(没有大小王)的52张牌中任取2张,求:(1)两张是不同花色牌的概率;(2)至少有一张是红心的概率.
- 上海是我国最大的工业城市,下列属于上海新兴工业部门的是A.机械、纺织 B.电子、化工 C.冶金、航空
- 已知抛物线y2=4x与直线x+y-2=0的交点为A、B,抛物线的顶点为O,在抛物线弧AOB上求一点C,使△ABC的面积最
- 在平面内,若直线a⊥c,直线b⊥c,则a∥b;在空间中,若直线a⊥c,直线b⊥c,则直线a与直线b不一定平行。这说明 A
- As we speddown the highway ,the lights of the city ________
- 语言运用题 阅读下面材料,在下列空白处填入适当的句子 画家早年颠沛流离,吃尽了人世的苦头。但中年以后却事业成功,名声日隆
- “入山见木,长短无所不知;入野见草,大小无所不识。然而不能伐林以作屋,采草以和药,此知草木所不能用也”。造成上述现象的根
- (本题满分8分)计算:1.(1) 2.(2)
- 下列说法正确的是 选项 实验 解释或结论 A 用洁净的Pt蘸取某溶液进行焰色反应,火焰呈黄色 该溶液中一定含有Na+,无
 、
、  ,有大量晶体析出
,有大量晶体析出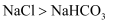
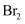 发生了取代反应
发生了取代反应


