物质的量的相关计算 知识点题库
物质的量相同的两种气体,在相同条件下,则它们必然( )
A . 具有相同数目的原子
B . 都占22.4L
C . 具有相同数目的分子
D . 具有相同摩尔质量
下列说法正确的是( )
A . 28 g氮气含有的原子数为NA
B . 4g金属钙的物质的量为1mol
C . 1 mol O2分子的质量等于1 mol氧原子的质量
D . 24 g O2分子和24 g O3分子所含的氧原子数目相等
同温同压下,有两瓶体积相等的CO和CO2 , 这两种气体中所含的分子数目之比为,所含的O原子数目之比为,所含的原子总数目之比为,所含的电子数目之比为,质量比为.
按要求填空:
-
(1) 0.5molSO2共约含有个原子,它与 gSO3所含硫原子数相等.
-
(2) 有100mL0.2mol/L的NaOH溶液,将此溶液稀释到200mL,则稀释后溶液中Na+的物质的量浓度是.
-
(3) 相同条件下,相同体积的 ①HCl、②NH3、③CO2、④O2四种气体中,含有电子数目由小到大的是(填序号).
下列有关物理量与其相应的单位不一致的是( )
A . 摩尔质量:g /mol
B . 气体摩尔体积:L/mol
C . 物质的量浓度:L/mol
D . 物质的量:mol
设NA表示阿伏加德罗常数,下列叙述中正确的是 ( )
A . 标准状况下,2.24 L H2O所含的原子数为0.5NA
B . 1mL 1mol/L NaCl溶液中离子总数为2NA
C . 18 g的H2O中含有的原子数为3NA
D . 标准状况下,22.4L氦气所含原子数为2 NA
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A . 28g CO所占的体积为22.4L
B . 1L 1mol/L HCl溶液中含有HCl分子为NA个
C . 标准状况下,2.24L水中约含有NA个氧原子
D . 标准状况下22.4LCO和CO2的混合气体中含碳原子数为NA
如图所示,①和②为两个体积相同的固定容器,图中“○”和“  ”分别表示氢原子和氧原子,则下列说法正确的是( )
”分别表示氢原子和氧原子,则下列说法正确的是( )
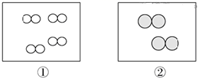
A . H2、O2均能发生化合反应,但不能发生置换反应
B . ①和②中气体的质量之比为1∶8
C . 若①中的H2为1 mol,则②中所含原子总数为3.01×1023个
D . 两容器的温度和压强均相同
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A . 标准状况下,33.6 L氯化氢中含有氯原子的数目为1.25NA
B . 1 L 0.1 mol·L-1的H2S溶液中,含S2-的数目为0.1NA
C . 通常状况下,2.24 L NO2和N2O4的混合气体中氮原子和氧原子数之比为1∶2
D . 将含有0.1 mol FeCl3的饱和溶液滴入沸水中,生成的胶体中含胶体粒子的数目为0.1NA
下列说法错误的是( )
A . 6.02×1023就是阿伏加德罗常数
B . 0.012kg12C含有的碳原子数就是阿伏加德罗常数的值
C . 某物质含有阿伏加德罗常数个粒子,则其物质的量是1mol
D . 1molNH3所含原子数约是2.408×1024
向100mLNaOH溶液中缓慢通入一定量的CO2气体,充分反应后,在减压低温下蒸发溶液,得到白色固体。请回答下列问题:
-
(1) 由于CO2通入量不同,所得到的白色固体的组成也不同,试推断有几种可能的组成,并分别列出。
-
(2) 若通入CO2气体为2.24L(标准状况下),得到9.5g的白色固体。
①请通过计算确定此白色固体组成为。
②所用的NaOH溶液的物质的量浓度为mol·L-1。
设NA为阿伏加德罗常数的值下列说法正确的是( )
A . 0.1mol羟基中含有的电子总数为NA
B . 22.4L(标准状况)丁烷完全裂解,生成乙烯分子的数目为NA
C . 0.1molCO(NH2)2完全燃烧生成N2、CO2和H2O转移的电子数为0.6NA
D . 0.1mol乙酸乙酯在稀硫酸催化下充分水解.生成乙醇分子的数目为0.1NA
设NA为阿伏加德罗常数的值。下列说法中正确的是( )
A . 12g金刚石中含有C-C的个数为4NA
B . 124g白磷(P4)晶体中含有P-P的个数为6NA
C . 28g晶体硅中含有Si-Si的个数为2NA
D . SiO2晶体中1mol硅原子可与氧原子形成2NA个共价键(Si-O)
设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
A . 1L0.1mol·L-1Na2SO3溶液中阴离子数目为0.1NA
B . 9.2gC2H6O含有共价键的数目为1.6NA
C . NA个CO2分子形成的晶体中电子对数目为4NA
D . 1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去电子数为2NA
标准状况下,V L某气体(此气体不与水反应)溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为 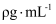 ,溶质的摩尔质量为
,溶质的摩尔质量为 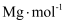 ,溶质的质量分数为w,溶质的物质的量浓度为
,溶质的质量分数为w,溶质的物质的量浓度为 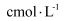 ,溶液的体积为
,溶液的体积为  ,下列关系中正确的是( )
,下列关系中正确的是( )
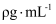 ,溶质的摩尔质量为
,溶质的摩尔质量为 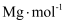 ,溶质的质量分数为w,溶质的物质的量浓度为
,溶质的质量分数为w,溶质的物质的量浓度为 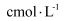 ,溶液的体积为
,溶液的体积为  ,下列关系中正确的是( )
,下列关系中正确的是( )
A . 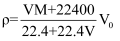 B .
B . 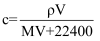 C .
C . 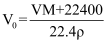 D .
D . 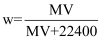
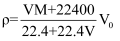 B .
B . 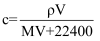 C .
C . 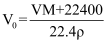 D .
D . 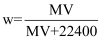
同温同压下,等质量的SO2和CO2相比较,下列叙述中正确的是( )
A . 物质的量之比为1:1
B . 体积之比为11:16
C . 氧原子数之比为1:1
D . 密度之比为11:16
粉煤灰是从煤燃烧后的烟气中收捕下来的细灰,主要成分有  、
、  、
、  和
和  等物质。综合利用粉煤灰不仅能够防止环境污染,还能制得纳米
等物质。综合利用粉煤灰不仅能够防止环境污染,还能制得纳米  等重要物质,流程如图:
等重要物质,流程如图:
 、
、  、
、  和
和  等物质。综合利用粉煤灰不仅能够防止环境污染,还能制得纳米
等物质。综合利用粉煤灰不仅能够防止环境污染,还能制得纳米  等重要物质,流程如图:
等重要物质,流程如图: 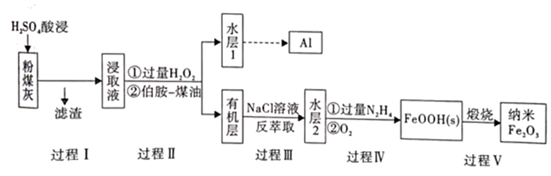
(查阅资料)①伯胺 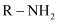 能与
能与  发生反应:
发生反应:
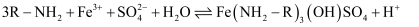 ,生成易溶于煤油的产物。
,生成易溶于煤油的产物。
②  在水溶液中能与
在水溶液中能与  发生反应:
发生反应: 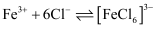 。
。
-
(1) “酸浸”过程中
 发生反应的离子方程式为;滤渣的主要成分是(填化学式)。
发生反应的离子方程式为;滤渣的主要成分是(填化学式)。
-
(2) 过程II中,加入过量
 的作用是(用离子方程式表示)伯胺-煤油可对浸取液进行分离,该操作的名称是。
的作用是(用离子方程式表示)伯胺-煤油可对浸取液进行分离,该操作的名称是。
-
(3) 利用化学平衡知识分析:用NaCl溶液进行反萃取的原理是。
-
(4) 过程IV中过量的
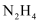 可将水层2中的
可将水层2中的  转化为
转化为  ,得到的
,得到的  再被
再被  氧化为FeOOH,其中第一步的离子方程式为
氧化为FeOOH,其中第一步的离子方程式为  (未配平),该反应中氧化剂与还原剂的物质的量之比为。
(未配平),该反应中氧化剂与还原剂的物质的量之比为。
-
(5) 测定产品纳米
 中的含铁量:将纳米
中的含铁量:将纳米  溶于过量酸中加热,先用过量的
溶于过量酸中加热,先用过量的 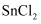 将
将  还原成
还原成  ,再加入
,再加入 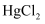 溶液除去过量的
溶液除去过量的 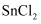 ,然后用标准
,然后用标准  溶液(已加入指示剂)滴定溶液中的
溶液(已加入指示剂)滴定溶液中的  。此过程发生的部分反应为:
。此过程发生的部分反应为: 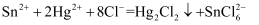 ;
; 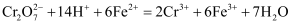 。
。 ①用
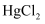 除去过量的
除去过量的 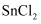 的目的是。
的目的是。②若称取纳米
 的质量为5.00g,配成100.0mL溶液,取出20.00mL,经上述方法处理后,再用0.1000
的质量为5.00g,配成100.0mL溶液,取出20.00mL,经上述方法处理后,再用0.1000 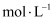
 标准溶液滴定,达到滴定终点时,消耗标准溶液20.00mL,则产品中铁元素的质量分数为。
标准溶液滴定,达到滴定终点时,消耗标准溶液20.00mL,则产品中铁元素的质量分数为。
60.8g铁和氧化铁的混合物恰好能完全溶解在500mL 2mol/L稀硫酸中,向反应后的溶液中加入KSCN溶液,无明显现象。试求:
-
(1) 混合物中铁元素的质量分数是多少?(计算结果保留一位小数)
-
(2) 反应过程中是否有氢气产生?若有,计算在标准状况下的体积是多少L,若无,通过计算说明理由。
含苯酚的工业废水处理的流程图如下图所示。下列说法正确的是( )
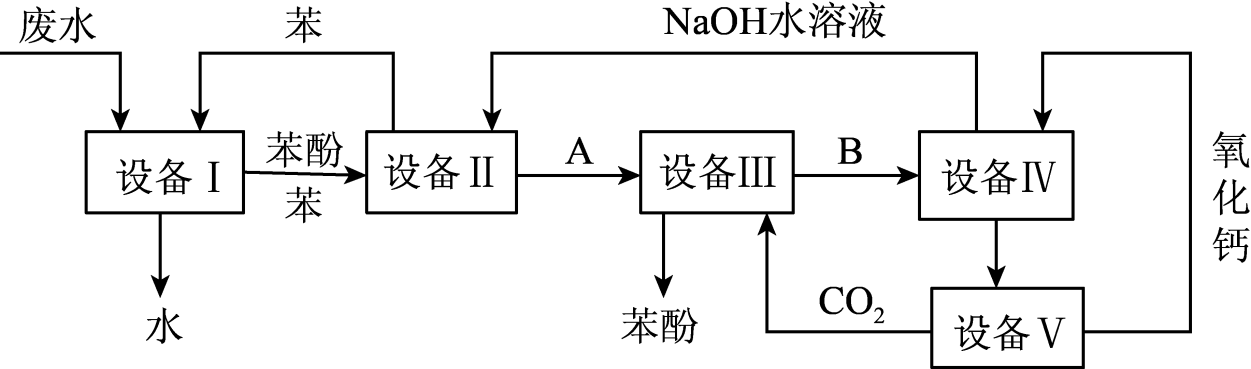
A . 上述流程里,设备I中进行的操作是萃取、分液,设备III中进行的操作是过滤
B . 图中能循环使用的物质是苯、CaO、CO2和NaOH
C . 在设备IV中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和CaCO3
D . 由设备II进入设备Ⅲ的物质A是C6H5ONa,由设备Ⅲ进入设备Ⅳ的物质B是Na2CO3
把3mol NO2气体依次通过 ①1L 1mol/L碳酸钠溶液 ②浓硫酸 ③足量Na2O2 的装置后(假设每一步的反应都是充分的),再用排水法收集残留气体,则收集到的气体是( )
A . 1molNO
B . 1molNO2和0.5molO2
C . 0.25molO2
D . 1/3mol NO
最近更新
- 求(1+2x-3x2)6的展开式中含x12的项的系数.
- 下列应用及原理(用化学方程式表示)都正确的是()A.用镁带燃烧验证质量守恒定律2Mg + O2 点燃 2MgOB.用小苏
- 在城市化过程中 A.城市人口占总人口的比重持续上升 B.劳动力由第一、二产业向第三产业逐渐转移 C.城市数目增多,规模缩
- 在做“研究导体的电阻跟哪些因素有关”的实验时,为了便于研究,每次须挑选两根合适的导线,用同一电源,测出通过它们的电流,然
- 1.依次填入下列各句横线处的成语,最恰当的一组是( ) ①收入差别过大,造成骨干教师流失,对那些师资力量本就不厚实的
- 一人自街上路灯的正下方经过,看到自己头部的影子正好在自己脚下,如果人以不变的速度沿直线朝前走,则他自己头部的影子相对于地
- 选出一个不会产生歧义的句子。 A.这个人谁都不认识。 B.贪小便宜的人看不起。 C.天色晚了,自行车没修好,修车的急坏了
- 一长=0.80m的轻绳一端固定在点,另一端连接一质量=0.10kg的小球,悬点距离水平地面的高度H = 1.00m.开始
- 设数列前项和为,关于数列有下列命题: (1)若则既是等差数列又是等比数列; (2)若,则为等差数列; (3)若为等比数列
- 题目:发生在 的一件事 要求:1.先将题目补充完整,如我身边、我家里、班级里、学校里、
- (本题满分15分)由于卫生的要求游泳池要经常换水(进一些干净的水同时放掉一些脏水), 游泳池的水深经常变化,已知泰州某浴
- 阅读下面的文字,完成5―7题。史学易犯忌蔡尚思史学原以记述近现代事实为主要任务,任何时代的近现代史都是史学家的研究中心。
- 在平面直角坐标系xoy中,点。 (1)求以线段AB、AC为邻边的平行四边形两条对角线的长; (2)设实数
- 下列词语加点的字读音完全相同的一组是 A.菁华禁受令行禁止襟怀坦荡身居津要 B.庇荫辟邪开天
- . Either you or the headmaster ______ the prizes to the gift
- 在一密闭容器内发生氨的分解反应: 2NH3N2+3H2 .已知NH3起始浓度是2.6 mol·L-1,4s末为1
- 在研究摩擦力的实验中,将木块放在水平长木板上.如图3-2-8 a所示,用力沿水平方向拉木块,拉力从零开始逐渐增大.分别用
- 下图是同一细胞不同分裂时期的图像,据图分析,下列判断正确的是( ) A.图①②③④表示一个完整的细
- 下列实验操作正确的是 ( )①用带橡皮
- 给出下列四种说法: ①函数(且)与函数(且)的定义域相同;[来②函数与的值域相同; ③函数与都是奇函数; ④函数与在区



