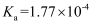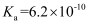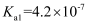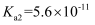溶液酸碱性的判断及相关计算 知识点题库
甲、乙、丙、丁、X是由短周期元素组成的纯净物,其中X为单质.上述物质转化关系如图所示(某些产物略去).
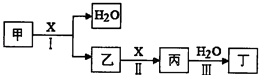
请回答下列问题:
-
(1) 若丁是一元强酸,甲→丁是工业生产丁的主要途径.
①写出反应I的化学方程式:
②常温下,1mol丙发生反应III放出46kJ热量,该反应的热化学方程式为:.
③在常温下,向VIL pH=11的甲溶液中加入V2L pH=3的盐酸,若反应后溶液的pH<7,则V1和V2的关系为V1V2(选填“>”、“<”或“=”),所得溶液中各种离子的浓度由大到小的顺序可能是:(写一种即可).
-
(2) 若丁是二元弱酸,丙是温室气体.
在容积为2L的容积固定的密闭容器中,将乙(g)和H2O(g)按下表用量分别进行反
应:乙(g)+H2O(g)⇌丙(g)+H2(g),得到如下数据:
实验组
温度/℃
起始量/mol
平衡量/mol
达平衡所需时间/min
乙
H2O
丙
1
650
4
2
1.6
5
2
900
2
1
0.4
3
3
900
2
1
0.4
1
①该反应的正反应为(填“吸热”或“放热”)反应.
②900℃时,上述反应按如下起始量分别加入该容器:
物质
乙
H2O
丙
H2
起始量/mol
0.8
1.0
0.6
0.8
则此时反应的v(正) v(逆)(填“>”、“<”或“=”).
③实验3跟实验2相比,改变的条件可能是.
 )>c(Cl﹣)>c(H+)>c(OH﹣)
B . 将pH=2 的稀盐酸与pH=12的氨水等体积混合,所得溶液pH>7
C . 0.10 mol•L﹣1的氨水用HNO3溶液完全中和后,溶液显中性
D . 用惰性电极电解稀硫酸时,实质是电解水,溶液的pH不变
)>c(Cl﹣)>c(H+)>c(OH﹣)
B . 将pH=2 的稀盐酸与pH=12的氨水等体积混合,所得溶液pH>7
C . 0.10 mol•L﹣1的氨水用HNO3溶液完全中和后,溶液显中性
D . 用惰性电极电解稀硫酸时,实质是电解水,溶液的pH不变
-
(1) 试判断用于汽车净化的一个反应2NO(g)+2CO(g)═N2(g)+2CO2(g),在298K、100kPa下能否自发进行(填“能”或“否”).已知:在298K、100kPa下该反应的△H=﹣113.0kJ•mol﹣1 , △S=﹣145.3J•mol﹣1•K﹣1 .
-
(2) 25℃下,将a mol•L﹣1的氨水与0.005mol•L﹣1的硫酸等体积混合,反应平衡时溶液中c(NH4+)=2c(SO42﹣),用含a的代数式表示NH3•H2O的电离常数Kb=.
-
(3) 25℃时,Ksp(BaSO4)=1.1×10﹣10 , Ksp(BaCO3)=2.6×10﹣9 , 现将BaCl2溶液滴入浓度均为0.01mol•L﹣1的Na2SO4和Na2CO3的混合溶液中,当两种沉淀共存时,溶液中c (CO32﹣):c(SO42﹣)=(不考虑CO32﹣的水解)
-
(4) 次磷酸(H3PO2)是一种一元中强酸,重要的精细化工产品.
①写出次磷酸的电离方程式:.
②已知某温度下0.01mol/L的NaOH溶液pH=10,将该NaOH溶液与等浓度等体积的H3PO2溶液混合,混合后溶液pH=7,则此时c(OH﹣)﹣c(H3PO2)=.该温度下将pH=a的盐酸Vaml与pH=b的氢氧化钠Vbml混合后溶液呈中性,且a+b=10,则Va:Vb=.
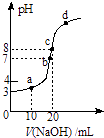
-
(1) 若A为CH3COOH,Q呈酸性,溶液中所有离子按浓度由大到小排列的顺序是;若A为HCl,100℃时(KW=10﹣12),溶液中由水电离出的H+浓度为mol•L﹣1;若A为H2S,Q接近中性,则HS﹣的电离能力水解能力(填“>”、“<”、“=”或“无法确定”).
-
(2) 根据(1)中信息比较相同条件下,浓度均为0.01mol•L﹣1的①NaHS、②CH3COONa、③NaCl溶液中,阴离子总浓度由大到小的顺序为(填序号).
-
(3) 用浓度为0.01mol•L﹣1的NaOH溶液滴定相同体积、相同浓度的①HCl溶液、②CH3COOH溶液、③H2S溶液,当滴定至中性时,消耗NaOH溶液的体积分别为a mL、b mL、c mL,则a、b、c的大小关系是.
序号 | 氢氧化钡溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
① | 22.00 | 0.00 | 8 |
② | 22.00 | 18.00 | c |
③ | 22.00 | 22.00 | d |
假设溶液混合前后的体积变化可忽略不计,则下列说法不正确的是( )
 溶液中增大
C . 向0.1mol·L-1的NaHSO3溶液中加入氨水至中性,则c(Na+)+c(NH
溶液中增大
C . 向0.1mol·L-1的NaHSO3溶液中加入氨水至中性,则c(Na+)+c(NH  )=2c(SO
)=2c(SO  )+c(HSO
)+c(HSO  )
D . 为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH<7,则H2A是强酸
)
D . 为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH<7,则H2A是强酸
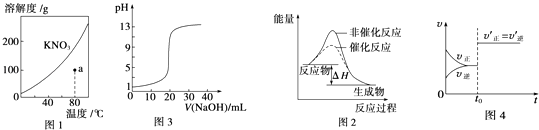
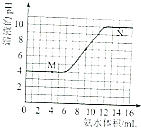
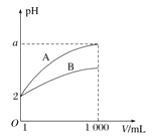
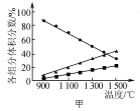 图甲表示H2S(g)受热分解时各组分体积分数随反应温度的变化关系,说明反应生成H2和S
B .
图甲表示H2S(g)受热分解时各组分体积分数随反应温度的变化关系,说明反应生成H2和S
B . 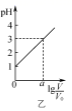 图乙表示V0 mL 0.1 mol·L-1的盐酸加水稀释至V mL,溶液的pH随lg
图乙表示V0 mL 0.1 mol·L-1的盐酸加水稀释至V mL,溶液的pH随lg  的变化关系,则a=2
C .
的变化关系,则a=2
C . 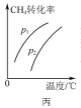 图丙表示密闭容器中CH4(g)+H2O(g)
图丙表示密闭容器中CH4(g)+H2O(g)  CO(g)+3H2(g)到达平衡时,CH4的转化率与压强、温度的变化关系曲线,说明p1>p2
D .
CO(g)+3H2(g)到达平衡时,CH4的转化率与压强、温度的变化关系曲线,说明p1>p2
D . 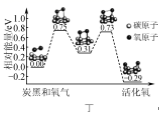 图丁表示炭黑作用下O2生成活化氧过程中能量变化情况,说明每活化一个氧分子吸收0.29 eV的能量
图丁表示炭黑作用下O2生成活化氧过程中能量变化情况,说明每活化一个氧分子吸收0.29 eV的能量
-
(1) Ⅰ.甲溶液的pH是4,乙溶液的pH是5,甲溶液与乙溶液的
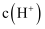 之比为________。
A . 10∶1 B . 1∶10 C . 2∶1 D . 1∶2
之比为________。
A . 10∶1 B . 1∶10 C . 2∶1 D . 1∶2 -
(2) 向
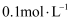 氨水溶液中加入少量的
氨水溶液中加入少量的  晶体时,会引起溶液中的___________。
A . pH增大 B .
晶体时,会引起溶液中的___________。
A . pH增大 B .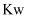 减小
C .
减小
C .  减小
D .
减小
D .  增大
增大
-
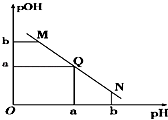
(3) 在某温度下的水溶液中,
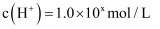 ,
, 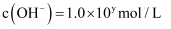 ,x与y的关系如图所示。该温度下,水的离子积常数为___________。
,x与y的关系如图所示。该温度下,水的离子积常数为___________。 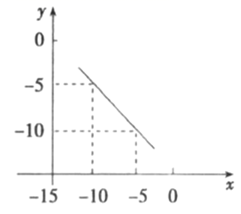 A .
A .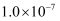 B .
B . 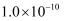 C .
C . 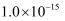 D .
D . 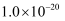
-
(4) 室温下,若溶液中水电离产生的
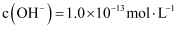 ,则该溶液的溶质可能是_________。
A .
,则该溶液的溶质可能是_________。
A .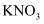 B .
B .  C .
C .  D .
D . 
-
(5) 将下列物质的水溶液加热蒸干、再灼烧,最终能得到原物质的是__________。A .
 B .
B .  C .
C . 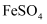 D .
D . 
-
(6) Ⅱ.常温下将
 溶液与
溶液与  溶液等体积混合。回答以下问题:
溶液等体积混合。回答以下问题: 反应后溶液中的溶质为(填化学式)。
-
(7) 反应后溶液呈碱性的原因是(用离子方程式表示)。
-
(8) 写出混合溶液中微粒浓度的下列几种关系:
①满足电荷守恒的关系式是。
②溶液中
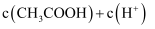
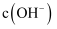 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③
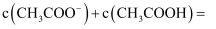
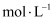 。
。 -
(9) 若
 溶液起始浓度为
溶液起始浓度为 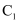 ,
,  溶液起始浓度为
溶液起始浓度为  ,等体积混合时溶液呈中性,则
,等体积混合时溶液呈中性,则 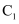
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
| 弱酸 | | | |
| 电离常数/( | | | |
下列说法错误的是( )
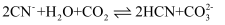 B .
B . 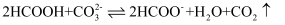 C . 中和等体积、等pH的
C . 中和等体积、等pH的 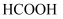 和
和 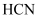 溶液,前者消耗
溶液,前者消耗  的量小于后者
D . 等体积、等浓度的
的量小于后者
D . 等体积、等浓度的 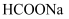 和
和 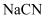 溶液中,前者所含离子总数小于后者
溶液中,前者所含离子总数小于后者
 溶液和
溶液和 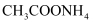 溶液均显中性,两溶液中水的电离程度相同
B . 常温下,
溶液均显中性,两溶液中水的电离程度相同
B . 常温下, 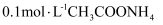 溶液的
溶液的 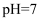 ,则
,则 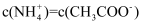 C . 常温下,
C . 常温下, 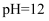 的
的 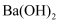 溶液与
溶液与 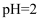 的盐酸等体积混合,溶液呈碱性
D .
的盐酸等体积混合,溶液呈碱性
D . 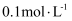 的
的  溶液中:
溶液中: 
- 下表为元素周期表短周期的一部分。回答下列问题: A D E G M (1)E元素原子核外有2个未成对电子,这2个电子所处
- (2013四川自贡一诊)如右图所示,M是一个小型理想变压器,原、副线圈匝数之比n1:n2=10:1,接线柱a、b接一正弦
- 2010年全国宗教工作会议强调,要认真贯彻实施《宗教事务条例》,充分发挥宗教界的积极作用,树立宗教和谐理念,推广宗教和谐
- 孙中山在《三民主义与中国》中指出:“似乎欧美各国应该家给人足,乐享幸福……然而试看各国的现象……富者极少,贫者极多……所
- (08台州中学第二次统考)下图表示某雄性动物的某个器官中的一些细胞图像,请据图回答: (1)综合分析
- 人体调节体温的神经中枢位于 A.下丘脑 B.延髓 C.
- 下列加点字的读音完全相同的一组是( ) A.爆炸 轰炸 炸锅 炸油条 B.年载 载道 记载 载波 C.与其 与会 与共
- 有一关于西汉历史的电视剧,一些剧情发生在都城长安的“市”里。下列关于该剧有关西汉“市”的场景,哪项不符合当时的历史实况
- 35. —Did you attend David’s wedding last night? —No. I _____
- 300 mL 2 mol·L硝酸与一定量的铝镁铁合金反应生成 3.36 L NO (标准状况)和铁盐、铝盐、镁盐等,再向
- 青少年补钙是必要的,但过量补钙对身体有害。这说明 A.人们对钙的认识又待进步 B.补钙要注意适
- 已知,是椭圆的左,右焦点,是的左顶点,点在过且斜率为的直线上,为等腰三角形,,则的离心率为() A.
- He asked Ginny ifshe would _______ to a small celebration af
- 下列变化属于物理变化的是() A.CO使人中毒 B.澄清石灰水长期露置在空气中 C.二氧化碳的水溶液使紫色石蕊试液变红
- 下图是工业区位选择模式图,其中线段长短表示影响程度大小。下列情况与甲、乙、丙、丁四图相符的是( )
- 某有机物X,在标准状况下的密度为2.679 g/L:把1.8g X完全燃烧,将燃烧产物通过浓硫酸,则浓硫酸增重2.16g
- 名著积累。(将涉及到的人物绰号、人名、作品名按顺序填入下表)(3分) (1)“一英雄 武艺强 受陷害 白虎堂
- 如图,把一个长方形的纸片对折两次,然后剪下一个角,为了得到一个锐角为60° 的菱形,剪口与折痕所成的角a 的度数应为(
- 阅读《孔乙己》中的几段文字,完成11-13题。孔乙己一到店,所有喝酒的人便都看着他笑,有的叫道,“孔乙己,你脸上又添上新
- 秦岭---淮河是我国重要的地理分界线。下列界线分布大致与其吻合的是 ( ) A 1月0℃等温线 B 400
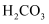
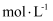 )(25℃)
)(25℃)