溶液酸碱性的判断及相关计算 知识点题库
在48mL0.1mol/LHNO3溶液中加入12mL0.4mol/LKOH溶液时,所得到的溶液呈( )
A . 弱酸性
B . 强酸性
C . 碱性
D . 中性
下列说法正确的是( )
A . 在由水电离产生的氢离子浓度为10﹣13 mol•L﹣1的溶液中:Ca2+、K+、Cl﹣、HCO  四种离子能大量共存
B . 已知MgCO3的Ksp=6.82×10﹣6 , 则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO
四种离子能大量共存
B . 已知MgCO3的Ksp=6.82×10﹣6 , 则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO 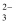 ),且c(Mg2+)∙c(CO
),且c(Mg2+)∙c(CO 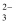 )=6.82×10﹣6
C . 对于反应2N2H4(l)=N2(g)+2H2(g),△H=﹣50.6 kJ∙mol﹣1 , 它只在高温下自发进行
D . 常温下,将0.2 mol∙L﹣1某一元碱(ROH)溶液和0.1 mol∙L﹣1HCl溶液等体积混合,混合后溶液pH<7,则c(ROH)>c(R+)
)=6.82×10﹣6
C . 对于反应2N2H4(l)=N2(g)+2H2(g),△H=﹣50.6 kJ∙mol﹣1 , 它只在高温下自发进行
D . 常温下,将0.2 mol∙L﹣1某一元碱(ROH)溶液和0.1 mol∙L﹣1HCl溶液等体积混合,混合后溶液pH<7,则c(ROH)>c(R+)
 四种离子能大量共存
B . 已知MgCO3的Ksp=6.82×10﹣6 , 则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO
四种离子能大量共存
B . 已知MgCO3的Ksp=6.82×10﹣6 , 则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO 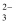 ),且c(Mg2+)∙c(CO
),且c(Mg2+)∙c(CO 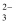 )=6.82×10﹣6
C . 对于反应2N2H4(l)=N2(g)+2H2(g),△H=﹣50.6 kJ∙mol﹣1 , 它只在高温下自发进行
D . 常温下,将0.2 mol∙L﹣1某一元碱(ROH)溶液和0.1 mol∙L﹣1HCl溶液等体积混合,混合后溶液pH<7,则c(ROH)>c(R+)
)=6.82×10﹣6
C . 对于反应2N2H4(l)=N2(g)+2H2(g),△H=﹣50.6 kJ∙mol﹣1 , 它只在高温下自发进行
D . 常温下,将0.2 mol∙L﹣1某一元碱(ROH)溶液和0.1 mol∙L﹣1HCl溶液等体积混合,混合后溶液pH<7,则c(ROH)>c(R+)
按要求填写下列问题:
-
(1) 某些共价化合物(如H2O、NH3、N2O4等)在液态时会发生微弱的电离,如:2H2O⇌H3O++OH﹣ , 则液态NH3电离的方程式是
-
(2) 某温度(t℃)时,测得0.01mol/L的NaOH溶液的pH=10,则该温度下水的KW=,在此温度下,将pH=b的NaOH溶液Vb L与pH=a的H2SO4溶液Va L混合,若所得混合液为中性,且a+b=13,则Va:Vb=
-
(3) 25℃时,0.1mol/L的HA溶液中
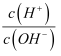 =1010 . 请回答下列问题:
=1010 . 请回答下列问题: ①HA是(填“强电解质”或“弱电解质”).
②在加水稀释HA溶液的过程中,随着水量的增加而增大的是(填字母)
A.c(HA) B.
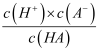 C.c(H+)与c(OH﹣)的乘积 D.c(OH﹣)
C.c(H+)与c(OH﹣)的乘积 D.c(OH﹣) -
(4) 在常温下,中和相同体积,相同pH的Ba(OH)2、NH3•H2O、NaOH三种稀溶液所用相同浓度的盐酸的体积分别为V1、V2、V3 , 则三种关系为(用“V1、V2、V3”和“>、<、=”表示).
-
(5) 今有A.盐酸 B.醋酸 C.硫酸三种酸:
①在同体积、同浓度的三种酸中,分别加入足量的碳酸氢钠粉末,在相同条件下产生CO2的体积由大到小的顺序是.(填写酸的序号并用符号“>、<、=”连接,下同)
②在同体积、同pH的三种酸中,同时加入形状、密度、质量完全相同的锌粒,若产生相同体积的氢气(同温同压下),则开始反应时速率大小关系是,反应所用时间长短关系是
常温下有体积相同的四种溶液:①pH=3的CH3COOH溶液 ②pH=3的盐酸 ③pH=11的氨水 ④pH=11的NaOH溶液.下列说法正确的是( )
A . 若将四种溶液稀释100倍,溶液pH大小顺序:③>④>①>②
B . ③和④分别用等浓度的硫酸溶液中和,消耗硫酸溶液的体积:③=④
C . ①与②分别与足量镁粉反应,生成H2的量:①<②
D . ②和③混合,所得混合溶液的pH大于7
今有室温下有四种溶液,有关叙述不正确的是( )
① | ② | ③ | ④ | |
pH | 11 | 11 | 3 | 3 |
溶液 | 氨水 | NaOH溶液 | 醋酸 | 盐酸 |
A . 分别加水稀释10倍,四种溶液的pH①>②>④>③
B . ①加入适量的氯化铵晶体后,溶液的pH减小
C . ①溶液中c(NH4+)+c(H+)大于④中的c(Cl﹣)+c(OH﹣)
D . VaL④与VbL②溶液混合后,若混合后溶液pH=4,则Va:Vb=11:9
根据问题填空:
-
(1) 在温度t℃时,某溶液中c(H+)=10﹣a mol•L﹣1 , c(OH﹣)=10﹣b mol•L﹣1 , 已知a+b=12,则t25(填“大于”、“小于”或“等于”).
-
(2) 常温下,向某Ba(OH)2溶液中逐滴加入pH=x的盐酸,测得混合溶液的部分pH如下表所示:
序号
氢氧化钡的体积/mL
盐酸的体积/mL
溶液的pH
①
22.00
0.00
12
②
22.00
18.00
11
③
22.00
22.00
7
x=.Ba(OH)2溶液的物质的量浓度为.
-
(3) 常温下,向100mLpH=2的硫酸与硫酸钠的混合溶液中,加入300mL上述Ba(OH)2溶液,沉淀正好达最大量,此时溶液的pH7(填“大于”、“小于”或“等于”);原混合溶液中硫酸钠的物质的量浓度为.
现有25℃的下列四种溶液,其中碱性最强的是( )
A . pH=11的溶液
B . 4 g NaOH溶于水形成1L的水溶液
C . c(OH﹣)=0.12 mol•L﹣1
D . c(H+)=1×10﹣10 mol•L﹣1的溶液
下列溶液一定呈中性的是 ( )
A . pH=7的溶液
B . c(H+)=c(OH-)的溶液
C . 由强酸、强碱等物质的量反应得到的溶液
D . 非电解质溶于水得到的溶液
25 ℃时,下列溶液的碱性最强的是( )
A . pH=11的溶液
B . 0.1 mol/L Ba(OH)2溶液
C . 1 L含有4 g NaOH的溶液
D . 0.1 mol/L KOH溶液
现有浓度均为0.1 mol·L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦氨水,请回答下列问题:
-
(1) ①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)。
-
(2) ④、⑤、⑥、⑦四种溶液中NH4+浓度由大到小的顺序是(填序号)。
-
(3) 将③和④按体积比1∶2混合后,混合液中各离子浓度由大到小的顺序是。
-
(4) 已知t ℃时,Kw=1×10-13 , 则t ℃(填“>”“<”或“=”)25 ℃。在t ℃时将pH=11的NaOH溶液a L与pH=1的H2SO4溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a∶b=。
下列实验操作能达到实验目的的是( )
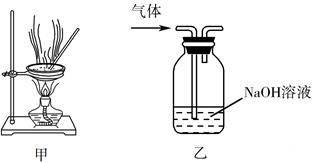
A . 用经水湿润的pH试纸测量溶液的pH
B . 将4.0 g NaOH固体置于100 mL容量瓶中,加水至刻度,配制1.000 mol·L−1NaOH溶液
C . 用装置甲蒸干AlCl3溶液制无水AlCl3固体
D . 用装置乙除去实验室所制乙烯中的少量SO2
常温下,将pH=3的H2SO4和pH=12的NaOH溶液混合,当混合溶液的pH=10时,强酸和强碱的体积之比为( )
A . 1∶9
B . 9∶1
C . 10∶1
D . 1∶10
下列物质加入水中,能使水的电离程度增大,且所得溶液显酸性的是( )
A . CH3COOH
B . Al2(SO4)3
C . NaOH
D . Na2CO3
下列说法正确的是( )
A . pH为6.8的溶液一定呈酸性
B . 中和pH和体积均相等的醋酸和盐酸溶液,所需NaOH的物质的量相同
C . 0.1mol·L-1的醋酸溶液加水稀释,溶液中所有离子的浓度都减小
D . 0.1mol·L-1的氨水溶液中:c(NH4+) +c(NH3·H2O) =0.1mol·L-1
下列水溶液一定呈中性的是( )
A . pH=7的溶液
B . c(H+)=1.0×10-7mol·L-1的溶液
C . c(H+)=c(OH-)的溶液
D . pH=3的酸与pH=11的碱等体积混合后的溶液
已知100℃时,水的离子积常数为1×10-12。在此温度下,将pH=8的NaOH溶液与pH=4的H2SO4溶液混合,得到pH=7的混合溶液,则NaOH溶液与H2SO4溶液的体积比约为( )
A . 11∶9
B . 9∶11
C . 1∶9
D . 1∶1
下列叙述正确的是( )
A . 常温下,0.001 mol/L的NaOH溶液的pH=11
B . pH=3的醋酸溶液稀释至10倍后pH=4
C . 95 ℃纯水的pH=6,说明加热可导致水呈酸性
D . 常温下,pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7
常温下,向1L含有0.2mol.L-l HA与0.1 mol.LlNaA的溶液中通入HCl气体(或加入NaOH固体),测得溶液pH的变化如图所示(忽略溶液体积和温度变化)。下列叙述错误的是( )
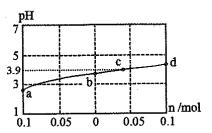
A . b点溶液中水的电离程度最大
B . 溶液由b向a变化过程中, 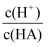 逐渐增大
C . c点溶液中c(HA)=c(A-),则Ka(HA)的数量级为10-4
D . d点对应的溶液中:c(A-)>c(Na+)>c(H+)>c(OH-)
逐渐增大
C . c点溶液中c(HA)=c(A-),则Ka(HA)的数量级为10-4
D . d点对应的溶液中:c(A-)>c(Na+)>c(H+)>c(OH-)
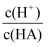 逐渐增大
C . c点溶液中c(HA)=c(A-),则Ka(HA)的数量级为10-4
D . d点对应的溶液中:c(A-)>c(Na+)>c(H+)>c(OH-)
逐渐增大
C . c点溶液中c(HA)=c(A-),则Ka(HA)的数量级为10-4
D . d点对应的溶液中:c(A-)>c(Na+)>c(H+)>c(OH-)
25℃时,向20 mL 0.1 mol·L-1某一元酸HA溶液中滴加0.1 mol·L-1的NaOH溶液,测得溶液pH的变化如图所示。下列说法错误的是( )
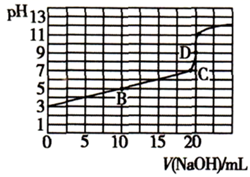
A . HA的电离方程式为HA  A-+H+ , Ka(HA)≈10-5
B . B点溶液中存在关系:2c(H+)+c(A-)=2c (OH-)+ c (HA)
C . C点溶液中存在关系:c(Na+)+c(H+)=c(A-)+ c(OH-)
D . D点溶液中微粒浓度大小关系:c(Na+)>c(A-)>c(OH-)>c(H+)
A-+H+ , Ka(HA)≈10-5
B . B点溶液中存在关系:2c(H+)+c(A-)=2c (OH-)+ c (HA)
C . C点溶液中存在关系:c(Na+)+c(H+)=c(A-)+ c(OH-)
D . D点溶液中微粒浓度大小关系:c(Na+)>c(A-)>c(OH-)>c(H+)
 A-+H+ , Ka(HA)≈10-5
B . B点溶液中存在关系:2c(H+)+c(A-)=2c (OH-)+ c (HA)
C . C点溶液中存在关系:c(Na+)+c(H+)=c(A-)+ c(OH-)
D . D点溶液中微粒浓度大小关系:c(Na+)>c(A-)>c(OH-)>c(H+)
A-+H+ , Ka(HA)≈10-5
B . B点溶液中存在关系:2c(H+)+c(A-)=2c (OH-)+ c (HA)
C . C点溶液中存在关系:c(Na+)+c(H+)=c(A-)+ c(OH-)
D . D点溶液中微粒浓度大小关系:c(Na+)>c(A-)>c(OH-)>c(H+)
下列叙述正确的是( )
A . 0.1mol•L-1NH4Cl溶液:c(NH4+)=c(Cl-)
B . 在25℃时,pH=4的盐酸与pH=10的氨水溶液等体积混合后pH>7
C . 0.1mol•L-1与0.2mol•L-1氨水溶液中c(OH-)之比为1:2
D . 中和pH与体积都相同的NaOH和Ba(OH)2溶液,消耗HCl的物质的量之比是1:2
最近更新
- 下图为泡沫灭火器及泡沫灭火器原理示意图,结合图示回答下列问题:(1)将装置Ⅱ倒置,将会出现什么现象? (2)请说出泡沫灭
- 中国饮食文化学者说:“饮食通过一日三餐的教化,把中国人的物质生活和文化精神聚在了一处。中国饮食文化必须要重视“传承”,既
- 与元素化学性质密切相关的是原子的() A.中子数 B.质子数 C.电子数 D.最外层电子数
- 一列横波沿弹性绳传播,某时刻绳上质点A向上运动到振幅位置时,在其右方相距0.3m的质点刚好向下运动到最大位移处,已知此波
- The little boywon’t go tosleep________his mother tells him
- “蜻蜓点水”与下列哪种动物的行为结果相同( ) A、雄鸡报晓 B、蜘蛛结网捕虫 C、鲤鱼产卵 D、蟋蟀咬架
- 如图:在数轴上A点表示数a,B点示数b,C点表示数c,b是最小的正整数,且a、c满足|a+2|+(c﹣7)2=0.(1)
- 一片草原上全部黄羊和全部生物,在生态学上分别称为( ) A种群和群落 B种群和生态系统 C
- 显微镜下分别观察小麦的叶肉细胞和干种子的胚乳细胞,发现叶肉细胞质中有明显的细胞质流动现象,而胚乳细胞中则无此现象,原因是
- 现有Fe、CuO、MgCl2、Ca(OH)2、稀H2SO4等五种物质,在常温下它们两两相互发生的化学反应有 A.3个
- 赠言是给别人留下的美好祝愿或真诚的希望,它可以增强信心、增进友谊。假如你是高三的同学,在这即将毕业离别之际,你最想把赠言
- 由于血缘关系的亲疏不同,西周贵族集团形成的宗法等级序列应该是( ) A、周王——卿——诸侯——士
- 据统计2010年5月某日在上海参观世博园的人数约为256000,这一人数用科学计数法表示为 .
- 某同学用低倍镜观察到根尖分生区细胞的清晰物像,这时如果转动转换器改用高倍镜观察,下列情况一般不会出现的是A.视野内的细胞
- 下列现象中不能用分子热运动观点解释的是 A.酒香不怕巷子深B.把青菜用盐腊成咸菜 C.沙尘暴起,尘土满天D.衣橱里的樟脑
- 如图所示,轻绳上端固定在天花板上的O点,下端悬挂一个重为10N的物体A,B是固定的表面光滑的圆柱体。当A静止时,轻绳与天
- 下列各组物质中,属于同分异构体的是 A.O2和O3
- 2009年3月27日,财政部代理发行2009年新疆维吾尔自治区政府债券(一期)。本期债券为固定利率附息债,期限3年,按年
- 中学化学课本中有大量的数据材料,下面是某学生对数据的利用,其中不正确的是( ) A.利用溶解度数据可判断煮沸Mg(HC
- 1.下列各句中,没有语病的一句是( ) A.目前地理信息交换的技术问题已经基本成熟,一旦地理信息为广大公众所认可,那



