溶液酸碱性的判断及相关计算 知识点题库
25℃时,向20mL浓度为0.1mol/L的CH3COOH溶液中逐滴加入0.1mol/L的NaOH溶液,溶液pH的变化如图所示,下列说法不正确的是( )
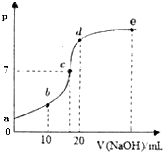
A . c点时,c(Na+)=c(CH3COO﹣)
B . b点时,c(Na+)>c(CH3COO﹣)>c(H+)>c(OH﹣)
C . d点时,c(Na+)>c(CH3COO﹣)>c(OH﹣)>c(H+)
D . 从a点到c点间可能有:c(CH3COO﹣)>c(H+)=c(Na+)>c(OH﹣)
室温下pH=9的Ba(OH)2溶液与pH=12的KOH溶液,按4:1的体积比混合,则混合溶液中H+浓度为(单位:mol•L﹣1)( )
A . 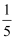 ×(4×10﹣9+1×10﹣12)
B .
×(4×10﹣9+1×10﹣12)
B . 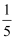 ×(8×10﹣9+1×10﹣12)
C . 5×10﹣10
D . 5×10﹣12
×(8×10﹣9+1×10﹣12)
C . 5×10﹣10
D . 5×10﹣12
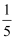 ×(4×10﹣9+1×10﹣12)
B .
×(4×10﹣9+1×10﹣12)
B . 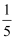 ×(8×10﹣9+1×10﹣12)
C . 5×10﹣10
D . 5×10﹣12
×(8×10﹣9+1×10﹣12)
C . 5×10﹣10
D . 5×10﹣12
在25℃时,将0.1mol•L﹣1的HA溶液与0.1mol•L﹣1的NaOH溶液等体积混合后,测得混合溶液pH=8,则下列所表示的该混合溶液中有关微粒的浓度关系中,错误的是( )
A . c(HA)+c(A﹣)=c(Na+)=0.1mol•L﹣1
B . c(Na+)﹣c(A﹣)=c(OH﹣)﹣c(H+)
C . c(Na+)>c(A﹣)>c(OH﹣)>c(H+)
D . c(OH﹣)=c(H+)+c(HA)
根据所学知识填空.
-
(1) 在25℃条件下将pH=11的氨水稀释100倍后溶液的pH为(填序号) .A . 9 B . 13 C . 11~13之间 D . 9~11之间
-
(2) 25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是(填序号) .A . 氨水与氯化铵发生化学反应 B . 氯化铵溶液水解显酸性,增加了c(H+) C . 氯化铵溶于水,电离出大量铵离子,抑制了氨水的电离,使c(OH﹣)减小
-
(3) 室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失),
①和两种粒子的物质的量之和等于0.1mol.
②和两种粒子的物质的量之和比OH﹣多0.05mol.
-
(4) 已知某溶液中只存在OH﹣、H+、NH4+、Cl﹣四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A.c(Cl﹣)>c(NH4+)>c(H+)>c(OH﹣)
B.c(Cl﹣)>c(NH4+)>c(OH﹣)>c(H+)
C.c(Cl﹣)>c(H+)>c(NH4+)>c(OH﹣)
D.c(NH4+)>c(Cl﹣)>c(OH﹣)>c(H+)
①若溶液中只溶解了一种溶质,该溶质的名称是,上述离子浓度大小顺序关系中正确的是(选填序号).
②若上述关系中C是正确的,则溶液中溶质的化学式是.
③若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl) c(NH3•H2O)(填“>”、“<”、或“=).
常温下,向0.1mol/L的H2SO4溶液中逐滴加入0.1mol/L的Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液的体积关系如图所示,下列说法中正确的是( )
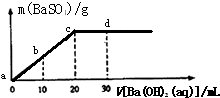
A . a﹣d溶液的pH:a<b<c<d
B . a﹣d溶液的导电能力:a<b<c<d
C . b处溶液的c(H+)与d处溶液的c(OH﹣)相等
D . c处溶液和d处溶液均呈碱性
室温下向10mL0.1mol•L﹣1NaOH溶液中加入0.1mol•L﹣1的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )
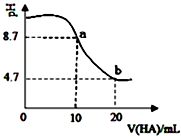
A . HA为强酸
B . a、b两点所示溶液中水的电离程度相同
C . b点所示溶液中c(A﹣)>c(HA)
D . pH=7时,c(Na+)=c(A﹣)+c(HA)
常温下,用pH=11的氨水,分别与pH=3的盐酸和某酸等体积混合,得到X、Y两种溶液,关于这两种溶液酸碱性的描述正确的是( )
A . X可能呈酸性
B . X溶液可能呈中性
C . Y溶液可能呈中性
D . Y溶液一定呈中性
(常温下)下列关于电解质溶液的正确判断的是( )
A . 在pH=12的溶液中,Al3+、Cl﹣、HCO3﹣、Na+可以大量共存
B . 在pH=0的溶液中,Na+、NO3﹣、SO32﹣、K+可以大量共存
C . 由0.1 mol/L一元碱BOH溶液的pH=10,可推知BOH溶液存在BOH⇌B++OH﹣
D . pH=2的一元酸和pH=12的一元强碱等体积混后溶液一定存在:c(OH﹣)=c(H+)
现有常温时pH=1的某强酸溶液10 mL,下列操作能使溶液的pH变成2的是
A . 加水稀释成100 mL
B . 加入10 mL的水进行稀释
C . 加入10 mL 0.01 mol·L-1的NaOH溶液
D . 加入10 mL 0.01 mol·L-1的HCl溶液
某温度下,水的离子积为Kw , 该温度下将a mol•L-1的一元酸HA与b mol•L-1的一元碱BOH等体积混合,若混合溶液显中性必须满足的条件是( )
A . a=b
B . c(H+)= c(OH-)=10-7mol/L
C . 混合液中Kw= c2(OH-)
D . c(H+)+c(B+)=c(OH-)+c(A-)
下列说法或表述正确的是( )
A . 25℃时,等体积等浓度的硝酸与氨水混合后,溶液pH = 7
B . 某醋酸稀溶液的pH = a,将此溶液稀释一倍后,溶液的pH = b,则a > b
C . Ba(OH)2溶液中加入过量Al2(SO4)3溶液,反应的离子方程式为:3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓ + 2Al(OH)3↓
D . 物质的量浓度均为1 mol·L-1的NaCl和MgCl2混合液中,含有Cl-的数目为3NA(NA表示阿伏加德罗常数的值)
常温下,将下列物质溶于水中分别配制成0.1 mol•L-1溶液,所得溶液pH大于7的是( )
A . NaCl
B . HCl
C . NaOH
D . CH3COOH
下列溶液一定呈中性的是( )
A . pH=7的溶液
B . 使石蕊试液呈紫色的溶液
C . c(H+)=c(OH﹣)=10﹣6mol·L﹣1的溶液
D . 酸与碱恰好反应生成的溶液
在某温度时,测定纯水中c(H+)=2.4×10-7 mol·L-1 , 则c(OH-)为( )
A . 2.4×10-7 mol·L-1
B . 0.1×10-7 mol·L-1
C .  mol·L-1
D . c(OH-)无法确定
mol·L-1
D . c(OH-)无法确定
 mol·L-1
D . c(OH-)无法确定
mol·L-1
D . c(OH-)无法确定
物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡。请回答下列问题:
-
(1) 常温下,物质的量浓度均为0.1mol·L-1的六种溶液
①Na2CO3、②NaCl、③NaOH、④(NH4)2SO4、⑤CH3COONa、⑥NH4NO3 , pH从大到小排列顺序为(填序号)。
-
(2) 已知T℃时,Kw=1×10-12,在该温度时,将pH=9的NaOH溶液bL与pH=2的H2SO4溶液aL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=3, 则a :b=。
-
(3) 现有HA、HB两种酸。室温下用0.1mol· L-1NaOH溶液分别滴定20.00mL浓度均为0.1mol·L-1的HA、HB两种酸的溶液,滴定过程中溶液的pH随滴入的NaOH溶液体积的变化如下图。
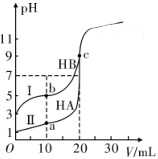
①由图可知;酸性HAHB,b 点对应的溶液中c(HB)c(B-)(填“>”“<”或“=”)。
②室温下HB的电离平衡常数Ka的数量级为。
已知常温下,Ka1(H2CO3)=4.3×10-7,Ka2(H2CO3)=5.6×10-11。某二元酸H2R及其钠盐的溶液中,H2R、HR-、R2-三者的物质的量分数随溶液pH变化关系如图所示,下列叙述错误的是( )
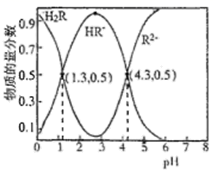
A . 在pH=4.3的溶液中:3c(R2-)=c(Na+)+c(H+)-c(OH-)
B . 等体积、等浓度的NaOH溶液与H2R溶液混合后,此溶液中水的电离程度比纯水小
C . 在pH=3的溶液中存在  =10-3
D . 向Na2CO3溶液中加入少量H2R溶液,发生反应:CO32-+H2R=HCO3-+HR-
=10-3
D . 向Na2CO3溶液中加入少量H2R溶液,发生反应:CO32-+H2R=HCO3-+HR-
 =10-3
D . 向Na2CO3溶液中加入少量H2R溶液,发生反应:CO32-+H2R=HCO3-+HR-
=10-3
D . 向Na2CO3溶液中加入少量H2R溶液,发生反应:CO32-+H2R=HCO3-+HR-
常温下,将0.1 mol·L-1氢氧化钠溶液与0.06 mol·L-1硫酸溶液等体积混合,该混合溶液的pH等于( )
A . 1.7
B . 2.0
C . 12.0
D . 12.4
下列操作会使H2O的电离平衡向正方向移动,且所得溶液呈酸性的是( )
A . 向水中加入少量的CH3COONa
B . 向水中加入少量的NaHSO4
C . 加热水至100 ℃,pH=6
D . 向水中加少量的CuSO4
25℃时,在20 mL 0.1 mol/L氢氟酸中加入V mL 0.1 mol/L NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法错误的是( )
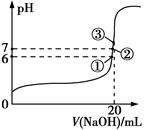
A . pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B . ①点时pH=6,此时溶液中,c(F−)−c(Na+)=9.9×10−7mol/L
C . ②点时,溶液中的c(F−)=c(Na+)
D . ③点时V=20 mL,此时溶液中c(F−)<c(Na+)=0.05 mol/L
常温下,向10mL0.05mol·L-1的某酸H2B溶液中滴入0.1mol·L-1氨水,溶液中由水电离出氢离子浓度随滴入氨水体积变化如图。下列说法错误的是( )
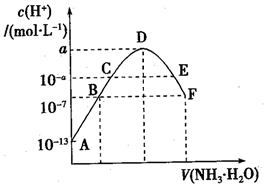
A . 常温下,0.1mol·L-1KHB溶液的pH=1
B . 过程中,随着氨水的加入,溶液pH先增后减
C . D,E,F三点中,D点水的电离程度最大
D . B点溶液呈酸性,F点溶液c(NH  )=2c(B2-)
)=2c(B2-)
 )=2c(B2-)
)=2c(B2-)
最近更新
- 本小题满分12分 设数列的前项和为,如果为常数,则称数列为“科比数列”. (1)等差数列的首项为1,公差不为零,若为
- 如图,PA、PB切⊙O于点A、B,点C是⊙O上一点,ACB=65º,则P= 。
- 下列不属于黄种人的民族是: ( )
- 肺泡内的气体进入血液,至少要通过几层细胞A.一层 B.二层 C. 三层
- 方形是轴对称图形,它共有__ _条对称轴.
- 化学与生活皆有着密切联系。下列有关说法错误的是( ) A.用纯碱和用清洁剂都能洗涤玻璃仪器表面油污,但去污原理不
- 请根据题意选择下列物质,并用其字母代号填空:(1)一种红棕色粉末,常用于红色油漆和涂料的是_________。 (2)要
- 为应对严重的国际金融危机,我国实行了积极的财政政策和适度宽松的货币政策。回答下题。 下列属于适度宽松的货币政策有 ①降低
- 读下列材料,回答问题。 材料一:核能发电能量密集,地区适应性强,极少排放二氧化碳等温室气体,不产生二氧化硫和氮氧化物等有
- 下列各元素中,原子半径依次增大的是() A.Na、Mg、Al B.N、O、F C.P、Si、Al D.C、S
- 如图5所示,A、B、C、D是匀强电场中一正方形的四个顶点.已知A、B、C三点的电势分别为φA=15V,φB=3V,φC=
- 下列各句中,没有语病的一句是 A.这个高台光滑突兀,陡峭高耸,十分危险。听老人们说,这个高台从来就没有行人上去过,上去的
- 范蠡曾是吴越争霸时期越国的谋臣,后来弃官从商,后世商人尊称他为商祖、经营之神。下列情景范蠡可能经历的是 A.官府控制商业
- I read ________ article _________ a boy from the USA A. an;
- 读我国主要河流分布示意图,以下说法正确的是 A.河流①是我国第二长河,注入东海 B.河流②是我国第一大河,
- 小明于2014年6月21日(夏至日)这一天进行了“立竿见影”的探究活动。读图10回答下列问题。1、从日出到正午,竹竿影子
- Ms. Claire is a strict but kind teacher, _____ I respect and
- 如图2-3-20所示,一个半球形的碗放在桌面上,碗口水平,O点为其球心,碗的内表面及碗口是光滑的.一根细线跨在碗口上,线
- 如图所示,光滑斜面AE被分成四个相等的部分,一物体由A点从静止释放,下列结论中不正确的是(
- 下列是几种粒子的结构示意图,有关说法不正确的是() A.①和②属同种元素 B.④属于金属元素 C.①和③的化学性质相似



