活化能及其对化学反应速率的影响 知识点
活化能对反应速率的影响:当活化能较小时,比如加入催化剂后,活化能会降低,致使普通分子变成活化分子更容易,活化分子百分数增大,导致碰撞后发生反应的几率增大,导致反应速率会增大。
活化能及其对化学反应速率的影响 知识点题库
 催化剂活性
催化剂活性 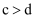 B .
B . 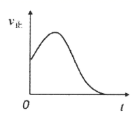
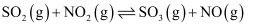
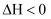 ,在恒容绝热容器中投入一定量
,在恒容绝热容器中投入一定量  和
和  ,正反应速率随时间变化
C .
,正反应速率随时间变化
C . 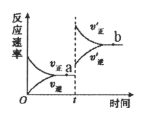
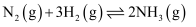
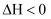 ,t时刻改变某一条件,则
,t时刻改变某一条件,则  D .
D . 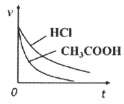 向等体积等pH的HCl和
向等体积等pH的HCl和  中加入等量且足量Zn,反应速率的变化情况
中加入等量且足量Zn,反应速率的变化情况
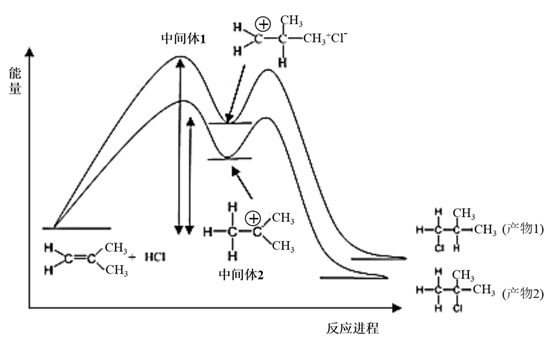
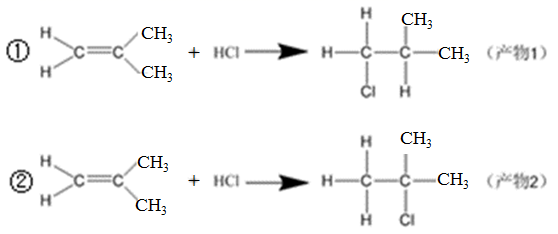
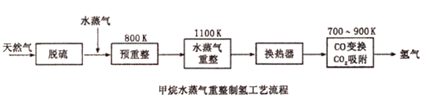
-
(1) 涉及的甲烷水蒸气重整反应方程式为:
CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1
CH4(g)+2H2O(g)=CO2(g)+4H2(g) ΔH2=+165kJ·mol-1
已知CH4、CO、H2的燃烧热分别为ΔH=-891kJ·mol-1、ΔH=-283kJ·mol-1、ΔH=-286kJ·mol-1、水的汽化热ΔH=+44kJ·mol-1 , 则ΔH1=。
-
(2) 天然气脱硫工艺中常用热分解法处理H2S,硫化氢分解的反应方程式为:2H2S(g)=2H2(g)+S2(g),在101kPa时各气体的平衡体积分数与温度的关系如图所示:
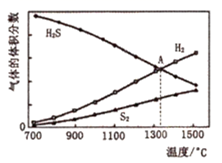
该反应的ΔH0(填“>”、“<”)。图中A点时反应的平衡常数Kp=(用平衡分压代替平衡浓度,平衡分压=总压X物质的量分数)。
-
(3) 利用甲烷水蒸气重整制得的氢气,工业上可用于合成氨生产。
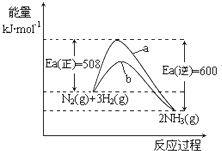
①“哈伯法”是制氨气的常用方法,反应方程式为:N2(g)+3H2(g)
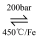 2NH3(g)向密闭容器中按1:3体积比通入N2和H2 , 反应达平衡时NH3的体积分数为25.0%,则N2的平衡转化率α(N2)=
2NH3(g)向密闭容器中按1:3体积比通入N2和H2 , 反应达平衡时NH3的体积分数为25.0%,则N2的平衡转化率α(N2)=②“球磨法”是一种在温和的条件下(45℃和1bar,1bar≈100kPa)合成氨气的新方法,氨的最终体积分数可高达82.5%。该法分为两个步骤(如图):第一步,铁粉在球磨过程中被反复剧烈碰撞而活化,产生高密度的缺陷,氮分子被吸附在这些缺陷上[Fe(N*)],有助于氮分子的解离。第二步,N*发生加氢反应得到NHx*(x=1~3),剧烈碰撞中,NHx*从催化剂表面脱附得到产物氨。“球磨法”与“哈伯法”相比较,下列说法中错误的是(选填标号)。
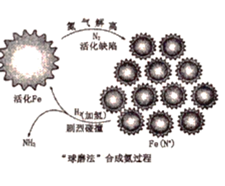
A.催化剂(Fe)缺陷密度越高,N2的吸附率越高
B.“哈伯法”采用高温主要用于解离氮氮三键,而“球磨法”不用解离氮氮三键
C.“球磨法”转速不能过快,否则体系升温太快,温度升高不利于N2吸附
D.“球磨法”不采用高压,是因为低压产率已经较高,加压会增大成本
-
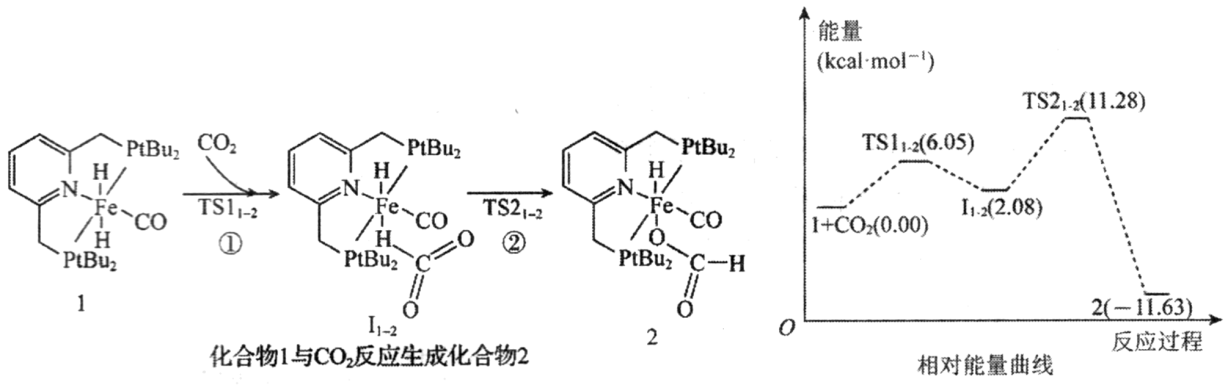
(4) 用催化剂Fe3(CO)12/ZSM-5催化CO2加氢合成乙烯的反应,所得产物含CH4、C3H6、C4H8等副产物,反应过程如图。
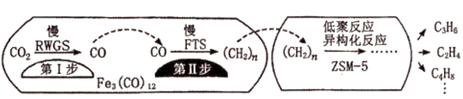
催化剂中添加Na、K、Cu助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如表。
助剂
CO2转化率(%)
各产物在有机产物中的占比(%)
C2H4
C3H6
其他有机物
Na
42.5
35.9
39.6
24.5
K
27.2
75.6
22.8
1.6
Cu
9.8
80.7
12.5
6.8
欲提高单位时间内乙烯的产量,在Fe3(CO)12/ZSM-5中添加助剂效果最好,加入助剂能提高单位时间内乙烯产量的根本原因是。
 、
、  均减小,反应速率加快
均减小,反应速率加快
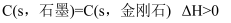 ,则石墨比金刚石稳定
C . 在一恒容密闭容器中发生反应
,则石墨比金刚石稳定
C . 在一恒容密闭容器中发生反应 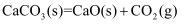 ,仅增加
,仅增加 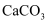 的质量,反应速率加快
D . 对于反应
的质量,反应速率加快
D . 对于反应 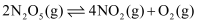 ,反应达到平衡后,保持其他条件不变,增大压强,化学平衡常数增大
,反应达到平衡后,保持其他条件不变,增大压强,化学平衡常数增大
下列说法错误的是( )
 (g)→
(g)→ (l)→
(l)→ (s),熵依次增加
B . 可逆反应都有一定的限度,限度越大反应物的转化率一定越高
C . 可逆反应,若总键能:反应物>生成物,则升高温度不利于提高反应物的转化率
D . 对于气体反应,其他条件不变,增大压强反应速率加快,与活化分子的百分含量无关
(s),熵依次增加
B . 可逆反应都有一定的限度,限度越大反应物的转化率一定越高
C . 可逆反应,若总键能:反应物>生成物,则升高温度不利于提高反应物的转化率
D . 对于气体反应,其他条件不变,增大压强反应速率加快,与活化分子的百分含量无关
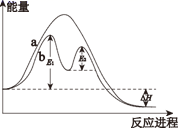
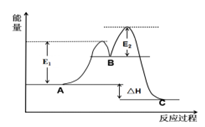
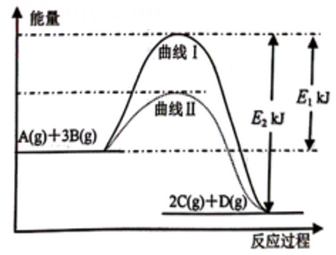
 2C(g)+D(g), 其反应过程和能量能量变化如图所示,下列说法正确的是( )
2C(g)+D(g), 其反应过程和能量能量变化如图所示,下列说法正确的是( )
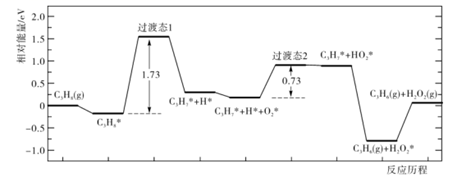
 C6H5OH(g)+N2(g)。
C6H5OH(g)+N2(g)。
-
(1) 已知6C(s,石墨)+3H2(g)
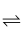 C6H6(g) ΔH1=+82.9kJ·mol-1
C6H6(g) ΔH1=+82.9kJ·mol-1
2N2(g)+O2(g)
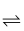 2N2O(g) ΔH2=+163.2kJ·mol-1
2N2O(g) ΔH2=+163.2kJ·mol-112C(s,石墨)+6H2(g)+O2(g)
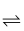 2C6H5OH(g) ΔH3=-243kJ·mol-1
2C6H5OH(g) ΔH3=-243kJ·mol-1则C6H6(g)+N2O(g)
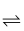 C6H5OH(g)+N2(g) ΔH=kJ·mol-1。
C6H5OH(g)+N2(g) ΔH=kJ·mol-1。 -
(2) 制备苯酚的苯和N2O的最佳投料比为10:1。此时,N2O、N2的平衡浓度分别为0.050mol/L、0.95mol/L。则制备反应的平衡常数Kc=(写出计算式)。
-
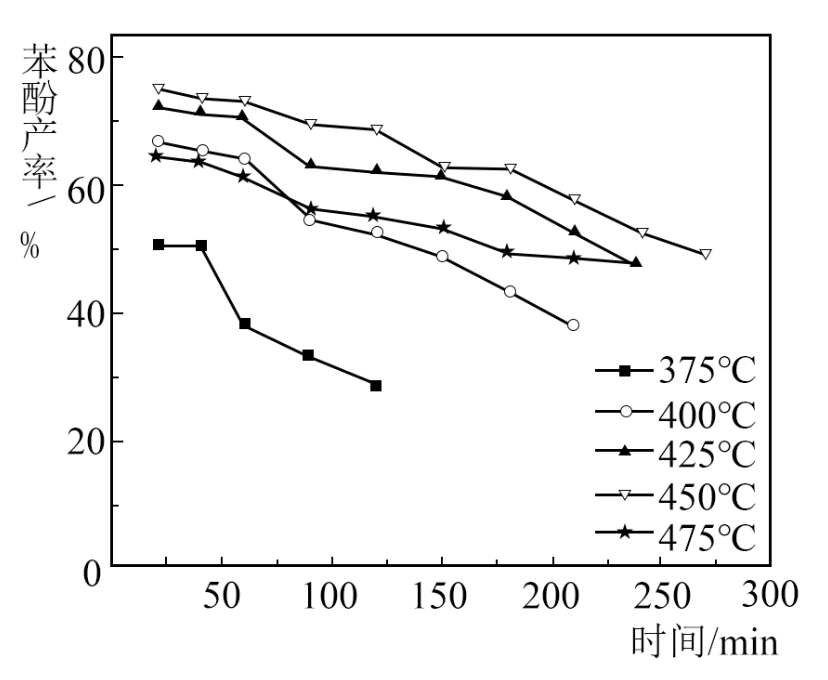
(3) 如图中,温度过低造成苯酚产率低的主要原因是;反应时间过长造成产率下降的可能原因是。
-
(4) 反应中使用更高效的催化剂(填“可”或“不可”)提高反应的平衡转化率。已知475℃下反应仍未达到平衡,此时的苯酚产率比450℃时的低,可能原因是。
-
(5) 研究表明,反应速率符合关系式v=kca(C6H6)cb(N2O),有关数据如表:
c(C6H6)/×10-3mol·L-1
c(N2O)/×10-3mol·L-1
v/×10-3mol·L-1·s-1
12
8.0
1.0
24
8.0
2.0
24
24
6.0
有人据此提出反应可分为三个步骤:
①N2O→N2+O*(活性氧) 快反应
②C6H6+O*→C6H5OH*(活性苯酚) 慢反应
③C6H5OH*→C6H5OH 快反应
下列有关说法正确的是____。
A . O*(活性氧)是该反应的催化剂 B . ②的反应的活化能最小 C . 反应速率v(N2O)=v(N2) D . 第二步中C6H6与O*的碰撞仅部分有效
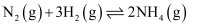
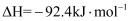 。
。
-
(1) 已知
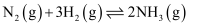 的活化能
的活化能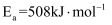 , 则氨分解反应:
, 则氨分解反应: 的活化能
的活化能
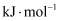 。
。
-
(2) 在一体积为2L的恒容刚性密闭容器中发生反应:
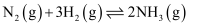 。在
。在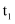 、
、 时刻改变反应的一个条件,Ⅰ、Ⅱ、Ⅲ阶段体系中各物质的物质的量随时间变化的曲线如图所示:
时刻改变反应的一个条件,Ⅰ、Ⅱ、Ⅲ阶段体系中各物质的物质的量随时间变化的曲线如图所示: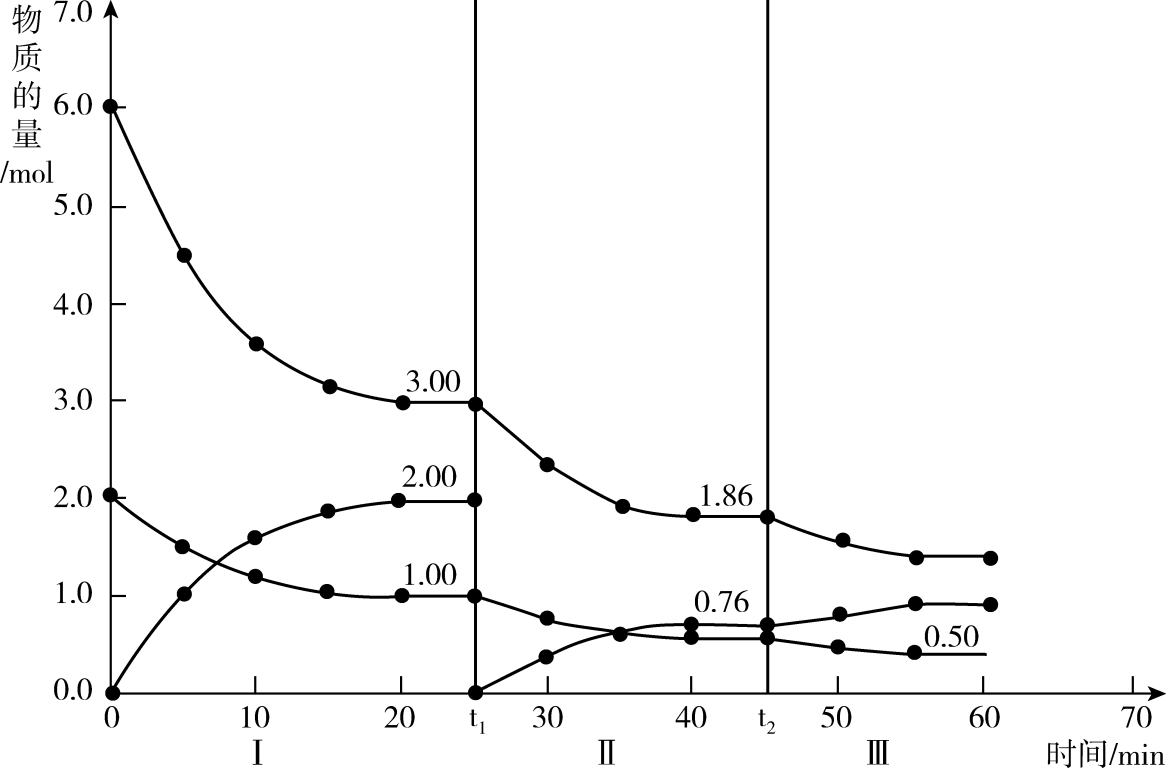
①第Ⅰ阶段的平衡常数
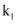 为(保留2位有效数字)。
为(保留2位有效数字)。②比较第Ⅱ阶段和第Ⅲ阶段平衡常数的大小:
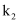
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。 -
(3) ①合成氨工业上通常采用铁触媒、在400~500℃和10MPa~30MPa的条件下合成氨,在Fe催化剂作用下的反应历程为(*表示吸附态)
化学吸附:
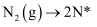 ;
;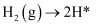 ;
;表面反应:
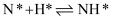 ;
;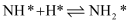 ;
;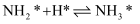
脱附:
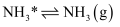
其中,
 的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。下列说法正确的是。
的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。下列说法正确的是。A.控制温度400~-500℃远高于室温,是为了保证尽可能的平衡转化率和快的反应速率
B.实际工艺中原料中
 和
和 物质的量之比为1∶2.8,氮气过量除了提高氢气的转化率,还可以提高整体反应速率
物质的量之比为1∶2.8,氮气过量除了提高氢气的转化率,还可以提高整体反应速率C.基于
 分子间有较强分子间作用力可将其液化,不断将液氨移去,有利于反应正向进行
分子间有较强分子间作用力可将其液化,不断将液氨移去,有利于反应正向进行D.
 、
、 的混合气只需一次通过合成塔
的混合气只需一次通过合成塔②我国科学家以
 为催化剂,在不同电解质溶液中实现常温电催化合成氨,其反应历程与相对能量模拟计算结果如图。
为催化剂,在不同电解质溶液中实现常温电催化合成氨,其反应历程与相对能量模拟计算结果如图。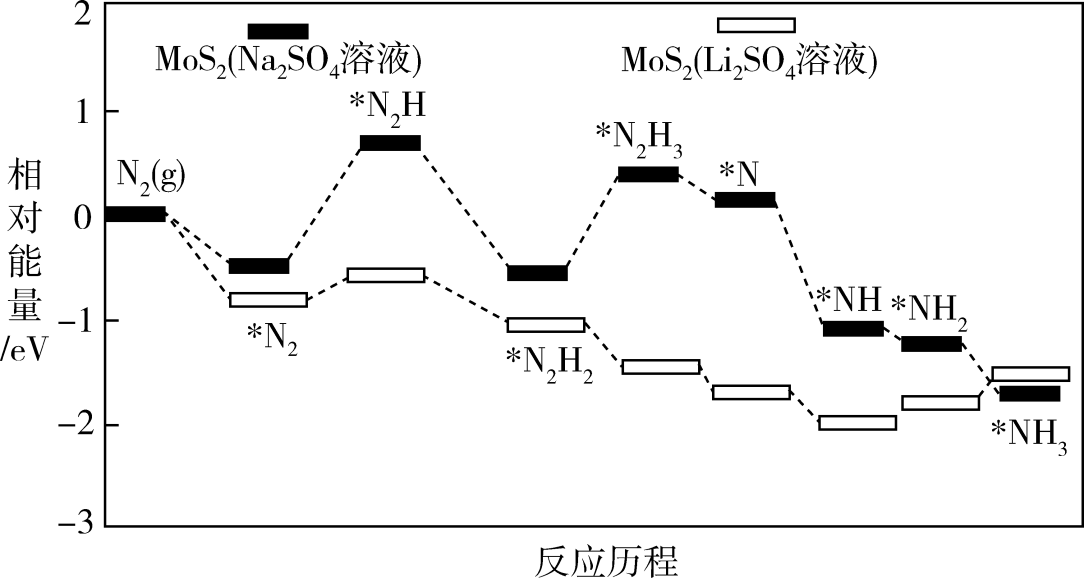
 在(填“
在(填“ ”或“
”或“ ”)溶液中催化效果更好:在
”)溶液中催化效果更好:在 溶液与
溶液与 溶液中,反应
溶液中,反应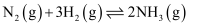 中的
中的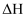 (填“前者大”“后者大”或“一样大”)。
(填“前者大”“后者大”或“一样大”)。
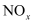 、
、 等)是主要的污染物之一,消除含氮化合物的污染倍受关注。
等)是主要的污染物之一,消除含氮化合物的污染倍受关注。
-
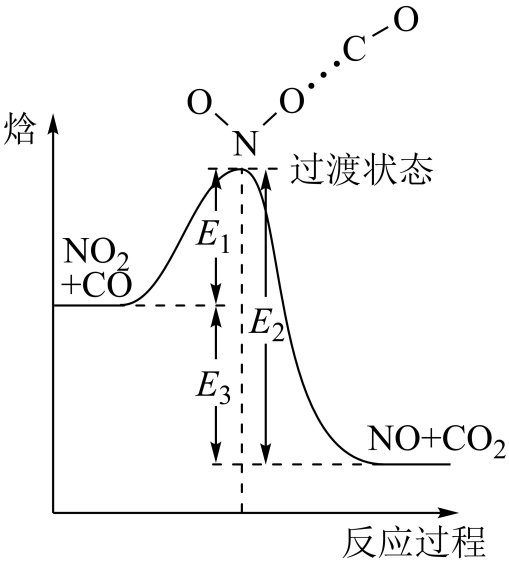
(1) 已知反应
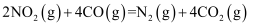
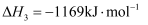 , 该逆反应活化能为
, 该逆反应活化能为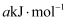 , 则其正反应活化能为
, 则其正反应活化能为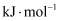 。(用含a的代数式表示)。
。(用含a的代数式表示)。
-
(2) 某种含二价铜微粒
 的催化剂可用于汽车尾气脱氮。催化机理如图1,反应历程如图2。
的催化剂可用于汽车尾气脱氮。催化机理如图1,反应历程如图2。
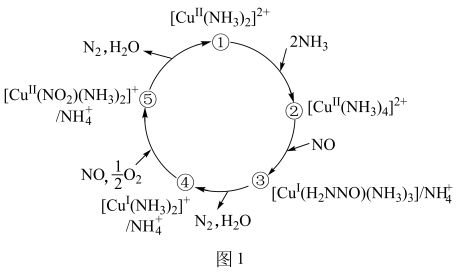
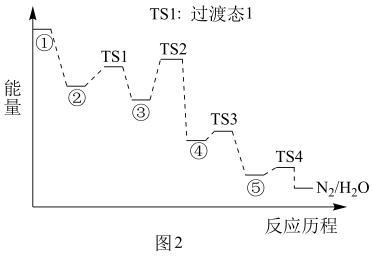
①从化学键的角度解释
 能结合
能结合 的原因:。
的原因:。②该脱氮过程的总反应方程式为。该反应历程的决速步骤是。(填选项)
a.状态①→状态② b.状态②→状态③
c.状态③→状态④ d.状态④→状态⑤
-
(3) 一种电解法处理含有
 、
、 的酸性废水,其工作原理及电极b中铁的化合物的催化机理如图3所示,H表示氢原子。
的酸性废水,其工作原理及电极b中铁的化合物的催化机理如图3所示,H表示氢原子。
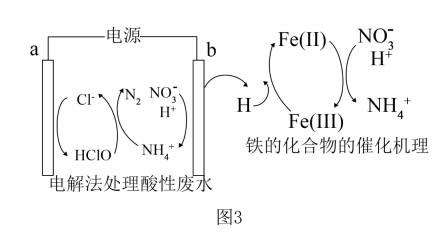
①写出阳极的电极反应方程式。
②电极b上铁的化合物催化含
 的酸性废水过程可描述为。
的酸性废水过程可描述为。
 加氢制
加氢制 是碳治理的重要方法,有利于实现碳资源的循环利用,体系中主要反应有:
是碳治理的重要方法,有利于实现碳资源的循环利用,体系中主要反应有:①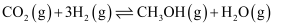
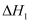
②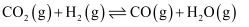

-
(1) 下表是部分化学键的键能数据
化学键
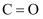
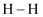
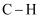
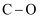
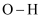
键能(
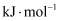 )
)803
436
414
326
464
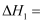 。反应①在(填“高温”或“低温”)条件下能自发进行。
。反应①在(填“高温”或“低温”)条件下能自发进行。 -
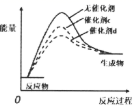
(2) 反应①在不同催化剂作用下的反应历程如图所示,催化效果更好的是(填“
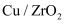 ”或“
”或“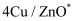 ”),判断依据是。
”),判断依据是。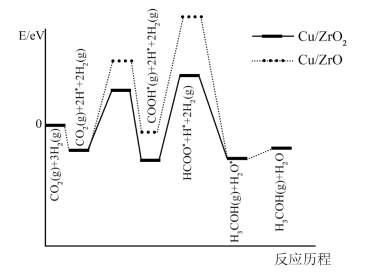
-
(3) 一定温度下,向容积为1L的密闭容器中加入1 mol
 和3 mol
和3 mol 发生反应①和②,达到平衡状态,
发生反应①和②,达到平衡状态, 平衡转化率为20%,
平衡转化率为20%, 的物质的量浓度为
的物质的量浓度为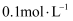 ,
,  的选择性=(
的选择性=( 的选择性
的选择性 ),反应①在该温度下的平衡常数
),反应①在该温度下的平衡常数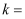
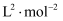 (写出计算式)。
(写出计算式)。
-
(4) 为提高
 的平衡产率,最佳反应条件为____。
A . 高温高压 B . 高温低压 C . 低温高压 D . 低温低压
的平衡产率,最佳反应条件为____。
A . 高温高压 B . 高温低压 C . 低温高压 D . 低温低压
- 根据图文材料(BS9为黄河三角洲示意图,图1O为珠江三角洲示意图),回答下列问題材料一:胜利油田在渤海采取海油陆采的方式
- 右图是研究二氧化硫性质的微型实验装置。现用60%的硫酸溶液和亚硫酸钠晶体制取SO 2 气体,实验现象很明显,且不易污染空
- 已知在数列中,,,. (1)证明数列是等差数列,并求的通项公式; ()设数列的前项和为,证明:.
- I don’t think the colour of you coat _____ very well with yo
- 造成温室效应的主要原因和缓解全球温室效应危机的重要措施分别是 A.煤、石油、天然气大量燃烧;植树造林 B.S
- 阅读下面这首唐诗,回答文后小题 陪金陵府相中堂夜宴 韦庄① 满耳笙歌满眼花,满楼珠翠胜吴娃②。 因知海上神仙窟,只似人间
- 温州市有一种可食用的野生菌,上市时,外商李经理按市场价格30元/千克收购了这种野生菌1000千克存放入冷库中,据预测,该
- 在下图右侧的四个三角形中,不能由△ABC经过旋转或平移得到的是( )
- 已知曲线,给出下列四个命题:①曲线与两坐标轴围 成的图形面积不大于;②曲线上的点到原点的距离的最小值为; ③曲线
- (8分)从高出地面3m的位置竖直向上抛出一个小球,它上升5m后回落,最后到达地面。规定竖直向上为正方向,若以抛出点为坐标
- 等物质的量的KClO3分别发生下述反应:①有MnO2催化剂存在时,受热分解得到氧气;②不使用催化剂,加热至470℃左右,
- 下列说法正确的是( ) A.空气的流动不属于机械运动 B.只有机器的运动才是机械运动 C
- 用哺乳动物的红细胞制备细胞膜的方法正确的是 ( )A.把细胞放在清水里,涨破细胞 B.用针戳
- 已知 (1)若时,求函数在点处的切线方程; (2)若函数在上是减函数,求实数的取值范围; (3)令是否存在实数,当是自然
- 西汉时期实行编户齐民制度,其最大特点是 ( )
- 清末自强运动时,恭亲王有一段话,颇能反映其主张与做法,兹录於下:“中国所当学者,固不止轮船,枪炮,即以轮船枪炮而论,雇买
- 印度的经济发展以美、欧、日为重点,积极拓展同发达国家的全面合作。同时,它也十 分重视同发展中国家的经济合作,成为世界经济
- 读“四种气候类型的气温与降水月份分配图”,完成1-2题。1.按顺序依次写出气候类型的名称() A.热带草原气候、热带
- 中华民族精神是中华民族自立于世界民族之林的基石和根本。在当代中国,弘扬和培育中华民族精神,最重要的是( ) A.正确对
- 2008年5月12日下午,四川汶川县发生了8.0级地震,造成重大人员伤亡。因此,有人认为,人在自然灾害面前是无能为力的。



