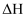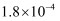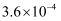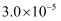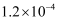活化能及其对化学反应速率的影响 知识点题库
CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1 I
CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1 I
CO2(g)+H2(g)  CO(g)+H2O(g) ΔH2 II
CO(g)+H2O(g) ΔH2 II
某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
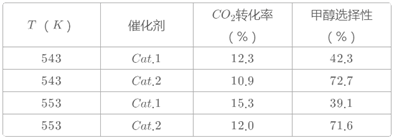
(备注)Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醇的百分比
已知:①CO和H2的标准燃烧热分别为-283.0kJ·mol-1和-285.8kJ·mol-1
②H2O(l)=H2O(g)ΔH3=44.0kJ·mol-1
请回答(不考虑温度对ΔH的影响):
-
(1) 反应I的平衡常数表达式K=;
-
(2) 有利于提高CO2转化为CH3OH平衡转化率的措施有___。A . 使用催化剂Cat.1 B . 使用催化剂Cat.2 C . 降低反应温度 D . 投料比不变,增加反应物的浓度 E . 增大CO2和H2的初始投料比
-
(3) 表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是。
-
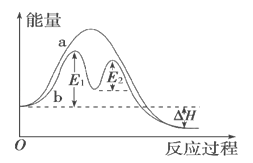
(4) 在图中分别画出反应I在无催化剂、有Cat.1和有Cat.2三种情况下“反应过程~能量”示意图。

反应I :C6H5CH2CH3(g)+CO2(g)  C6H5CH=CH2(g)+CO(g)+H2O(g) ΔH1=158.8 kJ/mol
C6H5CH=CH2(g)+CO(g)+H2O(g) ΔH1=158.8 kJ/mol
反应II :C6H5CH2CH3(g)  C6H5CH=CH2(g)+H2(g) ΔH2
C6H5CH=CH2(g)+H2(g) ΔH2
反应III :CO2(g)+H2(g)=CO(g)+H2O(g) ΔH3=41.2 kJ/mol
请回答:
-
(1) 反应II能够自发进行的条件(填“低温”、“高温”或“任何温度”)。
-
(2) 相同条件下,此工艺较乙苯直接分解制苯乙烯(反应II)的优势在于。
-
(3) 下列说法正确的是___________。A . 减压条件下有利于提高乙苯的平衡转化率 B . 可通过监测反应体系中CO(g)与H2O(g)浓度之比以判断是否达到平衡 C . 研发高效催化剂可提高苯乙烯的选择性,提高乙苯的平衡转化率 D . 利用过量O2替代CO2制取苯乙烯具有明显优势
-
(4) 常压下,乙苯分别在N2 (惰性介质)、CO2气氛中的平衡转化率与温度的关系如图所示。
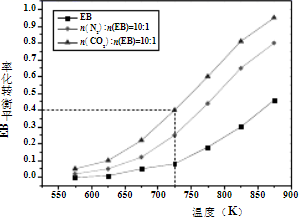
①常压、温度为725 K条件下,往容器中充入1 mol 乙苯、10 mol CO2 , 达到平衡时容器中有H2 0.08 mol。研究表明,45%的苯乙烯通过一步反应生成、55%的苯乙烯通过两步反应生成,反应Ⅲ的平衡常数K= (保留两位有效数字)。
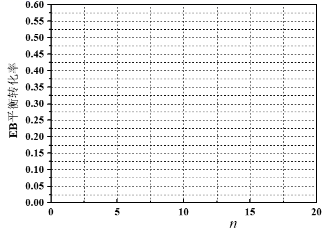
②常压、温度为725 K条件下,若N2或CO2与乙苯的物质的量之比为n:1,请分别画出乙苯的平衡转化率在N2或CO2气氛中随n变化的示意图。
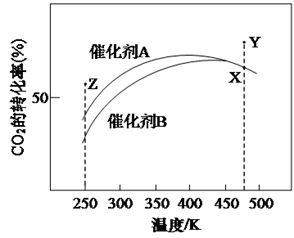
下列说法正确的是( )
 N2(g)+2CO2(g),反应过程中的能量变化如图所示。下列说法错误的是( )
N2(g)+2CO2(g),反应过程中的能量变化如图所示。下列说法错误的是( ) 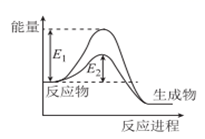
①673K时,NO2和CO发生基元反应(即一步完成):NO2+CO = NO+CO2 , 其反应过程如图所示:

②473K时,则经过两步反应,反应机理是:NO2+NO2→NO+ NO3(慢),CO+ NO3→NO2+CO2(快)。下列有关说法错误的是( )
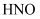 自由基与
自由基与  反应过程的能量变化如图所示:
反应过程的能量变化如图所示: 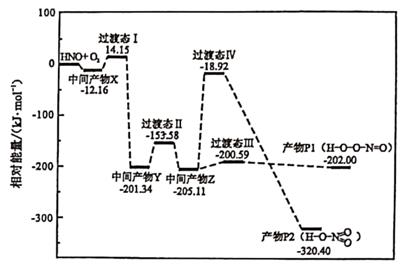
下列说法正确的是( )
 C . 该历程中最大正反应的活化能
C . 该历程中最大正反应的活化能 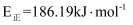 D . 相同条件下,由中间产物z转化为产物的速率:
D . 相同条件下,由中间产物z转化为产物的速率: 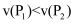
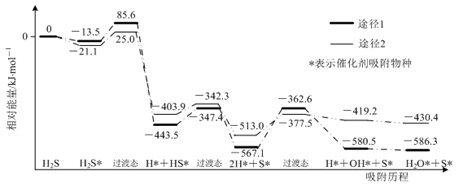
下列说法错误的是( )
-
(1) 工业上合成氨的反应为
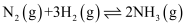
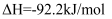 ,反应过程中能量变化如图所示。
,反应过程中能量变化如图所示。 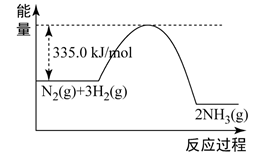
①反应
 的活化能为kJ/mol,有利于该反应自发进行的条件是。
的活化能为kJ/mol,有利于该反应自发进行的条件是。②合成氨时加入铁粉可以加快生成
 的速率,在上图中画出加入铁粉后的能量变化曲线。
的速率,在上图中画出加入铁粉后的能量变化曲线。 -
(2)
 催化重整不仅可以得到合成气(CO和
催化重整不仅可以得到合成气(CO和  ),还对温室气体的减排具有重要意义。回答下列问题:
),还对温室气体的减排具有重要意义。回答下列问题: ①
 催化重整反应为
催化重整反应为 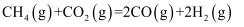
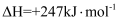 。某温度下,在体积为2L的容器中加入2mol
。某温度下,在体积为2L的容器中加入2mol  、1mol
、1mol  以及催化剂进行重整反应,5min达到平衡时
以及催化剂进行重整反应,5min达到平衡时  的转化率是50%。0-5min平均反应速率
的转化率是50%。0-5min平均反应速率 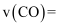
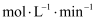
②反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如表:
积碳反应
消碳反应
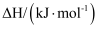
75
172
活化能/(
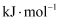 )
)催化剂X
33
91
催化剂Y
43
72
由上表判断,催化剂XY(填“优于”或“劣于”),理由是。
①I2(g)+H2(g)  2HI(g) △H=-9.48kJ·mol-1
2HI(g) △H=-9.48kJ·mol-1
②I2(s)+H2(g)  2HI(g) △H=+26.48kJ·mol-1
2HI(g) △H=+26.48kJ·mol-1
下列说法正确的是( )
 的反应历程如图所示。下列说法错误的是( )
的反应历程如图所示。下列说法错误的是( ) 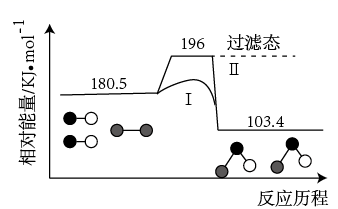
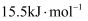 D .
D . 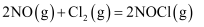 ,
, 
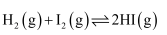 的相关信息如下表:
的相关信息如下表:
| 活化能Ea | H-H键能 | I-I键能 |
-11 | 173.1 | 436 | 151 |
键能:气态分子中1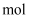 化学键解离成气态原子所吸收的能量。
化学键解离成气态原子所吸收的能量。
-
(1) 反应
 的焓变=
的焓变=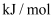 , 活化能=
, 活化能=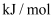 。
。
-
(2) 关于反应
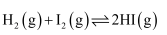 , 下列描述正确的是____A.
, 下列描述正确的是____A. 和
和 的总能量为587
的总能量为587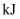 A .
A . 和
和 的总能量大于
的总能量大于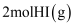 的能量
B . 加入催化剂,若正反应活化能减小100
的能量
B . 加入催化剂,若正反应活化能减小100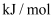 , 则逆反应活化能也减小100
, 则逆反应活化能也减小100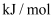 C . 恒温恒容,向已平衡体系中再加入
C . 恒温恒容,向已平衡体系中再加入 , 正反应活化能减小,逆反应活化能不变
, 正反应活化能减小,逆反应活化能不变
-
(3) 研究发现,大多数化学反应并不是经过简单碰撞就能完成的,而往往经过多个反应步骤才能实现。
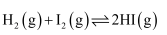 实际上是经过下列两步基元反应完成的:
实际上是经过下列两步基元反应完成的:基元反应i:
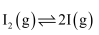 (快反应)
(快反应)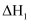 活化能:
活化能: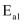
基元反应ii:
 (慢反应)
(慢反应) 活化能:
活化能: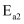
①决定
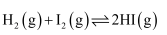 反应速率的步骤是(填“i”或“ii”),
反应速率的步骤是(填“i”或“ii”), 0(填“>”、“<”、“=”)
0(填“>”、“<”、“=”)②将
 和
和 通入1L容器中,达到化学平衡后将温度升高10℃,达到新平衡后,
通入1L容器中,达到化学平衡后将温度升高10℃,达到新平衡后, 较原平衡(填“增大”、“减小”或“不变”),请依据升高温度时基元反应i、ii的平衡移动情况,综合考虑浓度与温度对反应i平衡移动的影响,分析
较原平衡(填“增大”、“减小”或“不变”),请依据升高温度时基元反应i、ii的平衡移动情况,综合考虑浓度与温度对反应i平衡移动的影响,分析 变化的原因:。
变化的原因:。
-
(1) 丙烷脱氢制备丙烯。由图可得C3H8(g)=C3H6(g)+H2(g) ΔH=kJ·mol-1。
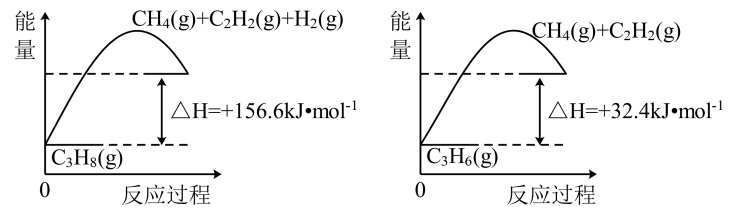
-
(2) 将一定浓度的CO2与固定浓度的C3H8通过含催化剂的恒容反应器发生脱氢反应。经相同时间,流出的C3H6、CO和H2浓度随初始CO2浓度的变化关系如下图所示。c(H2)和c(C3H6)变化差异的原因为(用化学方程式表示)。
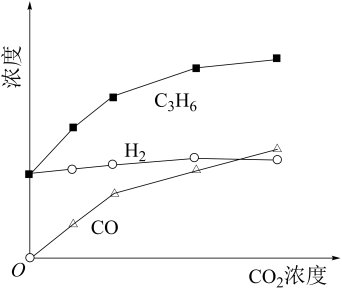
-
(3) 已知Arrhenius 经验公式为Rlnk=RlnA-
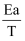 (Ea为活化能,k为速率常数,R、A为常数)。丙烷脱氢制备丙烯反应在某条件下的Arrhenius 经验公式的实验数据如图中曲线a所示,其活化能为J·mol-1 , 当其实验数据发生变化如图中b线所示,则可能的原因是。
(Ea为活化能,k为速率常数,R、A为常数)。丙烷脱氢制备丙烯反应在某条件下的Arrhenius 经验公式的实验数据如图中曲线a所示,其活化能为J·mol-1 , 当其实验数据发生变化如图中b线所示,则可能的原因是。
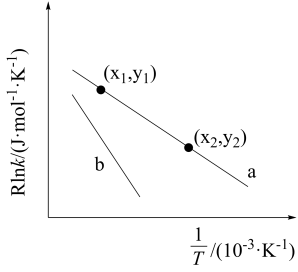
-
(4) 工业上用丙烯加成法制备1,2-二氯丙烷(CH2ClCHClCH3),副产物为3-氯丙烯(CH2=CHCH2Cl),反应原理为:
①CH2=CHCH3(g)+Cl2(g)→CH2ClCHClCH3 (g)
②CH2=CHCH3(g)+Cl2(g)→CH2=CHCH2Cl(g)+HCl(g)
一定温度下,向恒容密闭容器中充入等物质的量的CH2=CHCH3和Cl2发生反应,容器内气体的压强随时间的变化如下表所示。
时间/min
0
60
120
180
240
300
360
压强/kPa
80
74.2
69.2
65.2
61.6
58
58
该温度下,若平衡时HCl的体积分数为10%。此时CH2=CHCH3的转化率为。反应①的压力平衡常数Kp=kPa-1(保留小数点后2位)。
-
(5) 一定条件下,CH3CH=CH2与HCl发生反应有①、②两种可能,反应进程中的能量变化如图所示。
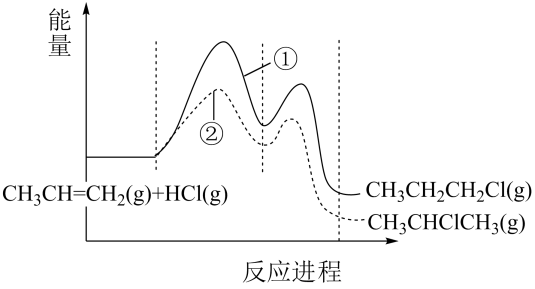
保持其他条件不变,若要提高产物中CH3CH2CH2Cl(g)的比例,可采用的措施是____。
A . 适当提高反应温度 B . 改变催化剂 C . 适当降低反应温度 D . 改变反应物浓度
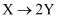 的影响,各物质浓度c随反应时间t的部分变化曲线如图,则( )
的影响,各物质浓度c随反应时间t的部分变化曲线如图,则( )
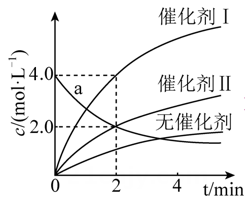
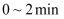 内,
内, 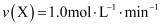
 和CO等,减少它们在大气中的排放是环境保护的重要内容之一。
和CO等,减少它们在大气中的排放是环境保护的重要内容之一。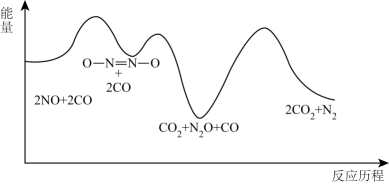
-
(1) 一定条件,反应
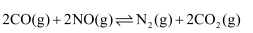 的反应历程如图所示,该历程分步进行,其中第步是决速步骤。
的反应历程如图所示,该历程分步进行,其中第步是决速步骤。
-
(2) 在恒温恒容密闭容器中进行上述反应,原料组成
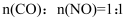 , 体系达到平衡时
, 体系达到平衡时 的体积分数为25%,则CO的平衡转化率=。
的体积分数为25%,则CO的平衡转化率=。
-
(3) 氮的氧化物脱除可用电化学原理处理,如下图装置可同时吸收
 和NO。已知:
和NO。已知: 是一种弱酸。直流电源的正极为(填“a”或“b”),阴极的电极反应式。该电解装置选择(填“阳”或“阴”)离子交换膜。
是一种弱酸。直流电源的正极为(填“a”或“b”),阴极的电极反应式。该电解装置选择(填“阳”或“阴”)离子交换膜。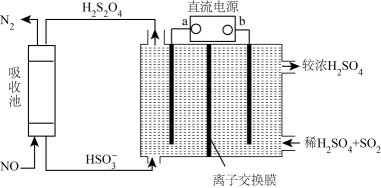
中国提出要实现“二氧化碳排放力争于2030年前达到峰值,争取在2060年前实现碳中和”的目标,二氧化碳的资源化利用对实现碳中和目标具有促进作用。
-
(4) 在一定条件下,向体积为2L的恒容密闭容器中通入1mol
 和3mol
和3mol , 发生反应
, 发生反应 , 测得
, 测得 和
和 随时间变化如图所示。
随时间变化如图所示。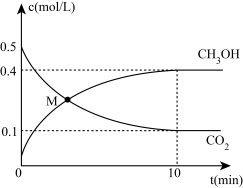
①M点时,
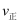
 。(填“>”、“<”或“=”)
。(填“>”、“<”或“=”)②下列叙述中一定能说明该反应达到平衡状态的是。
A.化学反应速率关系:
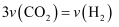
B.容器内混合气体的密度不再改变
C.单位时间内,每断裂2个C=O键,同时断裂3个O-H键
D.容器内混合气体的平均摩尔质量不再改变
-
(1) 一种重要的工业制备甲醇的反应为CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H。
CH3OH(g)+H2O(g) △H。 已知:①CO(g)+H2O(g)
 CO2(g)+H2(g) △H1=-40.9kJ·mol-1
CO2(g)+H2(g) △H1=-40.9kJ·mol-1②CO(g)+2H2O(g)
 CH3OH(g) △H2=-90.4kJ·mol-1
CH3OH(g) △H2=-90.4kJ·mol-1试计算制备反应的△H=。
-
(2) 对于反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),v正=k正p(CO2)·p3(H2),v逆=k逆·p(CH3OH)
CH3OH(g)+H2O(g),v正=k正p(CO2)·p3(H2),v逆=k逆·p(CH3OH) ·p(H2O)。其中k正、k逆分别为正、逆反应速率常数,p为气体分压(分压=物质的量分数×总压)。
在540K下,按初始投料比n(CO2):n(H2)=3:l、n(CO2):n(H2)=1:1、n(CO2):n(H2)=1:3,得到不同压强条件下H2的平衡转化率关系图:
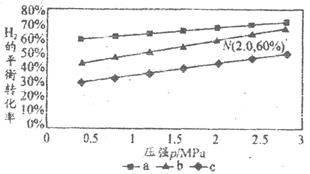
①比较a、b、c各曲线所表示的投料比大小顺序为(用字母表示)。
②点N在线b上,计算540K的压强平衡常数Kp=(用平衡分压代替平衡浓度计算)。
③540K条件下,某容器测得某时刻p(CO2)=0.2MPa,p(CH3OH)=p(H2O)=0.1MPa,
p(H2)=0.4MPa,此时v正:v逆=。
-
(3) 甲醇催化可制取丙烯,反应为:
3CH3OH(g)
 C3H6(g)+3H2O(g),反应的Arrhenius经验公式的实验数据如下图中曲线a所示,已知Arrhenius经验公式为R lnk=
C3H6(g)+3H2O(g),反应的Arrhenius经验公式的实验数据如下图中曲线a所示,已知Arrhenius经验公式为R lnk=  (Ea为活化能,k为速率常数,R和C为常数)
(Ea为活化能,k为速率常数,R和C为常数)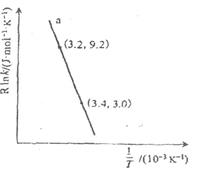
①该反应的活化能Ea=kJ·mol-1。
②当使用更高效催化剂时,在图中画出R lnk与
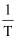 关系的示意图。
关系的示意图。 -
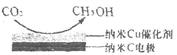
(4) 在饱和KHCO3电解液中,电解活化的CO2也可以制备CH3OH,其原理如下图所示,则
阴极的电极反应式为。
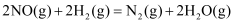 包含下列两步:①
包含下列两步:①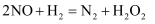 (慢)、②
(慢)、② (快),第一步反应的速率表达式为
(快),第一步反应的速率表达式为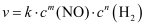 , 式中k为常数,m、n值可用下表中数据确定。T℃时测得有关实验数据如下:
, 式中k为常数,m、n值可用下表中数据确定。T℃时测得有关实验数据如下:序号 | c(NO)/(mol/L) | c(H2)/(mol/L) | 速率/(mol/(L·min)) |
I | 0.0060 | 0.0010 |
|
II | 0.0060 | 0.0020 |
|
III | 0.0010 | 0.0060 |
|
IV | 0.0020 | 0.0060 |
|
下列说法正确的是( )
 D . 相同条件下,浓度对反应速率的影响:
D . 相同条件下,浓度对反应速率的影响: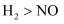
- 阅读材料,回答下列问题。 材料一 2009年5月16日我国局部地区地面天气图(单位:百帕) 材料二(1)图中A处天
- 英国医生赛达尼任格在对离体蛙心进行灌注实验时发现:用不含钙和钾的生理盐水灌注,蛙心收缩不能维持;用少量钙和钾的生理盐水灌
- He prefers ________ indoors ________ out this afternoon. A.
- 读图完成下列问题。 (1)造成D河河口附近著名古迹严重缺损的主要原因是( ) A.人类活动影响
- 把6mol气体A和5mol气体B通入容积为4 L的密闭容器中,在一定条件下发生如下反应:3A(g)+B(g)2C(g)+
- 简述党在抗日民族统一战线中的策略总方针。
- 如图所示为一列向某方向传播的简谐横波在某时刻的波形图,在波的传播方向上有一质点P在该时刻的振动方向如图.由图可知(
- 《独立宣言》被马克思称为“第一个人权宣言”,主要是因为它 ( ) A.宣告了美利坚和众国的诞生
- 新航路开辟后,西欧最早期的殖民者从美洲掠夺来大量黄金白银财富。这些黄金白银财富主要流入西班牙,这直接导致该国 A.国力增
- 图1是某县参加2007年高考的学生身高条形统计图,从左到右的各条形图表示学生人数 依次记为A1、A2、…A10(如A2表
- 2.在下面一段话的空缺处依次填入词语,最恰当的一组是 ( ) 独自坐在火炉旁边,静静地凝视面前 的
- .下列图片选自同一本著作,结合所学知识判断这些图片出自 农耕
- 2016年3月16日,我国首部《慈善法》获得第十二届全国人大四次会议表决通过,将于今年9月1日起施行。《慈善法》获得表决
- 人类已进入信息社会,光导纤维是传递信息的重要材料,光导纤维属于( ) A.有机高分子材料
- 设双曲线x2-y2=1的两条渐近线与右准线的三角区域(包含边界)D,P(x,y)为D内一个动点,则目标函数z=x-2y的
- 某反应的ΔH=+100 kJ·mol-1,下列有关该反应的叙述正确的是() A.正反应活化能小于100 kJ·mol-1
- “无边落木萧萧下,不尽长江滚滚来”,优雅的诗句中不仅描述了秋季美景,也包含了许多物理知识,其中“不尽长江滚滚来”主要是由
- 下列各组词语中加点的字的读音,与所给注音全部相同的一组是 A、角jiǎo 号角 角落 头角 群雄角逐
- 已知公差为正数的等差数列{an}满足a1=1,2a1,a3﹣1,a4+1成等比数列. (Ⅰ) 求{an}的通项公式; (
- (09威海).小明同学在课外用易拉罐做成如图1所示的装置做小孔成像实验,如果易拉罐底部有一个很小的三角形小孔,则他在半透