第1章 认识化学科学 知识点题库
 数目为0.1NA
C . 1 mol K2Cr2O7被还原为Cr3+转移的电子数为6NA
D . 48 g正丁烷和10 g异丁烷的混合物中共价键数目为13NA
数目为0.1NA
C . 1 mol K2Cr2O7被还原为Cr3+转移的电子数为6NA
D . 48 g正丁烷和10 g异丁烷的混合物中共价键数目为13NA
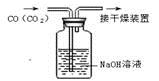 B . 苯萃取碘水中的I2分出水层后的操作
B . 苯萃取碘水中的I2分出水层后的操作 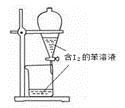 C . 配制0.10 mol·L-1NaOH溶液
C . 配制0.10 mol·L-1NaOH溶液 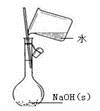 D . 记录滴定终点读数为12.20mL
D . 记录滴定终点读数为12.20mL 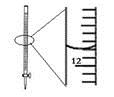
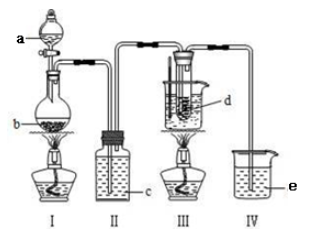
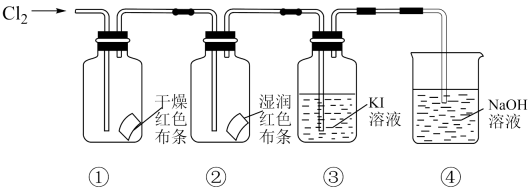
a为浓盐酸,b为MnO2 , c为饱和食盐水, d为30%KOH溶液,e为NaOH溶液
回答下列问题:
-
(1) 检查装置气密性后,添加药品,待装置III水温升至75℃开始反应。
①装置I中反应的离子方程式为。
②若取消装置II,对本实验的影响是。
③实验结束,拆解装置I前为了防止大量氯气逸出,可采取的措施是。
④从装置III的试管中分离得到KClO3粗产品,其中混有的杂质是KClO和。
-
(2) 为测定产品KClO3的纯度,进行如下实验:
步骤1:取2.45g样品溶于水配成250mL溶液。
步骤2:取25.00mL溶液于锥形瓶中,调至pH=10, 滴加足量H2O2溶液充分振荡以除尽ClO-。然后煮沸溶液1~2分钟,冷却。
步骤3:加入过量KI溶液,再逐滴加入足量稀硫酸。(ClO3-+6I-+6H+=Cl-+3I2+3H2O)
步骤4:加入指示剂,用0.5000mol/LNa2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。 (2S2O32-+I2=S4O62-+2I-)
①步骤2中除去ClO-的离子方程式是。“煮沸”的目的是。
②比较碱性条件下氧化性ClO3-ClO- (填写“>”或“<”)。
③样品中KClO3的貭量分数为。(答案保留三位有效数字, KClO3式量:122.5)
①标准状况下,1L HCl和1L H2O的物质的量相同
②标准状况下,11.2L H2和14g N2所含原子数相同
③28g CO的体积约为22.4L
④两种物质的物质的量相同,则它们在标准状况下的体积相同
⑤同温同体积时,气体物质的物质的量越大,则压强越大
⑥同温同压下,气体的密度与气体的相对分子质量成正比
-
(1) 浓盐酸在反应中表现出来的性质是(填写编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
-
(2) 氧化剂与还原剂物质的量之比为,若产生0.1molCl2 , 则转移电子的物质的量为mol。
A.NaHCO3 B.Na2CO3 C.Fe2O3 D.Ca(ClO)2 E. KAl(SO4)2·12H2O
-
(1) 俗称铁红的物质;
-
(2) 漂白粉的有效成分;
-
(3) 一种常见净水剂;
-
(4) 常用于焙制糕点的小苏打;
-
(5) 制普通玻璃的原料是石英、石灰石和。
 增大
增大
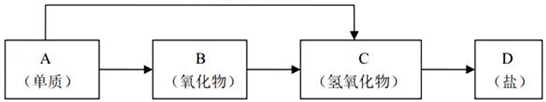
-
(1) 若B为呼吸面具中的供氧剂,其供氧时每生成1molO2 , 反应过程中转移的电子数为,A与水反应的离子方程式为:。
-
(2) 200℃时,11.6g CO2和H2O的混合物气体与足量的B反应,反应后固体增加了3.6g,则原混合物的平均相对分子质量为。
-
(3) 写出一种“C→D”转化的离子方程式:。
-
(4) 某同学将一小块A单质露置于空气中,观察到下列现象:
银白色
 变灰暗
变灰暗  变白色
变白色  出现液滴
出现液滴  白色固体
白色固体则下列说法正确的是_____________________。
A . ①发生了氧化还原反应 B . ①变灰暗色是因为生成了过氧化钠 C . ③是碳酸钠吸收空气中的水蒸气形成了溶液 D . ④只发生物理变化
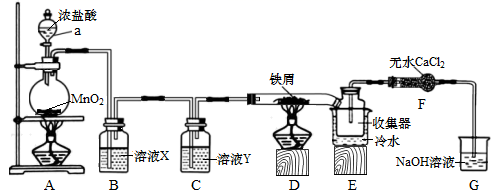
回答下列问题:
-
(1) 仪器a的名称是,装置A发生反应的化学方程式为。
-
(2) 溶液X、Y依次是、;装置D发生反应的化学方程式为。
-
(3) 实验结束时,应先熄灭(填“A”或“D”)处酒精灯;E中冷水的作用是。
-
(4) 装置F的作用是;装置G发生反应的离子方程式。
①  与
与 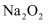 都能和水反应生成碱,它们都是碱性氧化物
都能和水反应生成碱,它们都是碱性氧化物
②  与
与  发生化合反应生成
发生化合反应生成  ,
, 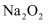 与
与  发生置换反应生成
发生置换反应生成 
③  是淡黄色物质,
是淡黄色物质, 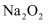 是白色物质
是白色物质
④ 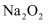 可作供氧剂,而
可作供氧剂,而  不可
不可
⑤ 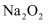 和
和  的焰色均为黄色
的焰色均为黄色

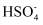 的摩尔质量为97
B . 第I阶段的反应中NO2被氧化
C . HNO2、NO2、H2O均为电解质
D . 第II、III阶段总反应的化学方程式为
的摩尔质量为97
B . 第I阶段的反应中NO2被氧化
C . HNO2、NO2、H2O均为电解质
D . 第II、III阶段总反应的化学方程式为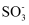 +H2O+NO2=HNO2+
+H2O+NO2=HNO2+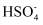
- 将下列语句依次填入文中的横线处,使上下文语意连贯,只填序号。 大沙丘的景致是典型的好莱坞西部片中的景色,戈壁,蓝天,还有
- 已知,过的直线与轴和轴分别交于两点,若恰为线段的中点,求两点的坐标.
- (Ⅰ)有机物M满足下列条件: ①它在空气中完全燃烧的产物是CO2和H2O,且燃烧过程中产生CO2的物质的量正好等于消耗掉
- (2分)某研究性学习小组的成员要测量某一电阻Rx较精确的阻值,他们先用多用电表粗测电阻Rx,所用多用电表的欧姆挡有×1,
- 研究NO2、SO2、CO等大气污染气体的处理具有重要意义。 (1)NO2可用水吸收,相应的化学反应方程式为_______
- 对可逆反应4NH3(g)+5O2(g)4NO(g)+6H2O(g),下列叙述中正确的是( )A.达到化学平衡时,4
- 已知:在△ABC中,AB=AC,D为AC的中点,DE⊥AB,DF⊥BC,垂足分别为点E,F,且DE=DF。求证:△ABC
- 读四省区水稻、小麦、棉花、油菜播种面积统计图,甲、乙、丙、丁分别代表的省区是( ) A.新疆、湖北
- 某电视台招聘业余记者、业余播音员各一名。假如你打算应聘,请按不同的目的各写一句话,分别从三个方面介绍自己的优势,每句话不
- 补写下列名篇名句中的空缺部分。(6分) (1)
- ---Tom, keep your_____ on your studies. --- Sure, mum. I'
- 配制一定溶质质量分数的氯化钠溶液,下列实验操作不正确的是 A.氯化钠
- 设nA为阿伏伽德罗常数的值,下列说法正确的是 A.2.24L NO2含有氧原子数为0.2nAB.常温常压下,乙烯和环丙烷
- 如果你的家人冬季到英国去旅行,你会告诉他,那里( )A.冬季比北京冷 B.冬季比北京温
- 若△ABC和△DEF的面积分别为、. (1)如图①,AC=DF,BC=DE,∠C=30°,∠D=150°,比较S1与S2
- (2014•郴州)花粉从花药中散放而落到雌蕊柱头上的过程,以及胚珠里的卵细胞与来自花粉管中的精子,形成受精的过程,依次叫
- 以党的十一届三中全会的召开为标志,我国开始了历史发展的伟大转折,进入改革开放和社会主义事业发展的新时期。请回答:(14分
- My MP4 has disappeared. Who _______ have taken it away?
- 某学校在组织教职员工体检时,发现有4名教职员工分别患有肺结核、痢疾、甲型流感、急性阑尾炎等疾病,那么与他们共同工作、生活
- 自然界中动物种类繁多,形态千差万别。下列哪种描述是正确的是 A.蚯蚓身体分节,因此蚯蚓属于节肢动物 B.身体分为头、胸、



