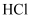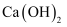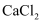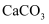第1章 认识化学科学 知识点题库
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A . 所含共价键数均为0.2NA的白磷(P4)和甲烷的物质的量相等
B . 1L 1mol/LH2O2的水溶液中含有的氧原子数为2NA
C . 将1molFe 与一定量的稀硝酸充分反应,转移的电子数可能为2NA
D . 1L0.1mol/LCH3COONa溶液中含有的Na+和CH3COO-的总数为0.2NA
碘是人体不可缺乏的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:KIO3+5KI
+3H2SO4=3I2+3H2O+3K2SO4
-
(1) 该反应的氧化剂是;氧化产物与还原产物的物质的量比是;如果反应生成0.3mol的单质碘,则转移的电子数目是。
-
(2) 先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,最后加入一定量的CCl4 , 振荡,这时候,观察到的现象是;
-
(3) 若采用下图实验装置将四氯化碳和I2的混合溶液分离。
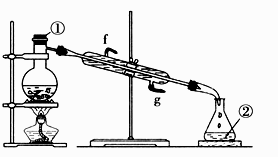
写出图中仪器的名称:①;该装置还缺少的仪器是;冷凝管的进水口是:(填g或f)
-
(4) 在容量瓶的使用方法中,下列操作正确的是
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
D.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
-
(5) 上面实验中用到一定物质的量浓度的稀硫酸,若配制0.5mol/L的硫酸溶液500mL,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为mL,如果实验室有15mL、20mL、50mL量筒,应选用mL量筒最好。
-
(6) 下面操作造成所配稀硫酸溶液浓度偏高的是_____________。A . 溶解的时候溶液没有冷却到室温就转移 B . 转移时没有洗涤烧杯、玻璃棒 C . 向容量瓶加水定容时眼睛俯视 D . 用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶 E . 摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
下列说法中正确的是 ( )
A . 若1 mol甲烷的体积为22.4 L,则一定是在标准状况下
B . 在0℃、101kPa下,2 mol 氧气和氢气的混合气体的体积约为44.8 L
C . 在标准状况下,1 mol水的体积为22.4 L
D . 1 mol O2 的质量只有在标准状况下才约是32 g
将1.95g由Na2SO4和Na2CO3组成的混合物溶于水得溶液A,在A中加入10mL未知的BaCl2溶液恰好完全反应,过滤得沉淀B,向B中加入足量稀盐酸,充分反应后剩余沉淀2.33g。计算:
-
(1) 原混合物中Na2CO3的质量分数。
-
(2) BaCl2溶液的物质的量浓度。
某同学在实验室欲配制物质的量浓度均为 1.0mol/L的NaOH溶液、稀硫酸各450ml.提供的试剂是:NaOH固体、98% 的浓硫酸(密度为1.84g/cm3 )和蒸馏水.
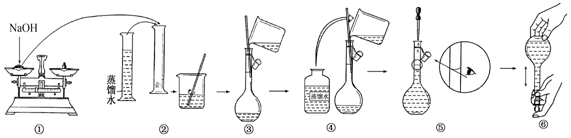
-
(1) 请你观察图示判断其中错误的操作有 (填序号).
-
(2) 应用托盘天平称量NaOH g,应用量筒量取浓硫酸mL.
-
(3) 浓硫酸溶于水的正确操作方法是
-
(4) 在配制H2SO4溶液实验中,下列操作引起结果偏高的有___________A . 该学生在量取浓硫酸时,俯视刻度线 B . 溶解硫酸后没有冷却至室温就立即完成后面的配制操作 C . 在烧杯中溶解搅拌时,溅出少量溶液 D . 没有用蒸馏水洗涤烧杯2~3次,并将洗液移入容量瓶中 E . 将量筒洗涤2~3次,并全部转移至容量瓶中 F . 容量瓶中原来存有少量蒸馏水 G . 胶头滴管加水定容时俯视刻度
实验室用碳酸钠晶体配制0.500
mol/L的Na2CO3溶液100mL,回答下列问题:
-
(1) 所需主要仪器为:药匙、托盘天平、烧杯、胶头滴管、、 .
-
(2) 本实验须称量碳酸钠晶体(Na2CO3•10H2O)g。
-
(3) ①如果定容时仰视会导致溶液浓度(填“偏高”、“偏低”或 “无影响” 下同);
②容量瓶未经干燥就用来配制该溶液,会导致溶液浓度 ;
-
(1) 在100mL 1.0mol/L的Na2SO4溶液中,Na+的物质的量浓度为 , 溶质Na2SO4的物质的量为
-
(2) 32gSO2在标准状况下的体积为,其中含氧原子的物质的量为
在给定条件下,下列加点的物质在化学反应中能完全消耗的是( )
A . 向150mL3mol·L-1的稀硝酸中加入6.4g铜
B . 标准状况下,将1g铁片投入15mL18.4mol·L-1的硫酸中
C . 用50mL8mol·L-1浓盐酸与10g二氧化锰共热制取氯气
D . 5×107Pa、500℃和铁触媒条件下,用1mol氮气和4mol氢气合成氨
下列说法正确的是( )
A . 光照氯水有气泡逸出,该气体是Cl2
B . 新制氯水呈黄绿色是因为其中存在Cl2
C . 久置氯水遇AgNO3溶液不会产生白色沉淀
D . 新制氯水光照一段时间后酸性减弱
ag气体A与bg气体B的分子数相同,下列说法错误的是( )
A . 同温同压下A,B两气体的密度之比为b:a
B . A与B的相对分子质量之比为a:b
C . 同质量气体A与B的分子数之比为b:a
D . 相同状况下同体积A,B的质量之比为a:b
利用下列装置进行相关实验,能达到实验目的的是( )
A . 加热熔融的纯碱固体 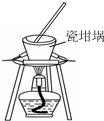 B . 收集CO2
B . 收集CO2 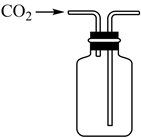 C . 配制一定物质的量浓度的H2SO4溶液
C . 配制一定物质的量浓度的H2SO4溶液 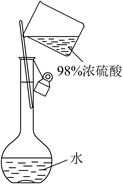 D . 测量氨气的体积
D . 测量氨气的体积 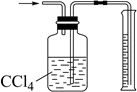
 B . 收集CO2
B . 收集CO2  C . 配制一定物质的量浓度的H2SO4溶液
C . 配制一定物质的量浓度的H2SO4溶液  D . 测量氨气的体积
D . 测量氨气的体积 
-
(1) Ⅰ.装置如图所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。请回答:
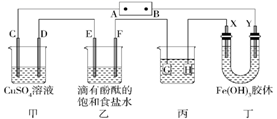
若AB电源是甲醇在酸性环境的燃料电池,则甲中C极的电极反应式为。
-
(2) 若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为。
-
(3) 丙是一个给铜件镀银的装置,当乙中溶液的c(OH-)=0.1mol/L时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为 g。
-
(4) Ⅱ.某同学用稀硝酸和铜反应制NO,发现化学反应速率较慢,因此改用浓硝酸按下图所示装置制取NO。
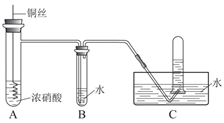
浓硝酸一般盛放在棕色试剂瓶中,原因是。
-
(5) B中反应的化学方程式是。
用NaOH固体配制一定物质的量浓度的NaOH溶液,造成所配溶液浓度偏高的原因是( )
A . 所用NaOH已吸潮
B . 定容时俯视刻度线
C . 溶解转移后未洗涤烧杯
D . 容量瓶未干燥
化学与科学技术的发展密切相关,技术的进步为化学的研究奠定了基础。下列说法错误的是( )
A . 就化工生产与技术的发展而言,催化剂往往成为技术改造和更新的关键
B . 酸碱中和滴定时只能用石蕊试液作终点指示剂,没有其他更好的办法
C . 利用飞秒激光脉冲技术使化学动力学研究进入分子动态学的领域
D . 利用比色分析的分光光度计可以帮助测定某些化学反应的反应速率
关于阿伏加德罗常数(用NA表示),下列叙述正确的是( )
A . 22.4L(标准状况)氖气含有的原子数为NA
B . 71g氯气溶于水,得到的水溶液中含有的Cl-的个数为2NA
C . 0.1mol/L的硫酸溶液中含有的氢原子个数为0.2NA
D . 1L浓度为2mol/L的NaCl溶液倒出一半后,剩余溶液浓度为1mol/L
 和
和 是生活中常见物质。下列方法无法区分两者的是( )
是生活中常见物质。下列方法无法区分两者的是( )
A . 分别取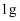 固体,各滴入几滴水,观察现象
B . 分别取
固体,各滴入几滴水,观察现象
B . 分别取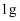 固体,各加入
固体,各加入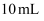 水,振荡,滴入几滴酚酞溶液,观察现象
C . 取等体积、等浓度两种物质的溶液,各加入少量
水,振荡,滴入几滴酚酞溶液,观察现象
C . 取等体积、等浓度两种物质的溶液,各加入少量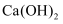 溶液,观察现象
D . 分别对两种固体用酒精灯加热,将产生的气体通入石灰水,观察现象
溶液,观察现象
D . 分别对两种固体用酒精灯加热,将产生的气体通入石灰水,观察现象
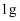 固体,各滴入几滴水,观察现象
B . 分别取
固体,各滴入几滴水,观察现象
B . 分别取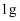 固体,各加入
固体,各加入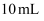 水,振荡,滴入几滴酚酞溶液,观察现象
C . 取等体积、等浓度两种物质的溶液,各加入少量
水,振荡,滴入几滴酚酞溶液,观察现象
C . 取等体积、等浓度两种物质的溶液,各加入少量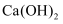 溶液,观察现象
D . 分别对两种固体用酒精灯加热,将产生的气体通入石灰水,观察现象
溶液,观察现象
D . 分别对两种固体用酒精灯加热,将产生的气体通入石灰水,观察现象
-
(1) 请写出
 溶液呈酸性的原因(用离子方程式表示)。
溶液呈酸性的原因(用离子方程式表示)。
-
(2) 氯元素在元素周期表中的位置,请用化学方程式表达实验室制氯气的原理。
-
(3)
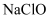 和
和 的混合溶液可用于
的混合溶液可用于 的尾气处理,请写出该反应的离子方程式。
的尾气处理,请写出该反应的离子方程式。
下列说法正确的是( )
A . 标准状况下,相同体积 H2 和 H2O 中所含的 H 原子数相等
B . 2.3g 钠分别完全转化为 Na2O 和 Na2O2 时转移的电子数相等
C . 相同物质的量 C2H4 和C3H6 所含 C-H 键的数目相等
D . 0.1mol/L 的 CH3COOH 和 CH3COONa 溶液中的 c(CH3COO-)相等
11.2g铁屑溶于100mL稀硫酸中,恰好完全反应。计算:
-
(1) 稀硫酸的物质的量浓度。
-
(2) 生成标准状况下H2的体积
物质间的转化体现了化学学科核心素养之一——变化观念。已知甲、乙、丙三种物质有如图所示的转化关系(→表示反应一步实现,部分物质和反应条件已略去)。则下列不符合甲、乙、丙相互转化关系的是( )
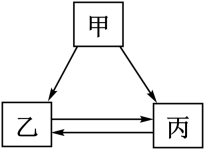
选项 | 甲 | 乙 | 丙 |
A |
|
|
|
B |
|
|
|
C |
|
|
|
D |
|
|
|
A . A
B . B
C . C
D . D
最近更新
- 如图所示,用细线吊着一个质量为m的小球,使小球在空中某一水平面内做圆锥摆运动,关于小球受力和运动情况的说法,错误的是(
- 如果椭圆的弦被点(4,2)平分,则这条弦所在的直线方程是___________。
- In after-school activities,students are into different
- 日本外务省次官粟山尚一在《动荡的90年代与日本外交的新展开》 中写道:“ 当今世界20万亿美元的国民生产总值中,美欧各占
- 在如图所示的四种电场中,分别标记有a、b两点。其中a、b两点的电势相等,电场强度大小相等、方向也相同的是 (
- - You should stop _______a rest after reading for such a lo
- 判断下列语句是否是全称命题或特称命题.(1)有一个实数a,a不能取对数.(2)所有不等式的解集A,都有AR.(3)三角函
- 设{an}是公差不为0的等差数列,a1=2,且a1,a3,a6成等比数列,则{an}的前n项和Sn=() A.+
- 24.右图反映了我国某一时期的对台政策,其转变始于 A.《告台湾同胞书》 B.《关于台湾回归祖国,实现和平统一的方针政策
- 生活中常常利用地图,相信你已经掌握了地图的基本知识,仔细阅读下图,完成 (1)、(2)题。 (1)学校在
- 现有部分短周期元素的性质或原子结构如下表: 元素编号 元素性质或原子结构 T M层上有6个电子 X 最外层电子数是次外层
- 1975年的全国整顿与1978年关于真理标准问题的讨论,二者的共同点是 ( )
- He used ___on the right in China, but he soon was used ____
- To improve our spoken English, we should practice _____ Engl
- 具有明显的主动运动能力的水生生物群落是: A 浮游生物 B 底栖生物 C 自游生物 D 漂浮植
- 党的十八大把对反腐败的认识提升到前所未有的高度,指出“不管什么人,不论权力大小、 职位髙低,只要触犯党纪国法,都要严惩不
- -- I book a table for dinner a few days ahead of time?
- 如图是“嫦娥二号”奔月示意图,卫星发射后直接进入地月转移轨道,最终被月球引力捕获,成为绕月卫星,并开展对月球的探测.下列
- 如图9-48,在一次暖气管道的铺设工作中,工程是由A点出发沿正西方向进行的,在A点的南偏西60°的方向上有一所学校,学校
- 目前,珠洲三角洲地区工业化与城市化,出现一系列问题的原因有 ①产业基础薄弱 ②市场腹地范围较小 ③城市缺乏合理的规划与