第1章 认识化学科学 知识点题库
①50mL12mol/L的盐酸与足量MnO2共热,转移电子数为0.3NA
②2.0gH218O与D216O的混合物中所含中子数为NA
③常温常压下,14 g 由N2与CO组成的混合气体含有的原子数目为NA
④常温常压下,6.72 L NO2与水充分反应转移的电子数目为0.2NA
⑤标准状况下,2.24L氯气溶于水发生反应,转移的电子数目为0.1NA
⑥10g46%的乙醇水溶液中所含氢原子数目为0.6NA
⑦60 g石英晶体中含有的Si﹣O键数目为2NA
⑧25℃时,100mlpH=13的Ba(OH)2溶液中OH﹣的数目为0.02NA
①0.1molH3PO4 ②10.6g碳酸钠 ③标况下11.2L 氦气(气) ④4℃时的9mLH2O
-
(1) Ⅰ.实验室配制490mL0.3mol/L的NaOH溶液
需称量NaOH固体g
-
(2) 在该溶液的配制过程中,用到的玻璃仪器:量筒、烧杯、玻璃棒。
-
(3) 如果在定容时仰视,溶液浓度将;(填“偏大”“偏小”“不影响” )
-
(4) Ⅱ、取上述实验中配制的NaOH溶液200mL,缓慢通入一定量的CO2 , 充分反应,测最后溶液的pH>7。在上述所得溶液中,逐滴缓慢滴加一定浓度的盐酸,所得气体的体积与所加盐酸的体积(不考虑溶解于水)关系如图所示:
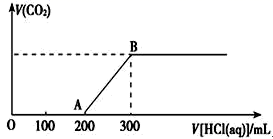
加入盐酸200mL之前,无气体产生,写出OA段发生反应的离子方程式。
-
(5) A点时,反应所得溶液中溶质的成分有
-
(6) 产生的CO2在标准状况下的体积为mL。
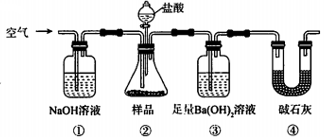
下列说法错误的是( )
-
(1) 制备CuCl2·2H2O晶体:
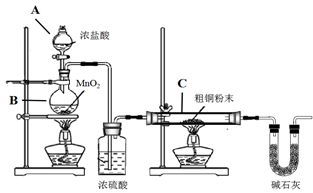
① B装置中发生反应的化学方程式是
② 装置C中粗铜粉末(含杂质Fe)与气体充分反应时的生成物是
③ 反应完成后,将C中的固体用稀盐酸完全溶解,再调节pH值除杂,经一系列操作便可获得CuCl2·2H2O晶体。溶解C中生成物固体时,有时会加入少量双氧水,目的是
-
(2) 制取CuCl,为了制取CuCl采用如图所示装置进行实验(夹持仪器略):
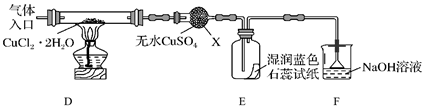
已知:
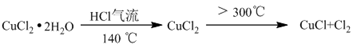
④仪器X的名称是
⑤实验操作的先后顺序是a→→e(填操作的编号)。
a.检查装置的气密性后加入药品 b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
⑥装置F中NaOH溶液的作用是。
⑦ 反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质。请分析产生CuCl2杂质的原因是
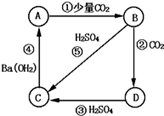
则这四种物质分别为(填化学式):
A、B、C、D。
有关反应的离子方程式:
①;
②;
③。

-
(1) 在标准状况下,6.72 L CO2质量为g,其中含有氧原子数目为。
-
(2) 在标准状况下,3.4 g氨气所占的体积约为L,它与同条件下mol H2S含有相同的氢原子数。
-
(3) V L Fe2(SO4)3溶液中含有a g SO
 ,取此溶液0.5 VL,用水稀释至2 VL,则稀释后溶液中SO
,取此溶液0.5 VL,用水稀释至2 VL,则稀释后溶液中SO  的物质的量浓度为。
的物质的量浓度为。
-
(4) 下列数量的各物质,所含原子个数由大到小的顺序是(填序号)。
①0.5 mol SO3 ②标准状况下22.4 L He
③4℃时9 mL水(水的密度为1 g/mL) ④0.2 mol CH3COONH4
-
(5) 现有下列九种物质:①HCl气体 ②Cu ③C2H5OH ④CO2 ⑤CuSO4·5H2O ⑥小苏打 ⑦Ba(OH)2溶液 ⑧熔融Na2SO4 ⑨NH3·H2O
属于电解质的是;属于非电解质的是;所给状态能导电的电解质是(填所给物质的序号)。

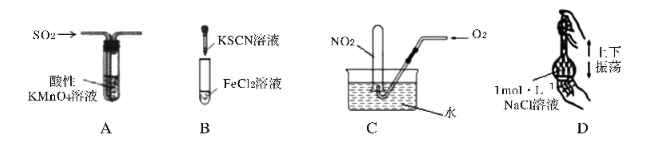
 溶液的颜色变浅,说明
溶液的颜色变浅,说明  具有漂白性
B . 溶液变为血红色,说明
具有漂白性
B . 溶液变为血红色,说明  已完全变质
C . 试管中充满溶液,说明通入氧气的体积为
已完全变质
C . 试管中充满溶液,说明通入氧气的体积为  体积的
体积的 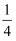 D . 上下振荡容量瓶,能使配制的NaCl溶液混合均匀
D . 上下振荡容量瓶,能使配制的NaCl溶液混合均匀
 的说法正确的是( )
的说法正确的是( )
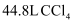 中含有共价键数目为
中含有共价键数目为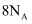 B .
B . 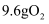 和
和 的混合气体中含有的电子数为
的混合气体中含有的电子数为 C . 足量的铜与含
C . 足量的铜与含 的浓硫酸充分反应,生成
的浓硫酸充分反应,生成 的数目为
的数目为 D .
D . 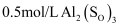 溶液中所含
溶液中所含 数目为
数目为
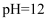 的NaClO溶液中由水电离出的
的NaClO溶液中由水电离出的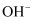 的数目为0.01NA
C .
的数目为0.01NA
C .  和
和 中,中子数均为3.2NA
D . 常温常压下,
中,中子数均为3.2NA
D . 常温常压下,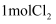 通入过量
通入过量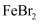 溶液中反应,转移电子数目为2NA
溶液中反应,转移电子数目为2NA
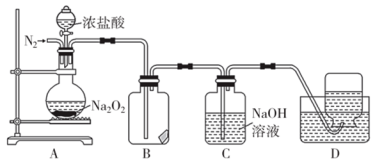
实验步骤及现象如下:
①检查装置气密性后,装入药品并连接装置A、B、C。
②缓慢通入一定量的N2后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,A中剧烈反应,有黄绿色气体产生。
③待装置D中导管口产生连续气泡后,将导管末端伸入集气瓶中,收集到无色气体。
④反应一段时间后,停止滴加浓盐酸,再通一段时间N2 , 直至装置中气体变为无色。
-
(1) 装置D中收集的无色气体X能使带火星的木条复燃,据此推断该气体X是。
-
(2) 装置B中湿润的淀粉碘化钾试纸变蓝。
甲同学根据A中气体的颜色推测试纸变蓝时发生反应的离子方程式为;
乙同学认为使试纸变蓝的原因也可能是(填序号)。
a.挥发的HCl气体使试纸变蓝
b.在此实验过程中生成的X气体也能将I-氧化为I2
c.通入的N2使试纸变蓝
-
(3) C中NaOH溶液的作用是。
-
(4) Na2O2与干燥的HCl能发生化学反应生成Cl2、NaCl和H2O,该反应的化学方程式为,当反应生成标准状况下2.24L Cl2时,转移的电子数为mol。
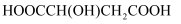 。下列说法错误的是( )
。下列说法错误的是( )
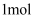 苹果酸与足量金属钠反应,能生成标准状况下氢气
苹果酸与足量金属钠反应,能生成标准状况下氢气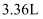 C . 苹果酸在一定条件下能与
C . 苹果酸在一定条件下能与 和
和 发生酯化反应
D . 苹果酸的分子式为
发生酯化反应
D . 苹果酸的分子式为
 为阿伏加德罗常数的值。下列说法正确的是( )
为阿伏加德罗常数的值。下列说法正确的是( )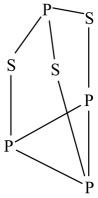
 制备
制备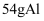 时,产生气体的分子数为3
时,产生气体的分子数为3 B .
B . 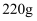 三硫化四磷(
三硫化四磷(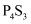 , 如图所示)中含有的极性键的数目为6
, 如图所示)中含有的极性键的数目为6 C . 标准状况下,22.4L氯气与足量烧碱溶液反应,转移的电子数为2
C . 标准状况下,22.4L氯气与足量烧碱溶液反应,转移的电子数为2 D .
D . 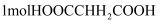 与足量乙醇在一定条件下反应,生成的酯基的数目为2
与足量乙醇在一定条件下反应,生成的酯基的数目为2
- 顺丁橡胶、制备醇酸树脂的原料M以及杀菌剂N的合成路线如下:(M) (1)CH2=CH—CH=CH2的名称是
- 如图是绿色植物体内几项生理活动关系示意图,下列能正确描述其过程的是 ( ) A.能量A是光
- 1971年11月,美国《时代》周刊以“The Chinese Are Coming(中国人来了)”作为封面标题,表明心中
- Question: My 14-year-old son is very disrespectful to my hus
- 人们的生产活动如围湖造田、开垦草原等,其结果是 A.降低了生态系统的自我调节能力
- 在北京市地铁价格调整方案听证会上,各方代表经过激烈的讨论,最终24名听证会代表全部赞成对地铁票价进行调整。这一听证会的召
- 2009年10月29日中国成功研制出千万亿次的超级计算机__,使中国成为继美国之后世界上第二个能够研制出千万亿次超级计算
- 在空间四边形ABCD中,E、F、G、H分别是AB、BC、CD、DA上的点,当BD平行于平面EFGH时,下面结论正确的是(
- 右图是温度和压强对X+Y2Z反应影响的示意图。图中横坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是A、上述可逆反应
- 读江苏和宁夏两省区水资源利用情况对照表,联系所学知识,回答下列各题。省(自治区) 人均 用水量 (m3/人 年) 人均
- (本小题满分12分) 某食品企业一个月内被消费者投诉的次数用表示,椐统计,随机变量的概率分布如下:0123p0.1
- 实验室常采用分解H2O2的水溶液(MnO2作催化剂)的方法制取氧气。 (1) 写出用分解H2O2的水溶液(MnO2作催化
- 国内某企业家说:“我觉得我们企业家要负起自己的责任。我们最应该做的事情就是把自己的企业做好,为社会提供更好的产品和服务。
- 在国际贸易领域中,发达国家工业制成品的出口价格通常高于其价值,发展中国家的初级产品的出口价格则低于其价值。产生这种价格“
- 一个足球运动员用100N的力踢一个重为5N的足球,球离脚后在水平草地上向前滚动了30m.在球滚动的过程中,运动员对足球做
- They used to nod to each other when they met, and now and th
- (2011浙江省嘉兴,9,4分)一个纸环链,纸环按红黄绿蓝紫的顺序重复排列,截去其中的一部分,剩下部分如图所示,则被截去
- 有人说:“对于西方的挑战,中国的反应之所以迟钝,是由于中国社会在19世纪中叶面临很不寻常的历史环境。内部事务万分火急,至
- 下列各组词语中加点字的注音,完全正确的一组是( ) A.锃亮(zènɡ) 拓片(tuò) 同仇敌忾
- 国际文化交流中心将组织一次由各国学生参加的“和平、友谊”夏令营活动,要求报名者提交英文个人简历。假设你是王珊,请根据下列



