第1章 认识化学科学 知识点题库
 数目为0.1NA
C . 1 mol K2Cr2O7被还原为Cr3+转移的电子数为6NA
D . 48 g正丁烷和10 g异丁烷的混合物中共价键数目为13NA
数目为0.1NA
C . 1 mol K2Cr2O7被还原为Cr3+转移的电子数为6NA
D . 48 g正丁烷和10 g异丁烷的混合物中共价键数目为13NA
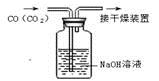 B . 苯萃取碘水中的I2分出水层后的操作
B . 苯萃取碘水中的I2分出水层后的操作 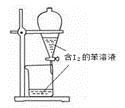 C . 配制0.10 mol·L-1NaOH溶液
C . 配制0.10 mol·L-1NaOH溶液 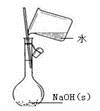 D . 记录滴定终点读数为12.20mL
D . 记录滴定终点读数为12.20mL 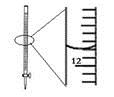
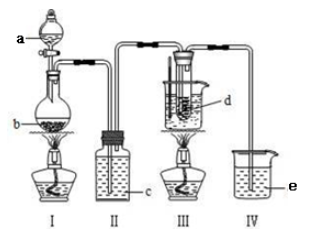
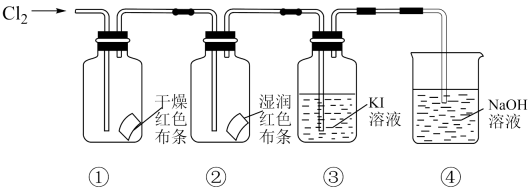
a为浓盐酸,b为MnO2 , c为饱和食盐水, d为30%KOH溶液,e为NaOH溶液
回答下列问题:
-
(1) 检查装置气密性后,添加药品,待装置III水温升至75℃开始反应。
①装置I中反应的离子方程式为。
②若取消装置II,对本实验的影响是。
③实验结束,拆解装置I前为了防止大量氯气逸出,可采取的措施是。
④从装置III的试管中分离得到KClO3粗产品,其中混有的杂质是KClO和。
-
(2) 为测定产品KClO3的纯度,进行如下实验:
步骤1:取2.45g样品溶于水配成250mL溶液。
步骤2:取25.00mL溶液于锥形瓶中,调至pH=10, 滴加足量H2O2溶液充分振荡以除尽ClO-。然后煮沸溶液1~2分钟,冷却。
步骤3:加入过量KI溶液,再逐滴加入足量稀硫酸。(ClO3-+6I-+6H+=Cl-+3I2+3H2O)
步骤4:加入指示剂,用0.5000mol/LNa2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。 (2S2O32-+I2=S4O62-+2I-)
①步骤2中除去ClO-的离子方程式是。“煮沸”的目的是。
②比较碱性条件下氧化性ClO3-ClO- (填写“>”或“<”)。
③样品中KClO3的貭量分数为。(答案保留三位有效数字, KClO3式量:122.5)
①标准状况下,1L HCl和1L H2O的物质的量相同
②标准状况下,11.2L H2和14g N2所含原子数相同
③28g CO的体积约为22.4L
④两种物质的物质的量相同,则它们在标准状况下的体积相同
⑤同温同体积时,气体物质的物质的量越大,则压强越大
⑥同温同压下,气体的密度与气体的相对分子质量成正比
-
(1) 浓盐酸在反应中表现出来的性质是(填写编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
-
(2) 氧化剂与还原剂物质的量之比为,若产生0.1molCl2 , 则转移电子的物质的量为mol。
A.NaHCO3 B.Na2CO3 C.Fe2O3 D.Ca(ClO)2 E. KAl(SO4)2·12H2O
-
(1) 俗称铁红的物质;
-
(2) 漂白粉的有效成分;
-
(3) 一种常见净水剂;
-
(4) 常用于焙制糕点的小苏打;
-
(5) 制普通玻璃的原料是石英、石灰石和。
 增大
增大
-
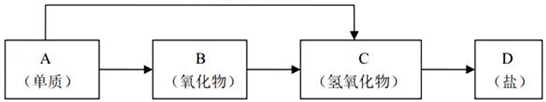
(1) 若B为呼吸面具中的供氧剂,其供氧时每生成1molO2 , 反应过程中转移的电子数为,A与水反应的离子方程式为:。
-
(2) 200℃时,11.6g CO2和H2O的混合物气体与足量的B反应,反应后固体增加了3.6g,则原混合物的平均相对分子质量为。
-
(3) 写出一种“C→D”转化的离子方程式:。
-
(4) 某同学将一小块A单质露置于空气中,观察到下列现象:
银白色
 变灰暗
变灰暗  变白色
变白色  出现液滴
出现液滴  白色固体
白色固体则下列说法正确的是_____________________。
A . ①发生了氧化还原反应 B . ①变灰暗色是因为生成了过氧化钠 C . ③是碳酸钠吸收空气中的水蒸气形成了溶液 D . ④只发生物理变化
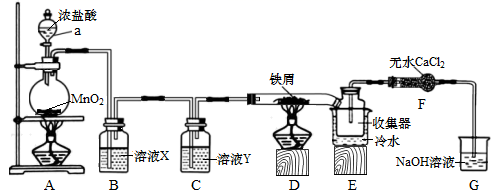
回答下列问题:
-
(1) 仪器a的名称是,装置A发生反应的化学方程式为。
-
(2) 溶液X、Y依次是、;装置D发生反应的化学方程式为。
-
(3) 实验结束时,应先熄灭(填“A”或“D”)处酒精灯;E中冷水的作用是。
-
(4) 装置F的作用是;装置G发生反应的离子方程式。
①  与
与  都能和水反应生成碱,它们都是碱性氧化物
都能和水反应生成碱,它们都是碱性氧化物
②  与
与  发生化合反应生成
发生化合反应生成  ,
, 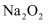 与
与  发生置换反应生成
发生置换反应生成 
③  是淡黄色物质,
是淡黄色物质, 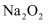 是白色物质
是白色物质
④ 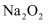 可作供氧剂,而
可作供氧剂,而  不可
不可
⑤ 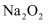 和
和  的焰色均为黄色
的焰色均为黄色

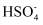 的摩尔质量为97
B . 第I阶段的反应中NO2被氧化
C . HNO2、NO2、H2O均为电解质
D . 第II、III阶段总反应的化学方程式为
的摩尔质量为97
B . 第I阶段的反应中NO2被氧化
C . HNO2、NO2、H2O均为电解质
D . 第II、III阶段总反应的化学方程式为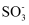 +H2O+NO2=HNO2+
+H2O+NO2=HNO2+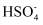
- 下面是关于麦克斯韦电磁场理论的四句话,其中正确的是() A.均匀变化的电场将产生均匀变化的磁场,均匀变化的磁场将产生均匀
- 设“●”“▲”“■”表示三种不同的物体,现用天平称了两次,情况如图所示,那么“■”“▲”“●”这三种物体按质量从大到小的
- 英、法这两个昔日战场上并肩作战的盟友却在巴黎和会上怒目相对,甚至以退出和会相要挟,两国的矛盾焦点是( ) A.
- 下列化学用语表示正确的是 A.氯化钙的化学式 CaCl B.HCl分子的电子式 C.乙烯的结构简式
- 中国食品产业网2007年10月25日报道:阿根廷的潘帕斯草原成为世界大牧场放牧业的典范,今年前半年,阿根廷的牛肉产量增长
- 看图填空(每空2分,共10分)如图是桃花的结构图,请据图完成问题:(1) 图中①④⑤构成_____________,②③
- 华雪同学想制作“叶脉书签”,需要50 g质量分数为10%的氢氧化钠溶液。请回答下列问题: (1)若用氢氧化钠固体配制,需
- 23. You must arrange a _____ time and place for our alumna g
- 如图所示,质量m=50 g、长为L=10 cm的铜棒用长度亦为L的两根轻软导线水平悬吊在竖直向上的匀强磁场中,磁感应强度
- 已知: 某企业合成高效、低毒农药杀灭菊酯的路线如下: (1)写出下列物质的结构简式: C______________
- 实现人生价值,就是要做大事,要做轰轰烈烈、惊天动地的大事。 判断: 理由:
- (本小题满分10分)选修4-5:不等式选讲 设函数。 (1)若解不等式; (2)如果,,求 的取值范围。
- 下列实验中能达到实验目的是() A. 用装置氧化废液中的溴化氢 B. 量取100.00mL溶液 C. 将萃取液中的苯与碘
- (2009年大连质检)在美国的一次大风暴后,有人搜集了136只受伤的麻雀,把它们饲养起来,结果活下来72只,死去64只。
- 2012年“世界水日”的主题是“水与粮食安全”。下列说法错误的是( ) A.水的天然循环能实现水的从新分配
- 下图是同一种动物体内有关细胞分裂的一组图象,下列说法中正确的是 ( )A、动物睾丸中可能同时出现①~⑤
- 读图,完成问题。该区域地貌特征形成的主要原因是
- 下图为我国三个流域水灾受灾比(受水灾的县域个数与总县域个数的比值)多年平均的月变化图,读图回答1—3题1.三个流域水灾受
- — _______ will he arrive here? —In an hour. A. How long
- 100℃时,将0.1 mol N2O4置于1 L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕



