第1章 认识化学科学 知识点题库
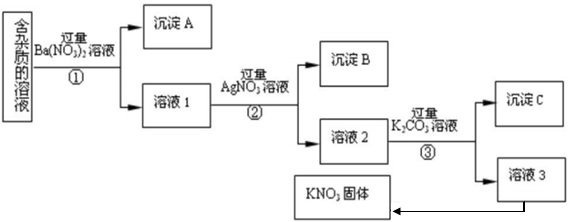
注:KNO3固体容易受热分解
-
(1) 沉淀A的主要成分是、(填化学式);
-
(2) 为了除去溶液3中的杂质,可以向其中加入适量的;除杂后从溶液3获得KNO3晶体的操作是、、过滤;
-
(3) 步骤③加入过量K2CO3溶液的目的是;
-
(4) 实验室用上述实验获得的KNO3体配制450mL0.40 mol/L KNO3溶液,需称取KNO3固体的质量是g;
-
(5) 下列操作会导致所配溶液浓度偏大的是(___________)A . 使用了生锈的砝码 B . 定容时仰视刻度线 C . 容量瓶使用前用蒸馏水洗净但没有干燥 D . 固体溶解后未冷却到室温就转移到容量瓶中
-
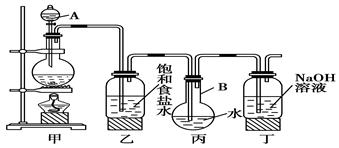
(1) 写出仪器的名称:A。
-
(2) 写出丙、丁装置中发生反应的离子方程式:丙,丁。
-
(3) 有同学提出如下改进建议:
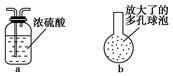
①在乙和丙之间增加上图中的a装置,你认为有无必要 (填“有”或“无”)。
②在丙的长导管下口处,接上图中的b装置,可以提高氯气的吸收效果。原因是。
-
(4) 用制得的氯水分别进行下列实验:①滴入碳酸钠溶液中,有气体生成,说明氯水中发生反应的粒子是;②滴入AgNO3溶液中,发生反应的离子方程式是。
-
(5) 用滴管将制得的饱和氯水慢慢滴入含酚酞的NaOH稀溶液中。当滴到最后一滴时红色突然退去。产生上述现象的原因可能有两种(简要文字说明):①是由于;②是由于。
 离子,测得Na+、Fe3+、Cl- 离子的物质的量浓度分别为0.4mol/L、0.2mol/L、0.6mol/L,则SO
离子,测得Na+、Fe3+、Cl- 离子的物质的量浓度分别为0.4mol/L、0.2mol/L、0.6mol/L,则SO  的物质的量浓度为( )
的物质的量浓度为( )
|
选项 |
陈述Ⅰ |
陈述Ⅱ |
判断 |
|
A |
碳酸钠溶液可用于治疗胃病 |
Na2CO3可与盐酸反应 |
Ⅰ对,Ⅱ对,有 |
|
B |
向Na2O2的水溶液中滴入酚酞变红色 |
Na2O2与水反应生成氢氧化钠 |
Ⅰ对,Ⅱ错,无 |
|
C |
金属钠保存在煤油中,以隔绝空气 |
常温下,金属钠在空气中会生成过氧化钠 |
Ⅰ对,Ⅱ对,有 |
|
D |
过氧化钠可用于航天员的供氧剂 |
Na2O2能和CO2、H2O反应生成O2 |
Ⅰ对,Ⅱ对,有 |
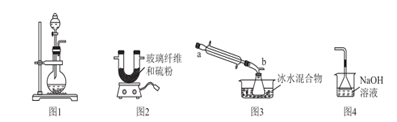
 等杂质)为原料制备。实验室提纯NaCl的流程如图:
等杂质)为原料制备。实验室提纯NaCl的流程如图: 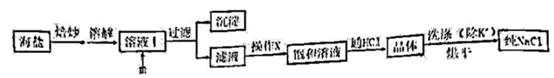
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳
-
(1) 欲除去溶液I中的Ca2+、Mg2+、Fe3+、
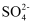 ,在提供的试剂中,选出m所代表的试剂,按滴加顺序依次为、NaOH、(只填化学式);洗涤除去NaCl晶体表面附带的少量KCl,在提供的试剂中,选用的试剂为。
,在提供的试剂中,选出m所代表的试剂,按滴加顺序依次为、NaOH、(只填化学式);洗涤除去NaCl晶体表面附带的少量KCl,在提供的试剂中,选用的试剂为。
-
(2) 操作X为用提纯的NaCl配制500mL 4.00mol/L NaCl溶液,所用的玻璃仪器除烧杯、玻璃棒外还有(填仪器名称)
-
(3) 用如图所示装置,以焙炒后的海盐为原料制备HCl气体,并通入NaCl饱和溶液中使NaCl结晶析出。
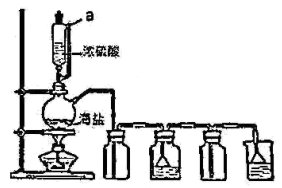
①用浓硫酸和海盐混合加热制取氯化氢利用了浓硫酸的性质是(填编号),相比分液漏斗,选用仪器a的优点是。
a.高沸点 b.强酸性 c.强氧化性
②对比实验发现,将烧瓶中的海盐磨细可加快NaCl晶体的析出,其原因是。
-
(4) 设计实验测定NaCl产品中SO
 的含量,填写表格。
的含量,填写表格。 操作
目的/结论
①
称取样品
 ,加水溶解,加盐酸调至弱酸性,滴加过量c1mol/LBaCl2溶液V1mL
,加水溶解,加盐酸调至弱酸性,滴加过量c1mol/LBaCl2溶液V1mL目的:。
②
过滤洗涤,干燥后称得沉淀为m2g
结论:样品中SO
 的质量分数为。(列算式)
的质量分数为。(列算式)
-
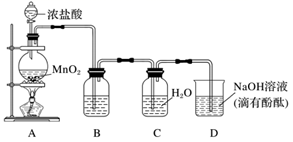
(1) Cl2有毒,实验前一定要检查装置的气密性。用文字表述检查这套装置气密性良好的方法及现象:。
-
(2) 装置B中所盛试剂是。
-
(3) 装置D用于吸收多余的氯气,其中所盛试剂能否换成氢氧化钙?并说明理由:。
-
(4) 同学们观察到装置D中红色褪去,并对褪色原因提出假设:
①ClO-破坏了酚酞的结构;
②。
该小组同学设计实验,取少许装置D中褪色后的溶液于试管中,请将后续操作和现象补充完整),证实了假设②不能成立。
-
(5) 取装置C中所得溶液,观察到溶液呈浅黄绿色,用pH计测量,读数为1.52。
①以上信息中可以证明氯气分子与水发生了化学反应的是,能说明反应是有一定限度的。测量pH时不能用pH试纸代替pH计,原因是。
②已知:Cl2(g)+H2O(l)
 H+(aq)+Cl-(aq)+HClO(aq) △H>0,该小组同学进一步探究氯气与水反应的可逆性:向20 mL饱和氯水中滴加1 mL浓硫酸,利用化学型传感器测量氯化物的含量随时间变化的关系(如图所示),从而判断溶液中Cl-的含量。
H+(aq)+Cl-(aq)+HClO(aq) △H>0,该小组同学进一步探究氯气与水反应的可逆性:向20 mL饱和氯水中滴加1 mL浓硫酸,利用化学型传感器测量氯化物的含量随时间变化的关系(如图所示),从而判断溶液中Cl-的含量。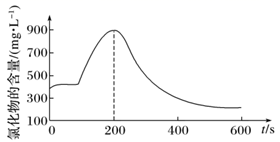
200s前,氯化物的含量突然增大的原因可能是;用平衡移动原理分析在200s后,氯化物的含量随时间减小的原因。
A.用量筒量取5.4mL浓硫酸,缓缓注入盛有约50mL蒸馏水的烧杯里,并用玻璃棒搅拌
B.用约30mL蒸馏水,分成三次洗涤烧杯和玻璃棒,将每次洗涤液都倒入容量瓶里
C.将稀释后的稀硫酸小心地用玻璃棒引流入容量瓶
D.检查100mL容量瓶口部是否发生滴漏
E.将蒸馏水直接加入容量瓶,至液面接近环形刻度线1~2cm处
F.盖紧瓶塞,反复倾倒振荡,摇匀溶液
G.用胶头滴管向容量瓶里逐滴滴入蒸馏水,至液面最低点恰好和环形刻度线相切
请回答下列问题:
-
(1) 正确的操作顺序是(填标号)。
-
(2) 进行A步操作时,应选用下列量器中的(填标号)。
①10mL量筒 ②50mL量筒 ③500mL量筒 ④1000mL量筒
-
(3) 如果对装有浓硫酸的量筒仰视读数为5.4mL,配制的稀硫酸的浓度将(填“偏高”“偏低”或“无影响”)。
-
(4) 进行A步操作时,必须后,才能进行后面的操作。
-
(5) 配制上述溶液时,下列操作会导致所配溶液的浓度偏高的是(填标号)。
a.洗涤烧杯和玻璃棒的溶液未转移入容量瓶中
b.定容时,眼睛俯视使溶液凹面最低点与容量瓶刻度线相切
c.容量瓶中原残留有少量蒸馏水
d.定容后加水过量,又从容量瓶中取出部分溶液,使液面降至刻度线
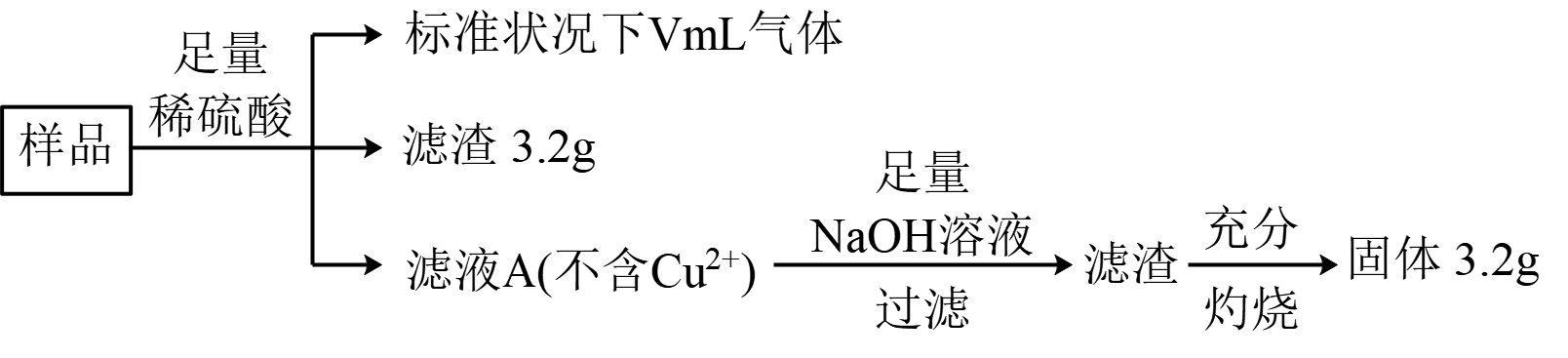
下列说法不正确的是( )
 离子中含有的质子数为NA
C . 常温常压下1molMgCl2中含Cl-数为2NA
D . 常温常压下11.2L甲烷中含有的氢原子数为2NA
离子中含有的质子数为NA
C . 常温常压下1molMgCl2中含Cl-数为2NA
D . 常温常压下11.2L甲烷中含有的氢原子数为2NA
- 某无色溶液能使紫色石蕊溶液变蓝色,则该溶液能使无色酚酞溶液A .变蓝色B .不变色C .变紫色D .变红色
- (04年全国卷Ⅰ)若以表示水的摩尔质量,v表示在标准状态下水蒸气的摩尔体积,为在标准状态下水蒸气的密度,NA为阿伏加德罗
- 火车的车厢后面有两间厕所,只有当两间厕所的门都关上时(每扇门的插销相当于一个开关),车厢中的指示牌内的指示灯才会发光,指
- 如果下图表示中国、德国、日本、美国四国工业扩散示意图,结合所学知识回答1—2题。 1.图中A、B、C
- 哲学家柏拉图说:“受过良好音乐教育的人可以敏捷地看出艺术作品和自然界事务的丑陋,很正确的加以厌恶。但一看到美的东西,他就
- 目前,我国的立法重点由制定新法转到修订旧法、抓紧配套方面。2012年国务院计划完成“商标法修订草案”等33项法律的起草、
- 阿伏加德罗常数的值约为6.02×1023mol-1,下列叙述中不正确的是( )①12.4g白磷晶体中含有的P-P
- 一金属铝的易拉罐内充满CO2,然后往罐内注入足量的NaOH溶液,立即用胶布封罐口。经过一段时间后,罐壁内凹而瘪。再过一段
- 某高三毕业班有人,同学之间两两彼此给对方仅写一条毕业留言,那么全班共写了 条毕业留言.(用数字作答)
- 已知豌豆的红花对白花为显性,一个豌豆品种代代只开白花,在种植这种白花豌豆的农田中,出现了一株红花豌豆,将这红花豌豆种下,
- The Eng lish story is very easy for me.There are_____new wor
- (1)中学教材中图示了NaCl晶体,它向三维空间延伸得到完美晶体。NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最
- 已知随机变量的分布律如右图,其中成等差数列,如果,则的值等于 ) A. B.
- Post LoginRegister Support Sourcingassistant needed Posted O
- 材料一: 我国部分行业发展情况 钢铁 水泥 汽车 纺织 服装 2003年投资增长 96.6% 121.9% 87.2%
- 一个长方形的长与宽分别时6cm、5cm,它的对角线的长可能是( ) A、整数 B、分数
- 中国古代专制主义中央集权达到顶峰的标志是( )。 A.秦朝创皇帝制 B.元朝实行行省制C.明朝
- Do you want to do well in exams? Sometimes your knowledge is
- W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可
- 从4,5,6,7,8这5个数中任取两个数,则所取两个数之积能被3整除概率是() A. B.



