第1章 认识化学科学 知识点题库
实验室模拟工业漂白液(有效成分为NaClO)脱除废水中氨氮(NH3)的流程如下:
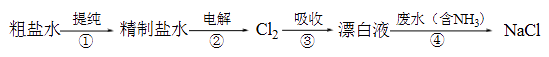
下列分析正确的是( )
A . ①中采用蒸馏的方法精制粗盐水
B . ②中阳极的主要电极反应:4OH- - 4e- = 2H2O + O2↑
C . ③中制备漂白液的反应:Cl2 + OH- = Cl- + HClO
D . ②、③、④中均发生了氧化还原反应
向如图所示装置中缓慢通入气体X,若打开活塞K,则品红溶液褪色;若关闭活塞K,则品红溶液无变化而澄清石灰水变浑浊。X和Y可能是( )
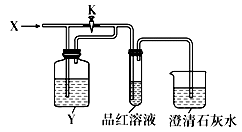
选项 | A | B | C | D |
X | SO2 | Cl2 | HCl | Cl2 |
Y | NaOH溶液 | 饱和NaHCO3溶液 | 饱和NaCl溶液 | Na2SO3溶液 |
A . A
B . B
C . C
D . D
实验室中需要配制2mol·L-1NaOH的溶液430mL,配制时应选用的容量瓶的规格和称取NaOH的质量分别是( )
A . 500mL,40g
B . 500mL,34.4g
C . 430mL,34.4g
D . 430mL,40g
向80mL浓硫酸中加入56g铜片,加热一段时间后,至不再反应为止,计算:
-
(1) 实验测得反应中共有13.44L标准状况下的SO2生成,被还原的硫酸的物质的量为mol,反应中转移的电子有mol。
-
(2) 将反应后的混合物加水稀释到100mL并除去不溶物,加入足量锌粉放出标准状况下5.376L氢气,则原浓硫酸的物质的量浓度为,反应的Zn的质量为。
据报道美国准备试验绿色航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,结构如图,它比肼燃烧释放能量更高,更安全、环保。下列说法错误的是( )
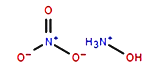
A . 羟基硝酸铵中各原子共平面
B . 固态时羟基硝酸铵是离子晶体
C . 羟基硝酸铵中含有离子键和共价键
D . 9.6g羟基硝酸铵中含有0.2NA个离子
下列哪些因素不是影响气体体积的主要因素( )
A . 温度
B . 压强
C . 微粒的大小
D . 微粒的数目
化学知识可以帮助解决日常生活中遇到的许多问题,下列说法错误的是( )
A . 胃酸过多的病人,可以服用碳酸氢钠来中和胃酸
B . 明矾有吸附性,可用于自来水的杀菌消毒
C . 溴化银见光易分解,是一种重要的感光材料,是胶卷中必不可少的成分
D . Na2O2吸收CO2产生O2 ,可用作呼吸面具供氧剂
设NA为阿伏加德罗常数的值,下列叙述错误的是( )
A . 1L0.2mol/L亚硫酸钠溶液中H2SO3、HSO3−、SO32−的总数为0.2NA
B . 常温常压下,1mol C2H4和1mol CH4所含的氢原子数均为4NA
C . 向含1 mol FeI2的溶液中通入等物质的量的Cl2 , 转移的电子数为2NA
D . 1mol白磷(P4)分子中所含化学键的数目为4NA
下列说法正确的是( )
A . 少用添加剂比多用添加剂安全
B . 天然添加剂比人工合成添加剂安全
C . 往奶粉中添加三聚氰胺(化学式为C3H6N6)是违法的
D . 不用防腐剂处理的食品比用防腐剂处理的食品安全
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
A . 常温常压下,11.2 L氧气所含的分子数为NA
B . 1.8 g 的NH4+中含有的电子数为1.1NA
C . 22 g二氧化碳与标准状况下11.2 L H2含有相同的原子数
D . 2.3 g金属钠与O2完全反应,转移电子的物质的量为0.1 mol
战国所著《周礼》中记载沿海古人“煤饼烧蛎房成灰”(“蛎房”即牡蛎壳),并把这种灰称为“蜃”。蔡伦改进的造纸术,第一步沤浸树皮脱胶的碱液可用“蜃”溶于水制得。“蜃”的主要成分是( )
A . CaO
B . SiO2
C . Al2O3
D . Ca(OH)2
等体积硫酸铝、硫酸锌、硫酸钠溶液分别与足量的氯化钡溶液反应。若生成的硫酸钡沉淀的质量比为1:2:3,则三种硫酸盐溶液的物质的量浓度比为( )
A . 1:2:3
B . 1:6:9
C . 1:3:3
D . 1:3:6
将8.7 g MnO2粉末与含14.6 g HCl的浓盐酸共热完全反应后,生成氯气的体积(标准状况)为(不考虑盐酸的挥发)( )
A . 等于4.48 L
B . 等于2.24 L
C . 在2.24 L~4.48 L之间
D . 小于2.24 L
如图是制取氯化铁粉末所需的装置,已知氯化铁粉末容易吸水生成结晶化合物:FeCl3+6H2O=FeCl3·6H2O。请回答下列问题。
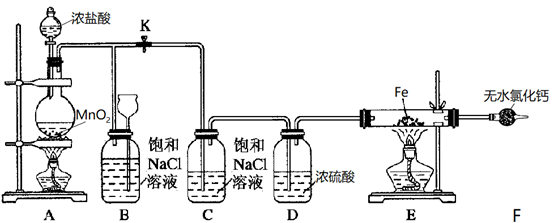
-
(1) 写出烧瓶A发生反应的化学方程式为,该反应中氧化剂是 (填物质名称);浓盐酸的作用是。
-
(2) 写出E中发生反应的化学方程式为。
-
(3) C的作用是;D的作用是。
-
(4) 应先点燃(填“A”或“E”)处的酒精灯,理由是。
-
(5) 这套实验装置是否完整?(填“是”或“否”)。若不完整,还须补充 (若第一空填“是”,则此空不需要作答)装置。
-
(6) E处反应完毕后,关闭弹簧夹K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是,此时B的作用是。
合成氨工业生产中所用的αFe催化剂的主要成为FeO、Fe2O3。
-
(1) 某FeO、Fe2O3混合物中,铁、氧的物质的量之比4∶5,其中Fe2+与Fe3+物质的量之比为。
-
(2) 当催化剂中Fe2+与Fe3+的物质的量之比为1∶2时,其催化剂活性最高,此时混合物中铁的质量分数为(保留2位小数)。
-
(3) 写出由C(炭粉)与Fe2O3在高温下反应制备α铁触媒的化学方程式(另一种产物可溶于水)。
-
(4) 为制得这种活性最高的催化剂,理论上应向480 g Fe2O3粉末加入炭粉的质量为,生成实验条件下CO2的体积为(假设此实验条件下,气体摩尔体积为24 L·mol-1)。
设 NA 为阿伏加德罗常数值。下列有关叙述正确的是( )
A . 6g 4He含有的中子数为1.5 NA
B . 标准状况下,22.4L 苯中含有的碳碳双键数为3 NA
C . 60g由乙酸和葡萄糖组成的混合物中含有氢原子的数目为4 NA
D . 密闭容器中,1molN2与4molH2充分反应生成的NH3分子数为2 NA
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 将4.6g 钠用铝箔包裹并刺小孔,与足量水充分反应生成H2分子数为0.1 NA
B . 标准状况下,22.4L 己烷中含有的共价键的数目为19NA
C . 标准状况下,11.2L 12C18O中含有的中子数为8NA
D . 标准状况下,7.1 gCl2通入足量石灰水中反应转移的电子数为0.2NA
将适量的金属钠投入下列物质的溶液中,有气体放出,但无沉淀生成的是( )
A . BaCl2溶液
B . 饱和Ca(OH)2溶液
C . FeCl3溶液
D . MgCl2溶液
下列说法符合化学史实的是( )
A . 门捷列夫将元素按质子数由小到大依次排列得到了第一张元素周期表
B . 舍勒发现了一种黄绿色气体,并命名它为氯气
C . 汤姆孙发现了电子,并提出了电子云模型
D . 侯德榜创立的“侯氏制碱法”缩短了生产流程,降低了制碱的成本
钠元素在自然界都以化合物的形式存在。
-
(1) 过氧化钠中氧元素的化合价为价,焰色试验为色。
-
(2) 过氧化钠用于呼吸面具的反应方程式为,,若有2mol的过氧化钠参与反应,转移的电子的物质的量为mol。
最近更新
- 下列关于细胞分裂、分化、衰老和凋亡的叙述,正确的是() A. 细胞分化使各种细胞的遗传物质有所差异,导致细
- 已知三棱柱ABC—A1B1C1,底面是边长为的正三角形,侧棱垂直于底面,且该三棱柱的外接球的体积为,则该三棱柱的体积为
- 20.在下面一段文字横线处补写恰当的语句,使整段文字语意完整连贯,内容贴切,逻辑严密。每处不超过15个字。(6分) 在科
- 14.读图11,回答问题.(1)图示区域内居民点分布有何特点?其形成的原因是什么? (2)图示区域内有众多的干涸河道和古
- 某校高三学生W参加X区人大代表选举,社区领导告知一定要选本社区的现任领导。W将此事反映给上级人大部门得到解决。这一事件涉
- (坐标系与参数方程选做题) 圆锥曲线 (t为参数)的焦点坐标是 .
- 同一平面内的三个力,大小分别为4N、6N、7N,若三力同时作用于某一物体,则该物体所受三力合力的最大值和最小值分别为
- 10月8日,比利时和英国两位物理学家获得2013年诺贝尔物理学奖。此奖以表彰他们描述了粒子物理学的标准模型,及成功预测希
- 下图事件的出现,表现了无产阶级的革命首创精神,这里的“首创”主要是指( )
- 下列关于流通中所需要的货币量的叙述,正确的选项是 ①与商品价格总额成正比 ②与商品价格总额成反比 ③与货币流通速度成反
- 某处控型食品保鲜剂以淀粉、二氧化硅(SiO2)为载体,吸附酒精制作而成,保鲜原理是酒精缓缓挥发,在食品周围形成一定浓度的
- 设集合A={|一1<<4,且∈N},B={|<1},则AB= A.{|0<<2}
- 直接导致唐朝灭亡的原因是 ( ) A.土地高度集中 B.唐末农民战争
- 标点符号使用正确的一句是 ( ) A.避讳之风可谓源远流长,“其俗起于周,成于秦,盛于唐宋,其历史垂二千年”(陈
- Chen Yuhang doesn’t know why, but every yearwhen Spring Fest
- Gao Ping really stand them. A.doesn't
- 下图是一件青铜矛,1997年出土于广东清远一座春秋墓葬,上面刻有两个繁体“门”形纹饰。从这一考古发现可知( )
- 一种+3价的金属氧化物A,在B气流中高温下生成固体物质C和气体D,D能使澄清石灰水变浑浊。若将C投入稀硫酸中,产生气体E
- 如图,在平面直角坐标系中,抛物线y=经过平移得到抛物线y=,其对称轴与两段抛物线所围成的阴影部分的面积为()A.2
- 纯铁的熔点为1535℃,而在高炉中炼铁时,生铁(含铁量较高铁的合金)在1200℃左右就熔化了,这是因为A.铁的纯度越高熔



