第一节 铁及其化合物 知识点题库
把Fe和Fe2O3组成的某混合物放入250mL2.0mol·L-1的HNO3溶液中,充分反应后,生成的NO气体在标准状况下的体积为1.12L,再向反应后的溶液中加入1.0mol·L-1的NaOH溶液,要使铁元素完全沉淀下来,所加入的NaOH溶液的体积最少是( )
A . 400mL
B . 450mL
C . 500mL
D . 550mL
制印刷电路时常用FeCl3溶液作为“腐蚀液”,发生的反应为:2 FeCl3 + Cu = 2FeCl2 + CuCl2 ;向盛有FeCl3溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是( )
A . 有 Cu无Fe
B . 有Fe无Cu
C . Fe、Cu都有
D . Fe、Cu都无
将铁屑溶于过量的稀盐酸后,再加入下列物质,会有Fe3+生成的是( )
A . 溴水
B . 硫酸锌
C . 硝酸钠
D . 氯化铜
向10.4g Fe3O4、Fe2O3、Cu的混合物中加入1mol•L﹣1的硫酸溶液140mL时,固体恰好完全溶解,所得溶液中不含Fe3+ , 若用过量的H2在高温下还原相同质量的原混合物,固体减少的质量为( )
A . 1.12g
B . 2.24g
C . 3.24g
D . 6.42g
下列说法正确的是( )
A . 绿色食品是不含任何化学物质的食品
B . 灼烧某物质时,用眼直接观察到火焰呈黄色,则可判断该物质不含钾元素
C . 向新制的FeSO4溶液中滴入适量的NaOH溶液,放置片刻,整个反应过程的颜色变化是:浅绿色溶液→白色沉淀→灰绿色沉淀→红褐色沉淀
D . 称取等质量的两份铝粉,分别加入过量的稀盐酸和过量的NaOH溶液,则放出氢气的体积(同温同压下)不相等
硫酸亚铁铵[(NH4)2Fe(SO4)2]是一种重要的化工原料,下列有关说法正确的是( )
A . Na+、Fe3+、NO3﹣、Cl2都可在该物质的溶液中大量共存
B . 向0.1mo1/L该物质的溶液中清加0.1mo1/LNaOH溶液,生成沉淀的物质的量与逐滴加入NaOH溶液体积关系如图所示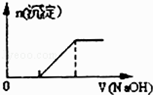 C . 检验该物质中Fe2+是否变质的方法是向该物质的溶液中滴入几滴KSCN溶液,观察溶液是否变红色
D . 向该物质的溶液中摘加Ba(OH)2溶液,恰好使SO42﹣完全沉淀的离子方程式为:Fe2++2SO42﹣+3Ba2++2OH﹣═2BaSO4↓+Fe(OH)2↓
C . 检验该物质中Fe2+是否变质的方法是向该物质的溶液中滴入几滴KSCN溶液,观察溶液是否变红色
D . 向该物质的溶液中摘加Ba(OH)2溶液,恰好使SO42﹣完全沉淀的离子方程式为:Fe2++2SO42﹣+3Ba2++2OH﹣═2BaSO4↓+Fe(OH)2↓
 C . 检验该物质中Fe2+是否变质的方法是向该物质的溶液中滴入几滴KSCN溶液,观察溶液是否变红色
D . 向该物质的溶液中摘加Ba(OH)2溶液,恰好使SO42﹣完全沉淀的离子方程式为:Fe2++2SO42﹣+3Ba2++2OH﹣═2BaSO4↓+Fe(OH)2↓
C . 检验该物质中Fe2+是否变质的方法是向该物质的溶液中滴入几滴KSCN溶液,观察溶液是否变红色
D . 向该物质的溶液中摘加Ba(OH)2溶液,恰好使SO42﹣完全沉淀的离子方程式为:Fe2++2SO42﹣+3Ba2++2OH﹣═2BaSO4↓+Fe(OH)2↓
如表各组物质中,不能按a→b→c关系相互转化的是(“→”表示一步完成)( )
选项 | a | b | c |
A | Fe | FeCl3 | FeCl2 |
B | Na | Na2O2 | NaOH |
C | Si | SiO2 | H2SiO3 |
D | HNO3 | NO | NO2 |
A . A
B . B
C . C
D . D
某校化学兴趣小组为探究铁与浓硫酸反应,设计了图1、图2所示装置进行实验.
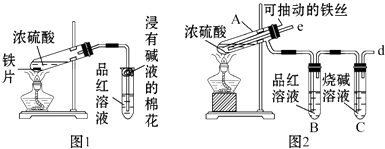
-
(1) 比较两实验装置,图2所示装置的优点是
①能更好地吸收有毒气体SO2 , 防止其污染环境;
② .
-
(2) 能说明有SO2气体产生的实验现象是
-
(3) 反应一段时间后,用滴管吸取A试管中的溶液滴入适量水中为试样,试样中所含金属离子的成分有以下三种可能:
Ⅰ:只含有Fe3+;Ⅱ:只含有Fe2+;Ⅲ:既有Fe3+又有Fe2+ .
为验证Ⅱ、Ⅲ的可能性,选用如下试剂:
A.稀盐酸 B.稀硫酸 C.KSCN溶液D.KMnO4溶液 E.NaOH溶液 F.淀粉KI溶液G.H2O2溶液
验证Ⅱ:取试样,先滴加少量的(填试剂序号,下同),振荡,再滴加少量的,根据溶液颜色的变化可确定假设Ⅱ是否正确.
验证Ⅲ:步骤1.取试样,滴加少量的(填试剂序号),溶液的颜色,则试样中含有Fe3+ , 发生反应的离子方程式为.
步骤2.再取适量的试样滴加少量的(填试剂序号),溶液的颜色变为色,则试样中含有Fe2+ .
下列有关铁及其化合物的说法中正确的是( )
A . 赤铁矿的主要成分是Fe3O4
B . 铁与水蒸气在高温下的反应产物为Fe2O3和H2
C . 除去FeCl2溶液中的FeCl3杂质可以向溶液中加入铁粉,然后过滤
D . Fe3+与KSCN产生血红色沉淀
高三一年的化学复习,学生要抓住两方面,一方面是教材,另一方面是历年的高考真题。每年的高考题,在教材中几乎都能找到影子,所以同学们一定要紧紧抓住教材,根据《必修一》第三章和第四章的内容回答下列问题:
-
(1) 实验3-1是取用钠单质的实验,用品有小刀,、、培养皿。
-
(2) 铁是人类应用最广泛,铁的氧化物有三种,其中Fe3O4是一种具有的黑色晶体,俗称磁性氧化铁.Fe2O3的用途(举一例)。
-
(3) 氢氧化铝其有两性,写出氢氧化铝分别溶于强酸和强碱的离子方程式 。
-
(4) 在抗震救灾中要用到大量漂白粉和漂白液杀菌消毒,漂白粉的制取过程如下:通过煅烧石灰石得到生石灰,生石灰溶于水得石灰乳,在向石灰乳中通入氯气反应得漂白粉,有关的反应化学方程式为:CaCO3
 CaO+CO2↑、。
CaO+CO2↑、。
通过所学知识,回答下面问题
-
(1) 写出铁与水蒸气在高温下反应方程式。
-
(2) 加热碳酸氢钠的化学方程式为
-
(3) 在呼吸面具中,Na2O2起反应的化学方程式为。当有7.8克Na2O2反应时,放出氧气的质量为。
-
(4) 将铜片投入到FeCl3溶液中恰好完全反应,发生的反应离子方程式为。
-
(5) 向FeSO4溶液中滴加NaOH溶液时,生成的白色絮状沉淀迅速变成灰绿色,最后变成红褐色。写出此变化过程的化学方程式: 。
碳酸锰(MnCO3)是制造电信器材软磁铁氧体的重要原料。工业上以软锰矿(主要成分为MnO2 , 含少量Fe2O3、Al2O3、SiO2、CuS等)与含SO2的烟气为主要原料制备碳酸锰(MnCO3),其工艺流程如下:
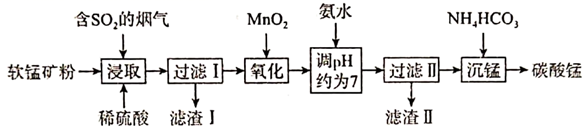
已知:①酸性条件下MnO2与CuS反应生成淡黄色沉淀;
②部分阳离子沉淀时溶液的pH。
|
离子 |
Al3+ |
Fe3+ |
Fe2+ |
Mn2+ |
Cu2+ |
|
开始沉淀的pH |
4.1 |
2.2 |
5.8 |
8.8 |
4.2 |
|
沉淀完全的pH |
4.7 |
3.2 |
8.8 |
10.1 |
6.7 |
请回答下列问题:
-
(1) 滤渣Ⅰ的主要成分是(填物质名称)。
-
(2) “氧化”步骤中,加入MnO2氧化的离子是,检验该离子被完全氧化的方法是。
-
(3) 加入氨水调节溶液的pH约为7,其目的是。
-
(4) “沉锰”步骤中,加入NH4HCO3时反应的离子方程式为。
-
(5) 碳酸锰纯度的测定:称量18.00 g碳酸锰样品(杂质不参加反应),溶于过量的稀硫酸中,向所得溶液中加入稍过量的磷酸和硝酸,加热发生反应:2Mn2++NO3-+4PO43-+2H+
 2[Mn(PO4)2]3-+NO2-+H2O。除去溶液中的NO3-和NO2- , 加入100.00 mL 2.00 mol/L的(NH4)2Fe(SO4)2溶液,发生反应[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2 PO43-;再用1.00 mol/L酸性K2Cr2O7溶液氧化过量的Fe2+ , Fe2+反应完全时消耗10.00 mL酸性K2Cr2O7溶液。则碳酸锰样品纯度为%。(保留三位有效数字)。
2[Mn(PO4)2]3-+NO2-+H2O。除去溶液中的NO3-和NO2- , 加入100.00 mL 2.00 mol/L的(NH4)2Fe(SO4)2溶液,发生反应[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2 PO43-;再用1.00 mol/L酸性K2Cr2O7溶液氧化过量的Fe2+ , Fe2+反应完全时消耗10.00 mL酸性K2Cr2O7溶液。则碳酸锰样品纯度为%。(保留三位有效数字)。
下列有关物质的性质与用途具有对应关系的是 ( )
A . Al2O3具有两性,可用作耐高温材料
B . NaHCO3溶液呈碱性,可用于制备纯碱
C . 铝具有良好导热性,可用作贮运浓硝酸
D . FeCl3溶液具有氧化性,可用作蚀刻铜电路板
现代社会的发展与进步离不开材料,下列有关材料的说法错误的是( )
A . 500米口径球面射电望远镜被誉为“中国天眼”,其“眼眶”是钢铁结成的圈梁,属于新型纯金属材料
B . 用于新版人民币票面文字等处的油墨中所含有的Fe3O4是一种磁性物质
C . 港珠澳大桥路面使用了沥青和混凝土,沥青可以通过石油分馏得到
D . 国庆阅兵仪式上的坦克和军车都喷涂着新式聚氨酯迷彩伪装涂料,能适应多种环境背景下的隐蔽需求,聚氨酯属于有机高分子材料
下列有关铁的化合物的说法错误的是( )
A . 实验室为了暂时妥善保存硫酸亚铁溶液,常加入少量的铁粉
B . 某溶液若加入KSCN溶液,无变化,但通入Cl2后变血红色,说明原溶液中含有Fe2+
C . 欲检验FeSO4溶液是否全部变质,可加入少量酸性高锰酸钾溶液观察紫色是否褪去
D . 将适量铁粉放入FeCl3溶液中完全反应后,溶液中Fe2+和Fe3+的浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比为1:1
FeSO4在工业上可用于制备FeCO3 , 实验室模拟工业流程如图所示。下列说法正确的是( )
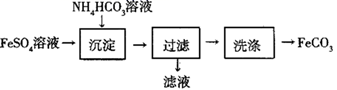
A . 可用KSCN溶液检验FeSO4溶液中Fe2+是否全部被氧化成Fe3+
B . 用Na2CO3代替NH4HCO3 , 可能有Fe(OH)2沉淀产生
C . 沉淀的同时有NH3产生
D . 检验沉淀是否洗涤干净,可用盐酸检验
三氯化铁溶液可腐蚀印刷电路板上的铜膜,腐蚀废液会污染环境.某小组为了从腐蚀废液(含有大量CuCl2、FeCl2和FeCl3)中回收铜,并将铁的化合物全部转化为腐蚀液原料循环使用,其流程如下:
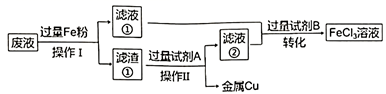
回答下列问题:
-
(1) 操作Ⅰ的名称.
-
(2) 滤渣①中的成分(用化学式表示).
-
(3) 若选用Cl2作试剂B,则“转化”过程中发生反应的离子方程式为;若从“绿色化学”的角度来考虑,试剂B可以是.
-
(4) 取少量滤液②于试管中加入NaOH溶液,生成了白色絮状沉淀后迅速变成灰绿色,过一段时间会生成红褐色物质,请写出生成红褐色物质时发生的化学反应方程式.
-
(5) 把1.0mol/L CuCl2溶液和2.0mol/L FeCl3溶液等体积混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入过量铁粉,经过足够长的时间后,铁粉有剩余.此时溶液中Fe2+的物质的量浓度是.
铁是人类较早使用的金属之一,运用所学知识,回答下列问题。
电子工业常用30%FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
-
(1) 写出FeCl3溶液与金属铜发生反应的离子方程。
-
(2) 某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:

请写出上述过程中滤渣③中所含成分的化学式,物质⑥的化学式。
下列化学方程式,不能表达其变化的是( )
A . 氢氟酸刻蚀玻璃: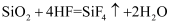 B . Fe(OH)2的白色沉淀在空气中久置:
B . Fe(OH)2的白色沉淀在空气中久置: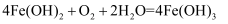 C . Na2O2用于呼吸面具:
C . Na2O2用于呼吸面具: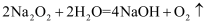
 D . 将SO2通入漂白粉溶液:
D . 将SO2通入漂白粉溶液:
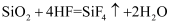 B . Fe(OH)2的白色沉淀在空气中久置:
B . Fe(OH)2的白色沉淀在空气中久置: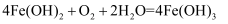 C . Na2O2用于呼吸面具:
C . Na2O2用于呼吸面具: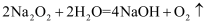
 D . 将SO2通入漂白粉溶液:
D . 将SO2通入漂白粉溶液:
下列说法正确的是( )
A . 铜与碘反应易生成碘化铜
B . 明矾水解时产生具有吸附性的胶体粒子,可以用于饮用水的杀菌消毒
C . 氨氮废水(含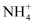 及
及 )可用化学氧化法或电化学氧化法处理
D . 向氯化亚铁溶液中加入
)可用化学氧化法或电化学氧化法处理
D . 向氯化亚铁溶液中加入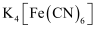 生成蓝色沉淀
生成蓝色沉淀
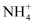 及
及 )可用化学氧化法或电化学氧化法处理
D . 向氯化亚铁溶液中加入
)可用化学氧化法或电化学氧化法处理
D . 向氯化亚铁溶液中加入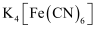 生成蓝色沉淀
生成蓝色沉淀
最近更新
- 下面为过M点(128°E,48°N)沿经线和纬线作相同长度的地形剖面示意图,读图回答若①、②为同一山脉,则该山脉的走向大
- 一辆摩托车能达到的最大速度为vm=30 m/s,要想在3 min内由静止起沿一条平直公路追上在前面s0=1 000 m处
- 财政部宣布自2011年起央企上缴红利的比例将上调5%,其中,石化、烟草、电力等15家垄断国企的上缴比例提高至15%。对此
- 用“等值算法”(更相减损之术),求下列两数的最大公约数.(1)225,135;(2)98,280.
- 下列试剂的贮存方法错误的是
- .如图,AB是⊙O的切线,B为切点,AO的延长线交⊙O于C点,连接BC,如果∠A=30°,AB=2,那么AC的长等于.
- 关于x的二次方程x2+(m-1)x+1=0在区间[0,2]上有解,求实数m的取值范围.
- 《兵车行》反映了频繁征兵开边给百姓带来的深重灾难,“君不闻 , , ”的诗句写出了田园荒芜的
- 硫蒸气中常含S2分子,常温下硫则常以S8的形式存在,下列说法正确的是() A.相同物质的量的S2与S8分别与足量O2燃烧
- 近年来,重金属污染土壤导致的严重危害环境和健康的事件时有发生。面对我国土壤污染的现状,有专家呼吁:我国针对土壤污染应该专
- 自来水厂常用氯气消毒杀菌,化学方程式为Cl2+H2O=HCl+HClO.而HCl、HClO在水中会解离出H+、Cl﹣和C
- 把大小两种草履虫放在一起培养,它们会争夺食物,其中一种会死亡。这两种生物之间的关系是 A.捕食 B
- Our bus drove ____ the Great Hall of the People. A. across
- 化学与生产、生活、社会密切相关。下列有关说法中,错误的是( ) A.今夏,台州地区出现了严重的旱情,缓解旱情的措施之
- 2009年8月15日起,公安部将在全国范围内严厉整治“酒后驾驶行为”。在为期两个月的专项行动中,对酒后驾驶行为,一律按《
- 读下图(2010年4月下旬我国部分地区农业气象灾害分布图),据此回答下面试题。有关甲乙两区域气象灾害的叙述正确的是
- 根据汉语意思完成句子。(10分)1、--- 你怎么了? --- 我背疼。--- What’s the matte
- 请以“架一座心灵之桥”为题,写一篇不少于800字的作文。 要求:①角度自选;②立意自定;③除诗歌外,文体自选。
- 如图所示,固定在水平绝缘平面上足够长的金属导轨不计电阻,但表面粗糙,导轨左端连接一个电阻R,质量为m的金属棒(电阻也不计
- 某无色溶液中含有K+、Cl-、OH-、SO2-3、SO2-4,为检验溶液中所含有的各阴离子,限用的试剂有:盐酸、硝酸、硝



