第一节 铁及其化合物 知识点题库
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | Fe3+有氧化性 | 实验室常用KSCN溶液检验Fe3+ |
B | SO2有较强的还原性 | SO2可使酸性KMnO4溶液褪色 |
C | Mg有还原性 | 电解MgCl2饱和溶液可制备Mg |
D | 浓H2SO4有吸水性 | 浓H2SO4可用于干燥氨气 |
 FeCl3
FeCl3 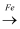 FeCl2
B . Cu
FeCl2
B . Cu 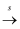 CuS
CuS  CuCl2
C . CO2
CuCl2
C . CO2 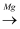 C
C  CO
D . NO2
CO
D . NO2  NO
NO 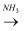 N2
N2
①NaAlO2(aq)  Al(OH)3
Al(OH)3  Al2O3(熔融)
Al2O3(熔融)  Al
Al  Fe
Fe
②S  SO3
SO3  H2SO4
H2SO4
③Cu(OH)2CO3  CuCl2(aq)
CuCl2(aq)  Cu
Cu
④Fe2O3  FeCl3
FeCl3  无水FeCl3
无水FeCl3
⑤饱和NaCl(aq) 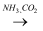 NaHCO3
NaHCO3  Na2CO3 .
Na2CO3 .
 Fe2O3+SO2↑+SO3↑,利用下图所示装置检验硫酸亚铁的分解产物(乙、丙、丁中的试剂是足量的)。下列说法中错误的是( )
Fe2O3+SO2↑+SO3↑,利用下图所示装置检验硫酸亚铁的分解产物(乙、丙、丁中的试剂是足量的)。下列说法中错误的是( ) 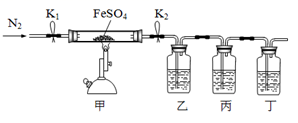
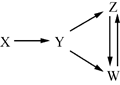
| 选项 | X | Y | Z | W |
| A | Al | Al2O3 | NaAlO2 | Al(OH)3 |
| B | Fe3O4 | Fe | FeCl2 | FeCl3 |
| C | H2SO4 | SO2 | S | SO3 |
| D | N2 | NH3 | NO | NO2 |
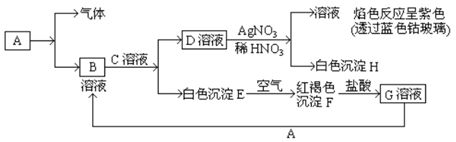
请回答下列问题:
-
(1) 写出B的化学式,D的化学式为;
-
(2) 写出由E转变成F的化学方程式。
-
(3) 写出D转化成H的离子方程式。
-
(4) 除去溶液B中混有的少量G溶液的最适宜方法是。
 制备还原铁粉的工业流程如下:
制备还原铁粉的工业流程如下: 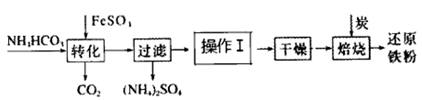
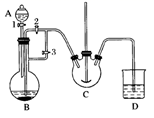
实验室中可用 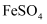 (用铁粉和稀硫酸反应制得)和
(用铁粉和稀硫酸反应制得)和 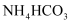 在如图装置模拟上述流程中的“转化”环节.
在如图装置模拟上述流程中的“转化”环节.
-
(1) 装置A的名称是,装置B中盛放的药品是,
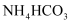 盛放在装置中.
盛放在装置中.
-
(2) 实验过程中,欲将生成的
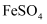 溶液和
溶液和 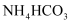 溶液混合,操作方法是.
溶液混合,操作方法是. 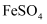 溶液要现用现配制的原因是.
溶液要现用现配制的原因是.
-
(3) 操作I的名称是,干燥过程的主要目的是脱去游离水,该过程中会有少量
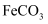 在空气中被氧化为
在空气中被氧化为 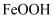 ,取干燥后的
,取干燥后的 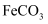 样品
样品 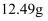 ,与炭混合后焙烧,最终得到还原铁粉
,与炭混合后焙烧,最终得到还原铁粉 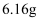 ,计算样品中杂质
,计算样品中杂质 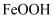 的质量g
的质量g
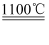 Fe3O4↑+2H2↑+4Na”生产金属钠。下列说法正确的是( )
Fe3O4↑+2H2↑+4Na”生产金属钠。下列说法正确的是( )
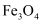 B . 用磁铁可以将Fe与
B . 用磁铁可以将Fe与 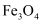 分离
C . 将生成的气体在空气中冷却可获得钠
D . 每生成1molH2 , 该反应转移的电子数约为
分离
C . 将生成的气体在空气中冷却可获得钠
D . 每生成1molH2 , 该反应转移的电子数约为 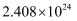
-
(1) (实验1)制备银镜:
i.配制银氨溶液,需要的试剂是。并取等量银氨溶液于多支试管中。
ii.向银氨溶液中加入等量的葡萄糖溶液,水浴加热。产生银镜,洗净,备用。 -
(2) (实验2)溶解银镜:分别向两支试管中加入5mLFe(NO3)3、Fe2(SO4)3溶液。
选用Fe2(SO4)3溶液的浓度为0.05mol/L,目的是保证相等。编号 a b 试剂 0.1mol/LFe(NO3)3 0.05mol/LFe2(SO4)3 现象 银镜消失较快; 溶液黄色略变浅; 产生少许白色沉淀 银镜消失较慢; 溶液黄色明显变浅; 产生较多白色沉淀 -
(3) 从a、b中均检出了Fe2+ , 说明Fe3+具有氧化性。a中Fe3+氧化Ag的离子方程式是。
-
(4) 确认b中沉淀为Ag2SO4(微溶),检验Ag2SO4固体中
 的方法是。
的方法是。
-
(5) 推测在a中的酸性条件下
 氧化了银,证据是。通过如下实验验证了推测是合理的:
氧化了银,证据是。通过如下实验验证了推测是合理的:
i.测pH:测定实验a中所用Fe(NO3)3溶液的pH=2;
ii.配制溶液:。取5mL此溶液加入有银镜的试管,现象是。
请将步骤ii补充完整。
-
(6) 分析a中白色沉淀的成分,提出假设。
假设1:Fe(OH)2;假设2:AgNO2;假设3:…
①设计实验方案验证假设1:取少量沉淀置于空气中,未变色。假设1不成立。
②设计实验方案验证假设2(已知:亚硝酸盐能与酸化的KI溶液反应)。
实验方案
预期现象和结论
(实验结论与讨论)铁盐能蚀刻银;
 能提高铁盐的蚀刻能力。推测硝酸铁溶液如果保持足够的酸性,可以避免产生沉淀。
能提高铁盐的蚀刻能力。推测硝酸铁溶液如果保持足够的酸性,可以避免产生沉淀。
| 选项 | 化学反应及其离子方程式 | 评价 |
| A | Fe3O4与过量稀硝酸反应:Fe3O4+8H+=2Fe3++Fe2++4H2O | 正确 |
| B | NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO | 正确 |
| C | 在稀氨水中通入过量CO2:NH3·H2O+CO2=NH | 正确 |
| D | FeBr2溶液与等物质的量的Cl2反应:2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2 | 错误,Fe2+与Br-的化学计量数之比应为1:2 |
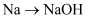 B .
B . 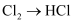 C .
C . 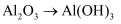 D .
D . 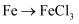
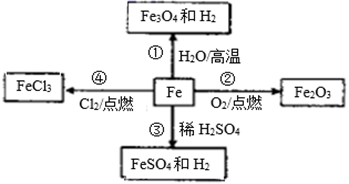
① ②
②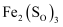 ③
③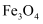 ④
④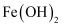 ⑤
⑤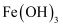 ⑥
⑥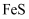
-
(1) I.A,B,C,D是中学化学的常见物质。已知:①A为黄绿色气体,B为金属单质;②A与B化合生成C,C的水溶液遇KSCN溶液呈红色;③D是第三周期的金属单质,能与盐酸、氢氧化钠溶液反应产生氢气,请回答:
C的化学式为; -
(2) 写出D与氢氧化钠溶液反应的化学方程式是;
-
(3) B与C的水溶液反应的离子方程式为。
-
(4) A可用于制取漂白粉,漂白粉的有效成分是(填化学式)。
-
(5) Ⅱ.海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验(苯,一种不溶于水,密度比水小的液体):
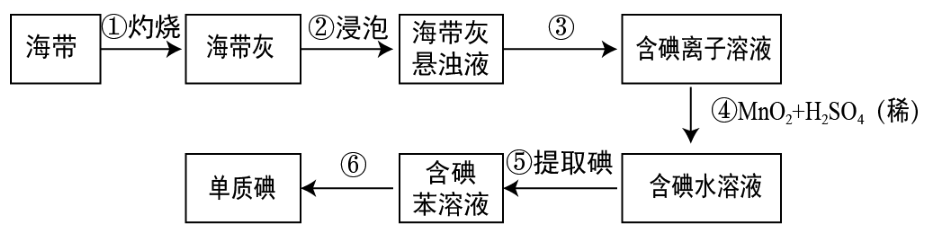
请填写下列空白:
步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是____(从下列仪器中选出所需的仪器,用标号字母填写在空自处)。
A . 烧杯 B . 坩埚 C . 表面皿 D . 泥三角 E . 酒精灯 F . 干燥器 -
(6) 步骤③的实验操作名称是。
-
(7) 步骤④中还可以用
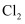 , 请写出
, 请写出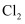 氧化
氧化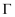 的离子方程式:。
的离子方程式:。
-
(8) 检验水溶液中是否含有单质碘可以用溶液。
- 东南亚大部分地区属于( ) A.热带季风气候和热带雨林气候 B.热带草原气候和热带沙
- 如图,在边长为1的小正方形组成的网格中,的三个顶点均在格点上, 请按要求完成下列各题: (1) 用签字笔画AD
- 如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线。现有t2℃时甲、 乙、丙三种物质的饱和溶液(无固体存在)。 下列说
- 已知正三棱柱ABC—A1B1C1中,A1B⊥CB1,则A1B与AC1 所成的角为 (A)450
- 为了验证胚芽鞘尖端确实能产生促进生长的某种物质,用胚芽鞘和琼脂块等材料进行实验时,对照实验的设计思路是
- 光线沿直线2x-y-3=0经两坐标轴反射后所在的直线是 A.2x+y+3=
- 已知一批基因型为AA和Aa的豌豆种子,其数目之比为1∶2,将这批种子种下,自然状态下(假设结实率相同)其子一代中基因型为
- 已知函数f(x)=x–2. (1)求函数f(x)=x–2的定义域,值域,并指出其奇偶性,并作出其大致图象(不描点); (
- 设奇函数在上是增函数,且,则不等式的解集为 A. B. C.
- 研究发现,在细胞有丝分裂间期,染色体复制并不是同步进行的,即有的先完成复制,有的后完成复制。下图中能准确反映有丝分裂间期
- A、B、C三种醇同足量的金属钠完全反应,在相同条件下产生相同体积的氢气,消耗这三种醇的物质的量之比为3∶6∶2,则A、B
- (湖南卷文18)如图所示,四棱锥的底面是边长为1的菱形,,E是CD的中点,PA底面ABCD,。 (I)证明:平面PBE平
- 《物权法》明确规定:“国家在社会主义初级阶段,坚持公有制为主体、多种所有制经济共同发展的基本经济制度。……国家巩固和发展
- 阅读下面的文言文,完成下列各题题。 杨 烈 妇 传 唐·李 翱 建中四年,李希烈①陷忭州。既又将盗陈州,分其兵数千人抵项
- 如图为动植物细胞亚显微结构模式图,下列有关该图的叙述正确的是()A.所有植物细胞都不具有的结构是[A] B.胰岛B细胞合
- It's not only rocket scientists and journalists who are foll
- 下列叙述中,错误的是() A.甲苯与溴蒸气在光照条件下反应主要生成邻溴甲苯和对溴甲苯 B.苯在合适条件下催化加氢可生成环
- 10.古诗文默写(6分,每句1分) (1)《逍遥游》中以“朝菌”和“蟪蛄”为例来说明“小年”的句子是:
- (2012江苏连云港)5.名著阅读题。(6分) (1)小说《格列佛游记》好几次提到中国,请简要列举相关内容。(3分)
- 若向量=(2,3),=(4,6),则=() A.(﹣2,﹣3) B.(2,﹣3) C.(2,3)
 +Ba2++2OH-=BaSO4↓+2H2O
+Ba2++2OH-=BaSO4↓+2H2O +HCO
+HCO 



