第一节 铁及其化合物 知识点题库
①铁能被磁铁吸引,但纯铁易锈蚀 ②在人体的血红蛋白中含有铁元素③铁是地壳中含量最高的金属 ④铁能在氧气中剧烈燃烧,但不能在水蒸气中反应 ⑤能通过化合反应生成FeCl3和Fe(OH)3
-
(1) 加热铁屑与稀硫酸时常常需要补充蒸馏水,原因。
-
(2) 实验中为减少硫酸亚铁的损失,过滤分离硫酸亚铁溶液时应注意的问题是。
-
(3) 为防止Fe2+被氧化,实验中可采取的措施是。
选项 | 现象或事实 | 解释 |
A | 用热的纯碱溶液洗去镀件油污 | Na2CO3可直接和油污反应 |
B | 施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 | K2CO3与NH4Cl反应生成氨气会降低氮肥肥效 |
C | 漂白粉在空气中久置变质 | 漂白粉中的CaCl2 与空气中的CO2反应生成CaCO3 |
D | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含有Cu2+的溶液中置换出铜 |
-
(1) 用FeSO4·7H2O配制FeSO4溶液时,需加入稀H2SO4和。
-
(2) 在过量FeSO4溶液中滴入稀硫酸,再滴入几滴H2O2溶液,溶液立即变黄。上述反应的离子方程式为。
-
(3) 为检验上述反应中的氧化产物,甲同学取少许上述反应后的溶液,加入,出现血红色溶液,证明氧化产物为Fe3+;乙同学取少许上述反应后的溶液,加入溶液,溶液变蓝,证明氧化产物为Fe3+ , 该反应的离子方程式为。
-
(4) 为证明上述反应后的溶液中仍存在过量的Fe2+ , 可向其中滴加溶液。
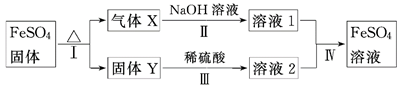
已知:①X由两种化合物组成,将X通入品红溶液,溶液退色;通入BaCl2溶液,产生白色沉淀。②Y是红棕色的化合物。
-
(1) 气体X的成分是(填化学式)。
-
(2) 反应Ⅰ的反应类型属于(填序号)。
a.分解反应b.复分解反应c.置换反应d.化合反应e.氧化还原反应
-
(3) 溶液2中金属阳离子的检验方法是。
-
(4) 若经反应Ⅰ得到16 g固体Y,产生的气体X恰好被0.4 L 1 mol·L-1 NaOH溶液完全吸收,则反应Ⅰ的化学方程式是,
反应Ⅳ中生成FeSO4的离子方程式是。
-
(5) 一瓶长期露置在空气中的FeSO4溶液,为检验其是否完全变质,则需要的试剂是(填写名称)。
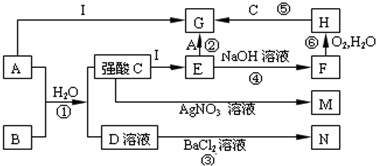
-
(1) 写出①的化学方程式。
-
(2) 写反应②的离子方程式。
-
(3) 写出将A通入石灰乳的化学方程式。
-
(4) 在①→⑥中,属于氧化还原反应的有(填编号)
-
(5) 将NaOH溶液加入到E中的现象为。
-
(6) 写出反应⑥的化学反应方程式。
-
(7) 写出分别将A、B通入石蕊试液中的现象:
AB。
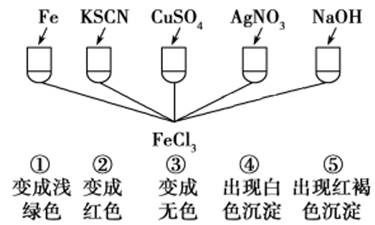
实验 | 结论 | |
A | 中和热的测定实验中,若将环形玻璃搅拌棒换成铜棒 | 测得ΔH偏小 |
B | 中和滴定实验中,锥形瓶用待测液润洗 | 测量结果将偏低 |
C | 向氯化铁溶液中滴入KSCN溶液出现红色沉淀 | Fe3+与SCN-反应生成红色物质 |
D | 25℃,分别向等体积,浓度分别为0.1 mol/L和0.5 mol/L的草酸溶液中滴入少量等量的酸性高锰酸钾,后者褪色快。 | 其它条件相同,草酸的浓度越大,反应速率越快 |
-
(1) I.天宫二号空间实验室己于2016年9月15日22时04分在酒泉卫星发射中心发射成功。请回答下列问题:
耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是(填化学式),该物质的类别属于(填“碱性氧化物”或“酸性氧化物”),实验室中不能用玻璃塞的试剂瓶盛放KOH溶液,原因是(用离子方程式表示)。
-
(2) 太阳能电池帆板是“天宫二号”空间运行的动力。其性能直接影响到“天宫二号”的运行寿命和可靠性。天宫二号使用的光太阳能电池,该电池的核心材料是,其能量转化方式为。
-
(3) II.铝和氢氧化钾都是重要的工业产品。
请回答:
铝与氢氧化钾溶液反应的离子方程式是。
-
(4) 用铝粉和Fe2O3做铝热反应实验,需要的试剂还有(填序号)。
a.KCl b.KClO3 c.MnO2 d.Mg
取少量铝热反应所得到的固体混合物,将其溶于足量稀H2SO4 , 滴加KSCN溶液无明显现象,(填“能”或“不能”)说明固体混合物中无Fe2O3 , 若能,则不用填写理由,若不能,理由是(用离子方程式说明)。
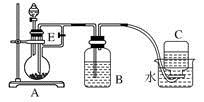
-
(1) B中盛一定量的NaOH溶液,A中应预先加入的试剂是,A中反应的离子方程式是:。
-
(2) 实验开始时就先将活塞E(填“打开”或“关闭”),C中收集到气体的主要成分是。
-
(3) 简述生成Fe(OH)2的操作过程。
-
(4) 拔去装置B中的橡皮塞,使空气进入,写出有关反应的化学方程式:。
 被还原为NO)。下列说法正确的是( )
被还原为NO)。下列说法正确的是( )
-
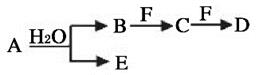
(1) 若A为淡黄色固体,物质A和D的摩尔质量相等,请写出B和F溶液反应生成C的离子方程式:。
-
(2) 若物质A中一种元素原子的最外层电子数为其电子总数的
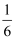 ,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O 反应的化学方程式:。
,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O 反应的化学方程式:。
-
(3) 若常温下A为有色气体,F是一种金属单质。请写出B和适量F反应生成C与气体E的离子方程式:;简述D溶液中的金属阳离子的检验方法。
| 已知事实 | 类推结论 | |
| A | 将Zn加入CuSO溶液中:Zn+Cu2+=Cu+Zn2+ | 将Na加入CuSO4溶液中:2Na+Cu2+=Cu+2Na+ |
| B | 将FeO加入稀盐酸溶液中:FeO+2H+=Fe2++H2O | 将FeO加入稀硝酸溶液中:FeO+2H+=Fe2++H2O |
| C | 电解NaCl冶炼金属钠:2NaCl(熔融) | 电解AlCl3冶炼金属铝:2AlCl3(熔融) |
| D | Cl2与SO2的水溶液反应:Cl2+2H2O+SO2=2HCl+H2SO4 | Br2与SO2的水溶液反应:Br2+2H2O+SO2=2HBr+H2SO4 |
单质 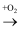 氧化物
氧化物  酸(或碱)
酸(或碱)  盐
盐
 试纸中央,试纸变红后不褪色
B . 向
试纸中央,试纸变红后不褪色
B . 向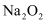 固体中加入适量水,再滴加几滴酚酞,溶液变红后不褪色
C . 向
固体中加入适量水,再滴加几滴酚酞,溶液变红后不褪色
C . 向 溶液中加入
溶液中加入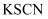 溶液,不变红,滴加少量氯水后溶液变红
D . 向碘的饱和水溶液中加入适量
溶液,不变红,滴加少量氯水后溶液变红
D . 向碘的饱和水溶液中加入适量 , 溶液分层,上层显紫红色
, 溶液分层,上层显紫红色
-
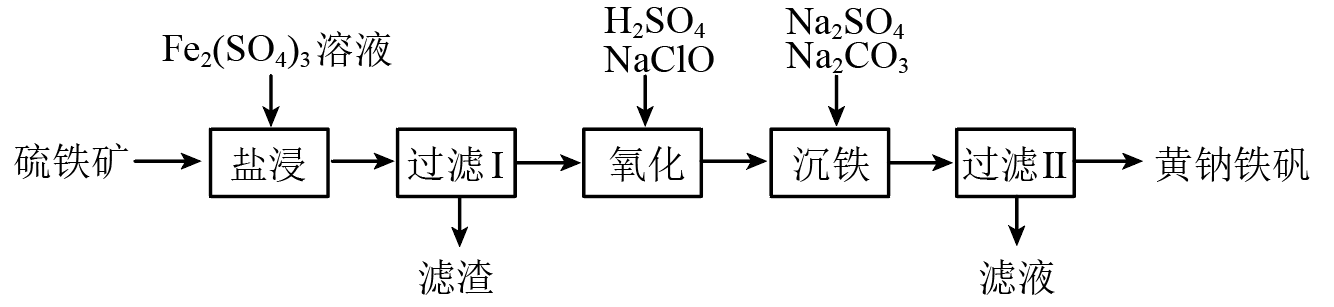
(1) “盐浸”时的反应为FeS2+Fe2(SO4)3→FeSO4+S↓(未配平),其中氧化剂和还原剂的物质的量之比为;滤渣的主要成分为SiO2和。
-
(2) “氧化”时发生反应的离子方程式为;用空气代替NaClO进行该反应具有成本低等优点,但存在的缺点。
-
(3) “沉铁”过程,控制不同条件可以得到不同的沉淀,所得沉淀与温度、pH的关系如图所示(图中阴影部分表示黄钠铁矾稳定产生的区域)。
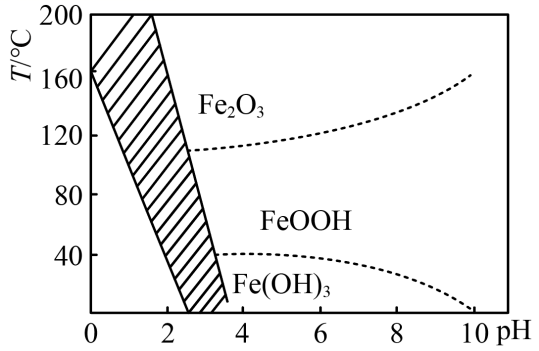
①80℃时,加入碳酸钠偏多时得到的黄钠铁矾中含有的杂质是。
②生成黄钠铁矾的离子反应方程式。
③由图在pH=2时,温度过高或过低,不易制得黄钠铁矾。试解释其原因。
-
(4) 测定黄钠铁矾样品中铁的质量分数:称取样品2.000g置于锥形瓶中,加入足量稀H2SO4溶解,滴入稍过量的KI溶液,待充分反应后,调节溶液近中性,滴入几滴淀粉溶液,用0.1500mol•L-1Na2S2O3溶液平行滴定,平均消耗20.00mL。(已知:I2+2S2O
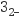 =2I-+S4O
=2I-+S4O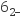 )
)①滴定终点的实验现象是。
②样品中铁的质量分数为。
-
(1) 写出漂白液有效成分的化学式:。
-
(2) 写出FeO在空气中被氧化后产物的化学式:;
-
(3) 写出铁和水蒸气反应的化学方程式:。
- 关于秦岭﹣﹣淮河,下列说法错误的是() A. 与我国1月份0℃等温线分布大致一致 B. 与我国400mm等降水量
- 在实数﹣,,,,0.80108,中,无理数的个数为()A. 1个 B. 2个 C. 3个 D. 4个
- “改善环境质量,推动绿色发展”。下列做法不符合该理念的是 A.生活垃圾分类处理
- 胰岛素的A,B两条肽链是由一个基因编码的。下列有关胰岛素的叙述,正确的是 A.胰岛素基因的两条DNA单链分别编码A,B两
- 用班氏试剂鉴别健康人的下列四种液体,出现红黄色沉淀的是 (
- 阅读下面的宋词,然后回答问题。(6分)如梦令 贺铸 莲叶初生南浦,两岸绿杨飞絮。向晚鲤鱼风①,断送彩帆何处! 凝伫
- 2008年诺贝尔化学奖授予美籍华裔钱永健等三位科学家,以表彰他们发现和研究了绿色荧光蛋白。荧光素是发光物质的基质,5-羧
- 我国动植物资源丰富,农、林、牧、副、渔各业综合发展,其主要原因是A、季风气候显著 B、大陆性气候显著 C、气候复杂
- 已知△ABC的坐标分别为A(1,1)、B(3,2)、C(2,4),(1)写出直线AB的向量方程及其坐标形式.(2)求出A
- 下列句子中标点适用正确的一项是 A、姚明在整个NBA赛季中都会因为这样那样的原因成为关注的目标。这到底是什么原因?是他的
- 在唾液腺细胞中参与合成与分泌唾液淀粉酶的细胞器有( ) A.线粒体、中心体、高尔基体、内质网 B.内质网、
- 主链上有6个碳原子,含有1个甲基和1个乙基两个支链的烷烃有() A.6种
- 金属元素铊的相关信息如右图所示。下列有关卡片信息解读 正确的是( ) A.铊元素的质量数是81
- 观察下图,回答问题:(1) 关节炎是一种常见疾病, 其病变部位应在甲图中[] ____________。 (2) 关
- 春天受潮的衣物、鞋子和食品上容易长出绒毛状的霉,请问这些霉属于下列哪类生物()A. 细菌 B. 乳酸菌 C. 霉菌 D.
- 下列词语中加点的字的注音错误最多的一组是 A.挑剔(tì) 缱绻(quǎn) 压
- 下列消化液中,不含消化酶的是 A.唾液
- 下列语句中加点的成语使用不正确的一项是( )(3分) A.他穷凶极恶,残忍狠毒,已经到了不可救药的地步。。B.皇帝
- 在一密闭容器中进行下列反应:2SO2(g)+O2(g)⇌2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度
- 已知是方程3x﹣ay=8的解,则a=.



