第三节 化学反应中的有关计算 知识点题库
(1)二氧化碳的质量为;
(2)当碳酸钙恰好完全反应时所得溶液中溶质的质量分数.(结果保留一位小数)
-
(1) 请从图1中选择适当的仪器组装实验装置.

①实验室制取二氧化碳,应选择上面仪器中的(填字母代号).
②若用高锰酸钾制取氧气,还需要补充的一种仪器是(填名称),反应的化学方程式为
-
(2) 小明同学采用如图2装置进行趣味实验.
①若 A 中是碳酸氢钠和稀盐酸,B 中是紫色石蕊溶液,
A 中反应的化学方程式为,B 中可观察到的现象为.
②若换一组药品,用所得干燥气体充气球,气球在空中上升,则 A,B 中应分别盛放、(写一组即可).
-
(3) 某同学用过氧化氢溶液和二氧化锰制取氧气,该同学取 50g 过氧化氢溶液和 1g 二氧化锰混合,完全反应后,称量剩余物质的质量为 49.4g.试计算过氧化氢溶液中溶质的质量分数.
-
(1) 常见的酸有硫酸、盐酸等,在它们的水溶液里由于存在相同的(填符号),因此,它们有很多相似的化学性质,如:、
等(写两条即可).
-
(2) 碱有氢氧化钠、氢氧化钙等,氢氧化钠可作某些气体的干燥剂,但不能干燥二氧化碳理由是,氢氧化钙可由生石灰与水反应制得,反应的化学方程式为
-
(3) 酸和碱能发生中和反应,它在日常生活和工农业生产中有广泛的应用,如硫酸厂的污水中含有硫酸等杂质,可用熟石灰进行处理,反应的化学方程式为.
-
(4) 2010年4月14日青海玉树大地震灾害发生后,为了灾区人民群众的饮用水安全,卫生防疫部门要经常对灾区水源进行监测,获得可靠的科学依据.若现有一瓶水样,要获取它的酸碱度,应如何操作:.
-
(5) 某化学兴趣小组经过一段时间的调查与探究,模拟工厂的治污原理,设计了如图所示装置,一方排出含硫酸的废水,另一方排出含氢氧化钠的废水,然后在池中混合,经充分反应后排放.若该工厂一天排出含氢氧化钠10%的废液400吨,需含硫酸9.8%的废水多少吨才能完全中和?

取MgCl2和NaCl的固体混合物10g做如下实验.请根据图中实验及数据进行计算.


-
(1) MgCl2中镁元素和氯元素的质量比为
-
(2) 计算溶液B中NaCl的质量分数(写出计算过程).
-
(3) 要配制与溶液B相同质量分数的NaCl溶液200g,需要质量分数为24.4%的NaCl溶液的质量是多少?(写出计算过程)
 B . 向相同质量与浓度的稀盐酸分别加入足量的铁粉和锌粉
B . 向相同质量与浓度的稀盐酸分别加入足量的铁粉和锌粉 C . 向相同质量的铁粉和锌粉中分别加入足量稀盐酸
C . 向相同质量的铁粉和锌粉中分别加入足量稀盐酸 D . 一氧化碳与一定量氧化铁在高温条件下完全反应
D . 一氧化碳与一定量氧化铁在高温条件下完全反应
(提示:2HCl+Na2CO3= 2NaCl+H2O+CO2↑)
次数 | 第1次 | 第2次 | 第3次 |
加入盐酸的质量/g | 20 | 20 | 20 |
剩余固体的质量/g | 30 | a | 20 |

请计算:
-
(1) 第2次加入盐酸后,a为g;
-
(2) 石灰石样品中碳酸钙的质量分数;(计算结果精确至0.1%)
-
(3) 10%的CaCl2溶液可做路面保湿剂。欲将第5次实验后的溶液配成10%的CaCl2溶液,可先向此溶液中加入足量的石灰石粉末,完全反应后过滤,这时还需要向滤液中加入水多少克?(假设实验过程中溶液损失忽略不计)(计算结果精确至0.1g)

反应时间(s) | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
溶液温度(℃) | 20.5 | 20.6 | 20.7 | 20.8 | 20.9 | 20.8 | 20.7 |
-
(1) 当稀盐酸与氢氧化钠溶液恰好完全反应时,溶液的温度是℃
-
(2) 计算稀盐酸中溶质的质量分数(精确到0.1%)
 为测定某炼铁厂生产的生铁样品中铁的质量分数,化学兴趣小组的同学称得该生铁样品
为测定某炼铁厂生产的生铁样品中铁的质量分数,化学兴趣小组的同学称得该生铁样品  ,放入烧杯中,向其中加入
,放入烧杯中,向其中加入  稀硫酸,恰好完全反应
稀硫酸,恰好完全反应  假设杂质不参与反应
假设杂质不参与反应  测得的实验数据如表:
测得的实验数据如表: | 反应前 | 反应后 | |
| 烧杯及其中物质的质量 | | |
请你完成有关计算  结果保留一位小数
结果保留一位小数 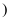 :
:
-
(1) 反应放出的氢气是多少?
-
(2) 生铁样品中铁的质量分数是多少.
| | | | |
| A.向盛有一定量的H2O2溶液的烧杯中加入MnO2 | B.二氧化锰与氯酸钾混合受热 | C.镁带在密闭容器中燃烧 | D.红磷在装有空气的集气瓶中燃烧 |
 Si+2CO↑
Si+2CO↑
-
(1) 二氧化硅中,硅、氧原子个数比为。
-
(2) 生成的Si与CO的质量比为。
-
(3) 若所用砂子中SiO2的的质量分数为60%,则:
①200t砂子中SiO2的质量为t。
②请补全下列计算过程,求出用200t砂子理论上最多能生成的Si的质量。
解:设理论上最多能生成Si的质量为x。

x=(_)t
答:理论上最多能生成Si的质量为 t。
-
(1) 反应生成二氧化碳的质量为 g。
-
(2) 计算石灰石中碳酸钙的质量分数。(写出计算过程)

-
(1) 写出a点对应溶液的溶质(填写化学式)。
-
(2) 试求原混合溶液中CuSO4的质量分数。(写出计算过程)


-
(3) 假设向原混合溶液中滴加NaOH溶液的过程及发生的相关反应都是匀速的,请在题21-2图中画出溶液中溶剂质量与加入NaOH溶液质量关系的曲线大致位置及趋势。
|
反应前物质的质量/g |
充分反应后物质的质量/g |
|
|
过氧化氢溶液 |
二氧化锰 |
固体与液体混合物质量 |
|
100 |
0.2 |
97 |
请计算:
-
(1) 该同学制得氧气的质量为;
-
(2) 该同学所用过氧化氢溶液的溶质质量分数(本问要写出解题过程)。
请计算:
-
(1) 反应生成的CO2的质量为?
-
(2) 若所取样品为50g,则样品中NaOH的质量分数是多少?
-
(1) 识别规范使用化学仪器,对学习化学实验有着重要的意义。

①上图所示仪器的名称是;
②使用烧杯给液体加热过程中发现烧杯炸裂其原因可能是什么?(答出一条即可)
③从实验室安全角度考虑下列做法错误的是(填序号)。
a、可用嘴尝化学实验室里蔗糖的味道
b、加热试管中药品时,不可以将试管口朝向自己或他人
c、过滤操作时,将需过滤液体直接倒入过滤器中
d、实验结束后,将用剩的药品带出实验室随意丢弃
-
(2) 实验室现有石灰石、氯酸钾、二氧化锰、稀硫酸、稀盐酸五种药品及相关仪器和用品,请结合下列装置回答问题:

①若用上述药品制取较纯净的氧气,选用的装置为(填字母),发生反应的化学方程式为。
②若用上述药品制取二氧化碳,选择的装置是(填字母),反应的化学方程式为。
-
(3) 某石灰水中含有氢氧化钙1.48g,要是该石灰水中的氢氧化钙全部变为沉淀,至少需要二氧化碳的质量是多少?
-
(1) 原混合物中氯化钠的质量。
-
(2) 反应后所得溶液溶质质量分数(计算结果精确到0.1%)。
- 祖籍江苏泰州的梅兰芳先生是我国向海外传播京剧艺术的先驱,他曾于1919年、1924年和1956年三次访问日本,1930年
- 下列卤代烃,既能发生水解,又能发生消去反应且只能得到一种单烯烃的是
- 世界上人口超过1亿的国家共有( ) A、10个 B、12个
- 下列生物中只含有一种核酸的是( ) A.噬菌体 B.细菌 C.酵母菌 D.白菜
- 目前流通的第五套人民币硬币材料分别为:1元硬币为铜芯镀镍合金,5角硬币为铜芯镀铜合金,1角硬币为硬铝合金。请回答:(题目
- 在数列{an}中,an-an+1=10,a1=2,则a6等于 A.-8
- 桑蚕全身都是宝——蚕粉可用来治疗糖尿病,蚕蜕皮是手术线的原料,蚕蛹虫草可作为冬虫夏草的替代品。图4是家蚕生殖发育不同阶段
- You may do theseexercises________ in class _______after cla
- —Have youworked here since you graduated? —No, I ________ a
- 两个不同的口袋中,各装有大小、形状完全相同的个红球、个黄球.现从每一个口袋中各任取球,设随机变量为取得红球的个数,则=_
- Ilike _______new ideas. A.look for B. looking for C. lo
- 某蓄电池因使用日久而正负极标志模糊。请根据另外找到的下列两组器材和试剂,回答两种判断该正负极模糊的蓄电池的正负极的方法。
- 1954年,在《浪淘沙,北戴河》中写到:“萧瑟秋风今又是,换了人间。”这里“换了人间”主要是指 ( )
- 下列语句中,加点的词语使用最恰当的一项是(2分)( ) A.经过挑选,63名正值豆蔻年华的女孩子踏进北京警院的
- 已知函数 (I)求函数的单调区间; (II)若函数的取值范围; (III)当
- “‘2008’经济全球化与工会”国际论坛上指出,经济全球化,既给各国发展
- 设a、b、c、d、m、n都是正数,P=+,Q=,则有( )A.P≤Q B.P≥Q
- 下列关于金属物品的使用正确的是( )A.铁制车棚定期喷涂油漆 B.铁桶中加入硫酸铜溶液和石灰乳
- 结合语境,填人下面横线上的句子排列顺序恰当的一项是( )(3分) 人的一生,就像一次旅行,____
- (08年江苏卷)(10分)工业上制备BaCl2的工艺流程图如下:某研究小组在实验室用重晶石(主要成分BaSO4)对工业过









