九年级(初三)试题
-
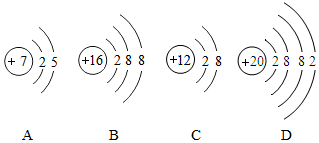
(1) 属于阳离子的是,属于阴离子的是,
-
(2) 在化学反应中容易失去电子的是,容易得到电子的是。
下图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论不正确的是 () 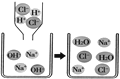
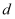 在
在 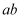 的延长线上,
的延长线上, 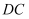 切
切 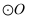 于
于 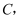 已知
已知 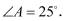
 为( )
为( )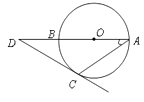
①国有经济 ②公有制经济 ③社会主义市场经济 ④非公有制经济 ⑤集体经济
 B .
B .  C .
C .  D .
D . 
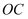 是
是 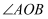 内部的一条射线,若
内部的一条射线,若 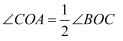 ,则我们称射线
,则我们称射线 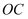 是射线
是射线 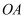 的伴随线.例如,如图1,
的伴随线.例如,如图1, 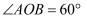 ,
,  ,则
,则 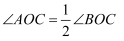 ,称射线
,称射线 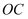 是射线
是射线 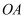 的伴随线;同时,由于
的伴随线;同时,由于 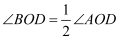 ,称射线
,称射线  是射线
是射线 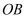 的伴随线.
的伴随线. 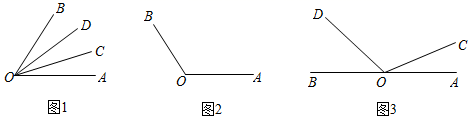
完成下列任务:
-
(1) 如图2,
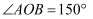 ,射线
,射线  是射线
是射线 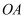 的伴随线,则
的伴随线,则 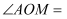
 ,若
,若 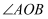 的度数是
的度数是 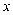 ,射线
,射线 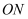 是射线
是射线 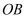 的伴随线,射线
的伴随线,射线 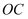 是
是 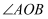 的平分线,则
的平分线,则 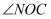 的度数是.(用含
的度数是.(用含 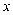 的代数式表示)
的代数式表示)
-
(2) 如图3,如
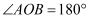 ,射线
,射线 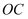 与射线
与射线 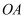 重合,并绕点
重合,并绕点 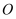 以每秒
以每秒 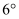 的速度逆时针旋转,射线
的速度逆时针旋转,射线  与射线
与射线 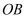 重合,并绕点
重合,并绕点 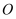 以每秒
以每秒 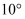 的速度顺时针旋转,当射线
的速度顺时针旋转,当射线  与射线
与射线 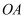 重合时,运动停止.
重合时,运动停止. ①是否存在某个时刻
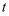 (秒),使得
(秒),使得 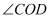 的度数是
的度数是  ,若存在,求出
,若存在,求出 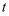 的值,若不存在,请说明理由;
的值,若不存在,请说明理由;②当
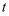 为多少秒时,射线
为多少秒时,射线 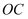 ,
,  ,
, 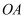 中恰好有一条射线是其余两条射线的伴随线.请直接写出结果.
中恰好有一条射线是其余两条射线的伴随线.请直接写出结果.
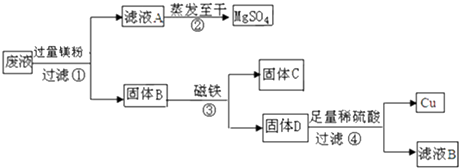
请回答:
-
(1) 滤液A和滤液B含有相同的溶质是,因此,可将滤液A和滤液B一起蒸发,其目的是.
-
(2) 写出步骤①中反应的化学方程式:,.
-
(3) 步骤①加入的镁粉为什么要过量,请你简要说明理由.
-
(4) 固体B的物质是.
 图象,若将A、B串联接入某电源两端,则闭合开关后,它们两端的电压
图象,若将A、B串联接入某电源两端,则闭合开关后,它们两端的电压  与
与  之比为;若将A、B并联接入电源两端,闭合开关后,测得干路电流为1.2A,则电源电压是V。
之比为;若将A、B并联接入电源两端,闭合开关后,测得干路电流为1.2A,则电源电压是V。 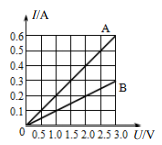
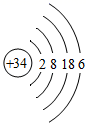
-
(1) 根据硒原子结构示意图,你能获得的信息有(填一种即可)。
-
(2) 硒离子的离子符号是。
-
(3) 410g Na2SeSO3理论上能产生g二氧化硒。
-
(1) (认识中和反应)
当两种化合物互相交换成分,生成物中有生成时,复分解反应才可以发生;中和反应属于复分解反应。
-
(2) 稀盐酸和氢氧化钠溶液混合没有明显现象,请设计实验证明稀盐酸与稀氢氧化钠溶液发生了中和反应,并完成实验报告。
实验用品包括烧杯、胶头滴管、玻璃棒、稀盐酸、稀氢氧化钠溶液、酚酞溶液。
实验步骤
实验现象
实验结论
一段时间后溶液由红色变为无色
证明稀盐酸与稀氢氧化钠溶液发生了中和反应
-
(3) (探究中和反应)
(提出问题)中和反应的实质是什么?
(查阅资料)a.一定体积的溶液中,离子的数目越多,其离子的浓度越大。电导率传感器用于测量溶液的导电性强弱,电导率值越大溶液导电能力越强。溶液的导电强弱主要与溶液中可自由移动离子的浓度和种类有关。如果离子的浓度和种类发生变化,则溶液的电导率也随之发生变化。
b.BaSO4难溶于水,即在水中难电离。
c.蒸馏水几乎不导电。
恒温条件下,向20mL一定浓度的稀Ba(OH)2溶液中滴加2滴无色酚酞溶液,插入电导率传感器,然后逐滴滴加稀硫酸,边滴加边用磁力搅拌器不断搅拌,测得溶液的电导率变化如甲图曲线所示。请写出Ba(OH)2与稀硫酸反应的化学方程式。
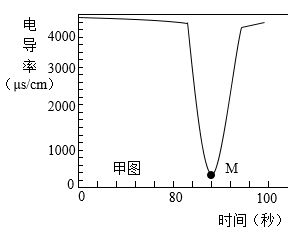
-
(4) 通过对甲图曲线的分析,下列说法正确的是_______(填字母)。A . M点前曲线下降的过程中,H+和OH-结合成H2O,Ba2+和
 结合成BaSO4
B . M点时离子浓度几乎为零
C . M点后溶液电导率逐渐增大,仅由于溶液中H+浓度逐渐增大
结合成BaSO4
B . M点时离子浓度几乎为零
C . M点后溶液电导率逐渐增大,仅由于溶液中H+浓度逐渐增大
-
(5) (拓展探究)
恒温条件下,向20mL一定浓度的稀氢氧化钠溶液中滴加2滴无色酚酞溶液,插入电导率传感器,然后逐滴滴加稀盐酸,边滴加边用磁力搅拌器不断搅拌,测得溶液的电导率变化如乙图曲线所示。通过对乙图曲线的分析,下列说法错误的是(填字母)。
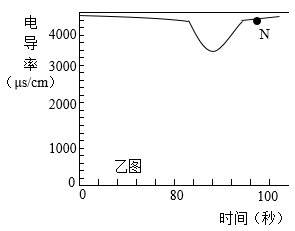
A 开始至完全反应过程中,电导率减小,溶液由红色逐渐变为无色
B 电导率下降到最低点时仍然较大,表明溶液中还存在较多离子
C 整个实验过程中,溶液中 Na+数目一直增大
-
(6) N点时,溶液中所含的离子有(填离子符号)。
-
(7) 从微观视角认识物质世界是研究化学的一种重要思维方法。下图表示乙图反应过程中烧杯中不同时间点的微观粒子示意图,按时间先后排列的顺序为(填字母)。
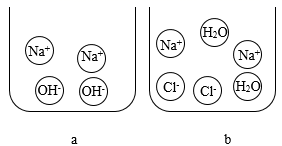
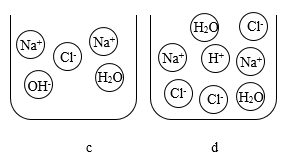
-
(8) 恒温条件下,向20mL同浓度的稀Ba(OH)2溶液中插入电导率传感器,然后滴加稀CuSO4溶液,请你预测,溶液的电导率变化与上图中的(填“甲”或“乙”)曲线更接近。
-
(1) 求这两年我市推行绿色建筑面积的年平均增长率;
-
(2) 2017年我市计划推行绿色建筑面积达到2400万平方米.如果2017年仍保持相同的年平均增长率,请你预测2017年我市能否完成计划目标?
- (极坐标系与参数方程选做题)在极坐标系中,已知曲线与直线相切,则实数a的值为 .
- (1)身边处处有化学。请从下列6种物质中选择合适物质的序号填空: ①小苏打 ②石灰石 ③盐酸 ④维生素C
- 课外科技小组制作一只“水火箭”,用压缩空气压出水流使火箭运动.假如喷出的水流流量保持为2×10-4m3/s,喷出速度保持
- 一台理想变压器,原、副线圈的匝数比∶=20∶1,原线圈接入220V的交流电压,副线圈向一电阻为110W的用电器供电,则原
- 下列各组物质中,从物质分类的角度看,后者从属于前者的是 A.纯净物、混合物 B.金属、非金属 C.纯净
- 两圆相交于两点(1,3)和(m,-1),两圆圆心都在直线x-y+c=0上,且m、c均为实数,则m+c= 3
- 化学与工农业生产和人类生活密切相关。下列说法中,不正确的是( ) w.w.w.k.s.5.u.c.o.m A.油
- 2008年10月28日,十一届全国人大常委会第五次会议通过企业国有资产法,这部受到公众普遍关注的法律历时15年终于出台。
- 自古以来,火就是纸的“天敌”。“纸包不住火”。日前,中科院上海硅酸盐研究所已成功合成出一种高柔韧性、可耐1000℃以上高
- 设M={a,b,c},N={-2,0,2},则从M到N的映射种数为
- 将等物质的量的镁和铝相混合,平均分成4份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是
- 太阳和地球间的距离为,阳光从太阳照射到地球所需的时间约为 _______秒。
- _____________,闻道龙标过五溪。(李白《闻王昌龄左迁龙标遥有此寄》)
- 设随机变量X ~ N(2,82),且P{2<x <4=0.3,则P{x <0=( ). A.0.8
- 假定英语课上老师要求同桌之间交换修改作文,请你修改你同桌写的以下作文。文中共有10处语言错误,每句中最多有两处。每处错误
- 长江被称为我国的“黄金水道”,是因为 A.河道长,流域面积广 B.流域物产丰富,运输量大 C.
- John was late for the business meeting because his flight ha
- 如图为某粒子结构示意图,下列说法错误的是()A.该元素属于非金属元素 B.该元素位于元素周期表第三横行 C.该粒子核外电
- 甲、乙两人独立破译一个密码,他们能独立译出密码的概率分别为和.(1)求甲、乙两人均不能译出密码的概率.
- 某行业2011年的劳动生产率是每小时生产2件商品,每小时创造的价值用货币表示为240元。如果某生产者2012年的劳动生产



