九年级(初三)化学试题

-
(1) 仪器a的名称;仪器b的名称。
-
(2) 实验室要制取和收集较纯净的氢气,现有镁条、锌粒、铁丝、铜片、稀硫酸(10%)、稀盐酸(10%),请你选择适当的药品和装置完成下列问题:
①制取氢气的化学方程式为,选用该原理的依据有。
A.原料廉价易得 B.反应速率适中
C.制得的气体要纯净 D.实验条件易于控制
②选用的装置有(填装置字母)。
-
(3) 用装置C制二氧化碳时,关闭开关,多孔隔板处依次观察到的现象是(用字母e、f、g对如图所示现象进行排序)。

-
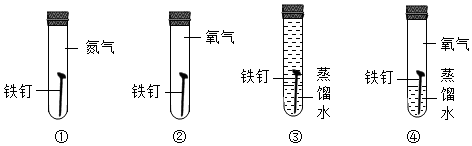
(4) 小英同学在做金属与盐溶液的反应时,发现锌片与硫酸铜溶液反应生成红色固体物质的同时有较多的气泡放出,生成的是什么气体呢?(提示:反应只生成一种气体)
【提出猜想】产生的气体可能是SO2、O2或H2中的一种。
【查阅资料】SO2易溶于水,化学性质与二氧化碳相似,它能使澄清石灰水变浑浊。
【设计并进行实验】(请在空白处写上对应问题的答案)
实验步骤
实验现象
实验结论
①向盛满该气体的试管中,插入带火星的木条
无明显变化
产生的气体不是O2
②将该气体通入澄清石灰水中
产生的气体不是SO2
③将该气体净化后通过表面含CuO的铜网(如图)

产生的气体是H2
-
(5) 【实验反思】由上述实验可以推出,硫酸铜溶液中可能含有。
-
(6) 【拓展视野】氢能是未来最理想能源,如图是利用ZnO和Fe2O3为催化剂制取氧气的一种方法。

“循环制氢体系”涉及的能量转化是由太阳能转化为能,请写出该体系制取氢气的化学方程式。

-
(1) t2℃时,a物质的溶解度为g;
-
(2) P点表示;
-
(3) t1℃时,将接近饱和的a溶液变为饱和溶液,可采用的方法(任写一种)。
物 质 | 所含杂质 | 除去杂质的试剂或方法 | |
A | NaCl溶液 | Na2CO3 | 过量盐酸,加热 |
B | CuO | Cu | 灼烧 |
C | KCl | KClO3 | MnO2 , 加热 |
D | O2 | H2O | 浓硫酸,干燥 |
实验室常用的制取气体的发生装置如下:
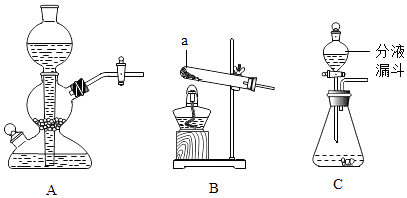
-
(1) ①仪器a的名称是;搭建B装置时,酒精灯应在固定仪器a之(选填“前”或“后”)放置.
②实验室用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式是.
-
(2) ③在实验室制取二氧化碳的研究中,进行了如下实验:
甲
乙
丙
丁
大理石
mg,块状
mg,块状
mg,粉末状
mg,粉末状
盐酸(过量)
wg,稀盐酸
wg,浓盐酸
wg,稀盐酸
wg,浓盐酸
Ⅰ.上述实验中反应的化学方程式是.
Ⅱ.若要研究盐酸浓度大小对反应的影响,可选择实验甲与对照(选填实验编号)
Ⅲ.除盐酸的浓度外,上述实验研究的另一个影响反应的因素是.
Ⅳ.研究发现酸的浓度越大,产生气体的速度越快,与甲比较,对丁分析正确的是(选填编号)
a.反应更为剧烈
b.最终剩余溶液的质量更小
c.产生二氧化碳的质量更大
d.粉末状大理石利用率更高
④表中的两个实验,尽管在原料状态、发生装置等方面存在差异,却都能控制气体较平稳的产生.请从实验目的、原理、原料、装置、操作等方面思考后,具体阐述每个实验中气体较平稳产生的最主要的一个原因.
目的
原料
发生装置
气体较平稳产生的最主要的一个原因
制取二氧化碳
块状大理石稀盐酸
A
制取氧气
粉末状二氧化锰3%的过氧化氢溶液
C
已知:2FeCl3+Fe=3FeCl2。
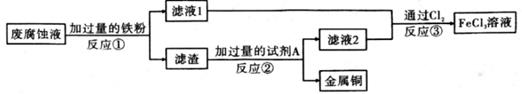
-
(1) FeCl3属于(选填“酸”“碱”或“盐”)。
-
(2) 反应①后进行的分离操作名称是,得到的滤渣成分是。
-
(3) 反应②的基本反应类型是。
-
(4) 写出反应③的化学方程式 。
-
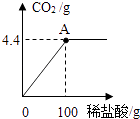
(1) CaCO3的相对分子质量
-
(2) 该石灰石样品中CaCO3的质量分数
-
(3) A点时所得溶液的溶质质量分数.
-
(1) 在盛有水的烧杯中加入以下某种物质,形成溶液的过程中温度上升。这种物质是______(填字母序号)。A . 氯化钠 B . 硝酸铵 C . 氢氧化钠 D . 浓硫酸
-
(2) 在实验室里配制50g10%的氯化钠溶液,操作如图所示,回答下列问题:
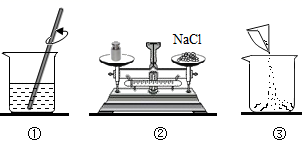
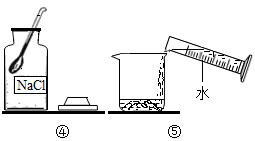
①请用图中的序号表示配制溶液的正确操作顺序。
②上图操作中有一项操作是错误的,如果其他操作步骤正确,则所配制溶液的溶质的质量分数(填“大于”“小于”或“等于”)10%。
③用15%的氯化钠溶液浸泡瓜果片刻可以起到消毒作用。常温下要使50 g 10%的氯化钠溶液的溶质质量分数变为15%,可采取的方法正确的有(计算答案取整数)。
A.加入3克的食盐搅拌 B.恒温蒸发25克水
C.与50克20%的食盐水混合 D.降温
A.干冰 B.聚乙烯 C.明矾 D.硫酸铜 E.火碱 F.稀硫酸 G.酒精 H.石灰石
-
(1) 常作生活净水剂的是;
-
(2) 可用于金属除锈的是;
-
(3) 可用于人工降雨的是;
-
(4) 可用于工业炼铁的是;
-
(5) 可用于食品包装的是;
-
(6) 可配制波尔多液的是。
2015年,我市启动了城郊河道的治理工作,羊亭河是河道治理工作的一个缩影,通过统筹运用截污治污、生态治理等手段,着力打造出了优美的水生态环境。其中一期工程对羊亭河下游2公里河道实施治理
-
(1) 下面是2014年羊亭河上、中、下游水质监测报告
编号
河段
酸碱性(正常值:6.5-8.5)
水质类别
主要污染指标
质量状况
①
上游
7.8
Ⅱ
无
良好
②
中游
6.1
Ⅳ
铜
一般
③
下游
6.3
劣Ⅴ
铜、磷、氮、氨
很差
pH是水质监测的重要指标之一,上述水样酸性最强的是。根据表中的主要污染指标分析污染物的来源可能是、(任答两点)。请列举两条河水被污染的危害:,。
-
(2) 在治理过程中,排查发现河道附近有一家化工厂,该化工厂有甲、乙两个车间,排出的废水澄清透明,经分析分别含有三种不同的离子,两厂废水中共有Ba2+、K+、Cu2+、OH-、NO3-、CO32-六种离子。
①将甲、乙两车间的废水按适当的比例混合,可以变废为宝,既能使废水中的Ba2+、Cu2+、OH¯、CO32¯等离子转化为沉淀除去,又可用上层清液来浇灌农田,清液中含的溶质主要是(填化学式)。
②经测定甲车间废水的pH=12,则乙车间废水中所含的阴离子是。
- 近几年,不断上涨的房价一直是人们关注的热点,读我国某城市住宅小区平均房价等值线分布示意图,图中数字为平均房价等值线(单位
- 东部季风区的河流() A.以雨水补给为主 B.以冰雪融水补给为主 C.以湖泊水补给为主 D.以地下水补给为主
- (16分)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300-1700oC的氮气流中反应制得3S
- 已知.证明:(1);(2).
- 一战期间民族工业发展的影响中最为深远的是( ) A.民族资产阶级的进一步壮大 B.促进了新文
- 2011年到2012年的我国县乡基层人大代表换届选举是新修改的选举法颁布实施后的第一次。全国参加县级人大代表选举的选民
- 已知分别是圆锥曲线和的离心率,设 ,则的取值范围是 A.(,0) B.(0,) C.(,1
- 公有制为主体、多种所有制经济共同发展是我国社会主义初级阶段的基本经济制度。毫不动摇地巩固和发展公有制经济,毫不动摇地鼓励
- 动物界中种类最多、数量最大、分布最广的一类动物是() A. 原生动物 B.节肢动物
- 下列数据是常见物质的pH范围,其中酸性最强的是() A.液体肥皂(9.5~10.5) B.番茄汁(4.0~4.4) C.
- 如图,在四棱锥P-ABCD中,侧面PAD⊥底面ABCD,侧棱,,底面为直角梯形,其中BC∥AD, AB⊥AD, ,O为A
- 在贝壳上滴稀盐酸,能产生使澄清石灰水浑浊的气体, 这说明贝壳中含有的离子是()。 A.Ca2+ B.CO C.SO
- Children are not permitted the film designed for adults.A.
- — Itwill _____ only about 50 minutes to travel to Mou
- 29.To pass the exam, Li Hua had a busy week ______ to the ra
- 被誉为古代织锦“活化石”的南京云锦借用西方的“错视艺术”,因其时尚度高而深得年轻人 喜爱;用硫酸纸拼装的创意秦淮花灯,内
- 18.名句默写(10分) (1)《师说》通过“古之圣人”与“今之众人”的对比,批判了“今之众人” , 。
- 用辨证的观点分析下列说法,你不赞成的是…………………………( ) A.从源头上防止环境污染,比造成污染后再去治理
- 一个容量为40的样本,数据依次为x1,x2,…,x40,若这个样本的标准差为s=,记.则等于( ) A.2
- 如图,四个边长为1的小正方形拼成一个大正方形,A、B、O是小正方形顶点,⊙O的半径为1,P是⊙O上的点,且位于右上方的小



