高一化学试题
根据  的微粒结构示意图,下列说法中错误的是( )
的微粒结构示意图,下列说法中错误的是( )
A . 它们属于不同元素
B . 它们都具有稳定结构
C . 它们都是离子
D . 它们核外电子排布相同
有①  O、
O、  O、
O、  O②H2、D2、T2③石墨、金刚石 ④
O②H2、D2、T2③石墨、金刚石 ④  H、
H、 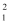 H、
H、  H四组微粒或物质.回答下列问题:
H四组微粒或物质.回答下列问题:
 O、
O、  O、
O、  O②H2、D2、T2③石墨、金刚石 ④
O②H2、D2、T2③石墨、金刚石 ④  H、
H、 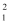 H、
H、  H四组微粒或物质.回答下列问题:
H四组微粒或物质.回答下列问题:
-
(1) 互为同位素的是(填编号).
-
(2) 由①和④中微粒结合形成的水分子种类有种.
在容积为2L的密闭容器中进行如下反应:A(g)+2B(g)⇌3C(g)+nD(g),开始时A为4mol,B为6mol,5 min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol•L﹣1•min﹣1 .
计算:
-
(1) 5min末A的物质的量浓度,
-
(2) B的转化率为.
-
(3) 前5min内用B表示的化学反应速率v(B).
-
(4) 化学方程式中n值.
在①178O、1②188O、③2311Na、④2412Mg、⑤146C、⑥147N中:
-
(1) 和互为同位素(填序号,下同);
-
(2) 和的质量数相等,但不能互称同位素;
-
(3) 和的中子数相等,但质子数不等,所以不是同一种元素.
已知还原性:SO32﹣>I﹣ . 向含有amolKI和amolK2SO3的混合液中通入bmolCl2充分反应(不考虑Cl2与I2之间的反应).下列说法不正确的是( )
A . 当a≥b时,发生的离子反应为SO32﹣+Cl2+H2O=SO42﹣+2H++2Cl﹣
B . 当5a=4b时,发生的离子反应为SO32﹣+2I﹣+5Cl2+4H2O=4SO42﹣+I2+8H++10Cl﹣
C . 当a≤b≤  a时,反应中转移电子的物质的量n(e﹣)为amol≤n(e﹣)≤3amol
D . 当a<b<
a时,反应中转移电子的物质的量n(e﹣)为amol≤n(e﹣)≤3amol
D . 当a<b<  a时,溶液中SO42﹣、I﹣与Cl﹣的物质的量之比为a:(3a﹣2b):2b
a时,溶液中SO42﹣、I﹣与Cl﹣的物质的量之比为a:(3a﹣2b):2b
 a时,反应中转移电子的物质的量n(e﹣)为amol≤n(e﹣)≤3amol
D . 当a<b<
a时,反应中转移电子的物质的量n(e﹣)为amol≤n(e﹣)≤3amol
D . 当a<b<  a时,溶液中SO42﹣、I﹣与Cl﹣的物质的量之比为a:(3a﹣2b):2b
a时,溶液中SO42﹣、I﹣与Cl﹣的物质的量之比为a:(3a﹣2b):2b
在标况下,下列各组气体混合其平均相对分子量可达到40的是( )
A . N2和O2
B . CO2和O2
C . SO2和CO2
D . HI和Cl2
将等质量的下列各烃,完全燃烧生成CO2和H2O,耗氧量最大的是( )
A . CH4
B . C2H4
C . C6H6
D . C3H6
乙醇、乙二醇、丙三醇分别与足量金属钠反应产生等体积的H2(相同状况下),则上述三种醇物质的量之比为( )
A . 2:3:6
B . 3:2:1
C . 4:3:1
D . 6:3:2
现有A,B,C三种化合物,各取40g相混合,完全反应后,得18g B,49g C,还有D生成.已知D的相对分子质量为106.现将80g A和33g B反应,能生成D( )
A . 1 mol
B . 0.5 mol
C . 0.75 mol
D . 0.25 mol
某硫单质的分子式为Sx , n mol的Sx在足量氧气中完全燃烧,产生气体全部通入含有m molCa(OH)2的石灰水中,恰好完全沉淀,且8n=m,则x的值为( )
A . 8
B . 6
C . 4
D . 2
下列化学用语正确的是( )
A .  H、
H、  H、H+和H2是氢元素的四种不同粒子
B . 18O2和16O3互为同位素
C . S2-的结构示意图为:
H、H+和H2是氢元素的四种不同粒子
B . 18O2和16O3互为同位素
C . S2-的结构示意图为:  D .
D .  U中质子数和中子数相差147
U中质子数和中子数相差147
 H、
H、  H、H+和H2是氢元素的四种不同粒子
B . 18O2和16O3互为同位素
C . S2-的结构示意图为:
H、H+和H2是氢元素的四种不同粒子
B . 18O2和16O3互为同位素
C . S2-的结构示意图为:  U中质子数和中子数相差147
U中质子数和中子数相差147
将一定质量的铜溶于50mL 11mol/L的浓硝酸中,待铜完全溶解后,生成0.2mol NO2和NO的混合气体,并测得溶液中H+的浓度为1mol/L.假设反应后溶液的体积仍为50mL,则金属铜的质量为( )
A . 6.4g
B . 9.6g
C . 11.2g
D . 12.8g
若某原子的摩尔质量是M g/mol,则一个该原子的真实质量是( )
A . M g
B .  g
C .
g
C .  g
D .
g
D .  g
g
 g
C .
g
C .  g
D .
g
D .  g
g
取1.43gNa2CO3•xH2O溶于水配成10mL溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸2.0mL,并收集到112mL CO2(标准状况).试计算:
-
(1) CO2的物质的量
-
(2) Na2CO3•xH2O的物质的量.
-
(3) x的值.
-
(4) 所用稀盐酸的物质的浓度.
同位素示踪法可用于反应机理的研究,下列反应中同位素示踪表示正确的是()
A . 2Na218O2 + 2H2O = 4Nal8OH + O2↑
B . NH4Cl + 2H2O  NH3·2H2O + HCl
C . K37ClO3 + 6HCl = K37Cl + 3Cl2↑ + 3H2O
D . 2KMnO4 + 5H218O2 + 3H2SO4 = K2SO4 + 2MnSO4 + 518O2↑ + 8H2O
NH3·2H2O + HCl
C . K37ClO3 + 6HCl = K37Cl + 3Cl2↑ + 3H2O
D . 2KMnO4 + 5H218O2 + 3H2SO4 = K2SO4 + 2MnSO4 + 518O2↑ + 8H2O
 NH3·2H2O + HCl
C . K37ClO3 + 6HCl = K37Cl + 3Cl2↑ + 3H2O
D . 2KMnO4 + 5H218O2 + 3H2SO4 = K2SO4 + 2MnSO4 + 518O2↑ + 8H2O
NH3·2H2O + HCl
C . K37ClO3 + 6HCl = K37Cl + 3Cl2↑ + 3H2O
D . 2KMnO4 + 5H218O2 + 3H2SO4 = K2SO4 + 2MnSO4 + 518O2↑ + 8H2O
将6.4g铜与足量的浓硫酸在加热情况下充分反应,铜没有剩余.试计算:提示:(Cu+2H2SO4(浓)  CuSO4+SO2↑+2H2O)
CuSO4+SO2↑+2H2O)
 CuSO4+SO2↑+2H2O)
CuSO4+SO2↑+2H2O)-
(1) 参加反应的硫酸的物质的量.
-
(2) 生成的SO2的体积(标准状况下).
-
(3) 将反应后的溶液用水稀释到100mL,计算硫酸铜溶液的物质的量浓度.
将一定量的饱和一元醇分成两等份,将其中一份完全燃烧,消耗28.8g氧气,在另一份中加入过量金属钠,产生2.24L(标况)H2 , 则该醇的分子式为( )
A . 乙醇
B . 丙醇
C . 丁醇
D . 甲醇
下列各组化合物中,不论二者以任何比例混合,只要总质量一定,则完全燃烧时消耗O2的质量和生成水的质量不变的是( )
A . CH4、C2H6
B . C2H6、C3H6
C . C2H4、C3H6
D . C2H4、C3H4
某元素1个原子的质量是a g,又知1个12C原子的质量为b g,NA表示阿伏加德罗常数
① ②
② ③aNA ④
③aNA ④ 数,则下列各式中能表示该原子的相对原子质量数值的是( )
数,则下列各式中能表示该原子的相对原子质量数值的是( )
A . ①②
B . ①④
C . ②④
D . ②③
已知向某碳酸盐溶液中滴加稀盐酸至过量,生成气体的质量(m)与加入盐酸的体积(V)的关系如图一所示.现将1.12gKOH和1.38gK2CO3混合并配成溶液,向其中滴加稀盐酸,图二是甲、乙、丙三位同学分别绘制的产生气体的质量(m)与稀盐酸的体积(V)的关系的示示意图.下面判断正确是( )

A . 甲图正确
B . 乙图正确
C . 丙图正确
D . 无法判断
最近更新
- 有甲、乙、丙3种气体,甲为无色,可由两种单质气体化合而成,在一定条件下,甲能与氧气反应生成乙;乙不溶于水,但能进一步与氧
- 某研究性学习小组调查发现,甲、乙两工厂排放的污水各含下列离子H+、Cu2+、K+、NO3—、OH—中的三种离子(两厂含有
- 【湖南省娄底市】(二)使至塞上 使至塞上 王维 单车欲问边,属国过居延。征蓬出汉塞,归雁入胡天。 大漠孤烟直,长河落日圆
- 依次填入下列句子中的词语,恰当的一组是: ①如果我们的编辑都能够 ,敢说敢劝,那么某些不良文风和诗风或许会早日改
- 下列不属于青春期发育特征的是A.身高突增
- 为达到相应的实验目的,下列实验的设计或操作最合理的是( ) A.为比较Cl与S元素的非金属性强弱,相同条
- 一个质点做方向不变的直线运动,加速度的方向始终与速度方向相同,但加速度大小逐渐减小直至为零,在此过程中()A.速度逐渐减
- 下列给变量赋值的语句正确的是() A.3=a B.a+1=a C.a=b
- “酒驾”是当前热门话题之一.交巡警检查驾驶员是否饮酒的仪器里装有K2Cr2O7,K2Cr2O7中Cr元素的化合价为()
- 奥司他韦是治疗新型甲型H1N1流感的首选药物。其分子式为C16H28N2O4·H3PO4,结构简式如右图所示:根据奥司他
- 分析位于52ºS附近某地区的相关等值线图,回答问题 (1)简析该区域东西两侧降水差异及原因。(2)简析该地区气温分布规律
- 下列有关氧化还原反应的叙述正确的是 A.金属单质在氧化还原反应中只能作还原剂,非金属单质只能作氧化剂 B.化合物中某元素
- .在四棱锥的底面是菱形, 底面,, 分别是的中点, .(Ⅰ)求证: ; (Ⅱ)求直线与平面所成角的正弦值; (III)在
- 一瓶含有酵母菌的葡萄糖溶液,当通入不同浓度的氧气时,其产生的C2 H 5O H 和CO2的量如表所示。下列叙述错误的是
- 2010年公立医院改革试点有序推进,新能源汽车补贴试点启动,教育体制改革的十大试点陆续启动。先行试点主要体现的辩证法道理
- 关于磁场,下列说法中正确的是( )A.其基本性质是对处于其中的磁体和电流有力的作用B.磁场是看不见摸不着、实际不存
- 乙偶姻(F)是一种重要的香料,存在于啤酒中,是酒类调香中一个极其重要的品种。某人工合成乙偶姻的路线如下: 已知:请回答下
- 14—16世纪,世界历史发生着深刻而巨大的变化,一个崭新的时代即将到来,下列事件为新时代的到来创造条件的是 ①文
- 有一种专门存放贵重物品的“银行”,为了防止物品被冒领,“银行”必须记录下存放者的“手纹”、“眼纹”和“声纹”,今后存放者
- 如图6-10所示是简化后的跳台滑雪的雪道示意图.整个雪道由倾斜的助滑雪道AB和着陆雪道DE,以及水平的起跳平台CD组成,



