高一化学试题
某有机物的蒸汽完全燃烧时需三倍于其体积的氧气,产生二倍于其体积的二氧化碳该有机物可能是( )
A . C2H6
B . C2H5OH
C . C2H4O
D . C2H4O2
下列是几种原子结构示意图,其中正确的是
A .  B .
B .  C .
C .  D .
D . 
两种金属混合物共15g,投入足量的盐酸中,充分反应得11.2L H2(标况下)则原混合物组成中肯定不能为下列的( )
A . Mg、Al
B . Fe、Mg
C . Al、Zn
D . Mg、Zn
向溶10mLNaHSO4液中逐滴滴加Ba(OH)2溶液,产生沉淀的质量m与加入的Ba(OH)2的物质的量n之间的关系如图所示,下列说法错误的是( )

A . a点溶液中离子浓度:c(Na+)>c(SO  )
B . b点溶液为中性,c点SO
)
B . b点溶液为中性,c点SO  恰好沉淀完全
C . b→c段发生反应为H++SO
恰好沉淀完全
C . b→c段发生反应为H++SO  +Ba2++OH-=BaSO4↓+H2O
D . 原溶液的浓度为2.0mol•L-1
+Ba2++OH-=BaSO4↓+H2O
D . 原溶液的浓度为2.0mol•L-1
 )
B . b点溶液为中性,c点SO
)
B . b点溶液为中性,c点SO  恰好沉淀完全
C . b→c段发生反应为H++SO
恰好沉淀完全
C . b→c段发生反应为H++SO  +Ba2++OH-=BaSO4↓+H2O
D . 原溶液的浓度为2.0mol•L-1
+Ba2++OH-=BaSO4↓+H2O
D . 原溶液的浓度为2.0mol•L-1
将0.2mol MnO2和50mL 12mol•L﹣1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量的AgNO3溶液,生成AgCl的物质的量为(不考虑盐酸的挥发)( )
A . 等于0.3 mol
B . 小于0.3 mol
C . 介于0.3~0.6 mol之间
D . 以上都不正确
下列物质之间的相互关系不正确的是( )
A . CH3﹣CH2﹣NO2和H2N﹣CH2﹣COOH互为同分异构体
B . H、D、T互为同位素
C . O2和O3互为同素异形体
D . CH3CH2CH2CH3与 性质完全相同
性质完全相同
 性质完全相同
性质完全相同
已知金属钠投入水中能发生下列反应2Na+2H2O═2NaOH+H2↑.如将2.3g钠投入水中,充分反应.据此,请计算下列问题:
-
(1) 求生成的NaOH的物质的量;
-
(2) 求生成的H2的体积(标准状况).
“华龙一号”是我国自主研制的核电技术,其使用后的乏燃料中含有  Pu和
Pu和  Pu。下列有关说法错误的是( )
Pu。下列有关说法错误的是( )
 Pu和
Pu和  Pu。下列有关说法错误的是( )
Pu。下列有关说法错误的是( )
A .  Pu中所含中子数为144
B .
Pu中所含中子数为144
B .  Pu和
Pu和  Pu互为同位素
C . 由
Pu互为同位素
C . 由 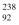 U转化为
U转化为  Pu的过程属于化学变化
D .
Pu的过程属于化学变化
D .  Pu和
Pu和  Pu的核外电子数均为94
Pu的核外电子数均为94
 Pu中所含中子数为144
B .
Pu中所含中子数为144
B .  Pu和
Pu和  Pu互为同位素
C . 由
Pu互为同位素
C . 由 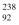 U转化为
U转化为  Pu的过程属于化学变化
D .
Pu的过程属于化学变化
D .  Pu和
Pu和  Pu的核外电子数均为94
Pu的核外电子数均为94
铜元素有质量数为63和65的两种天然同位素,它的近似相对原子质量是63.5,则同位素63Cu所占的质量百分比为( )
A . 20%
B . 25%
C . 74.4%
D . 75%
固体A在一定温度下分解生成气体的反应为:2A=B↑+2C↑+3D↑,若测得相同条件下生成的混合气体对氢气的相对密度为15,则固体A的摩尔质量是( )
A . 30g/mol
B . 60 g/mol
C . 90g/mol
D . 120 g/mol
下列有关同位素的说法错误的是( )
A . 同位素是指同一元素的原子中,中子数不同的核素
B . 元素周期表中,每种元素都存在同位素
C . 天然存在的同位素,相互间保持一定的比率
D . 核电池(又称同位素电池)就是以放射性核素为主要原料制成的特殊能源
用铝热法从下列金属氧化物中制取相应的金属各1mol,消耗铝的质量最多的是( )
A . Fe2O3
B . V2O5
C . MnO2
D . Cr2O3
下列化学用语错误的是 ( )
A . S2-的结构示意图:  B . 中子数为7的氮原子
B . 中子数为7的氮原子  N
C . 葡萄糖分子的实验式:CH2O
D . 乙炔的结构式:H-C≡C-H
N
C . 葡萄糖分子的实验式:CH2O
D . 乙炔的结构式:H-C≡C-H
 N
C . 葡萄糖分子的实验式:CH2O
D . 乙炔的结构式:H-C≡C-H
N
C . 葡萄糖分子的实验式:CH2O
D . 乙炔的结构式:H-C≡C-H
向铜片中加入某浓度的硫酸120ml,在加热条件下反应,待铜片全部溶解后,将其溶液稀释到500ml。再加入足量锌粉,使之充分反应,收集到标准状况下氢气2.24L,过滤残留固体,干燥后称量,质量减轻了7.50g。求:
-
(1) 溶解的铜的质量。
-
(2) 原硫酸的物质的量浓度。(要求写出简要计算过程)
根据题意进行计算:
-
(1) 向200mL0.5mol/LAl2(SO4)3溶液中,加入350mL2mol/L NaOH溶液,充分反应后可以得到Al(OH)3沉淀多少g?
-
(2) 若想得到3.9g Al(OH)3沉淀,应向200mL0.5mol/LAl2(SO4)3溶液中加入2mol/L NaOH溶液多少mL?
3.6g碳在一定量的氧气中燃烧,完全反应后生成的气体质量为9.2g.则在标准状况下,生成物CO和CO2的体积比为( )
A . 3:2
B . 4:1
C . 5:1
D . 7:4
在光照条件下,CH4能与Cl2发生取代反应.若1mol CH4与一定的量的Cl2完全反应,反应后有四种取代产物生成,且四种产物物质的量相等,则消耗的Cl2为( )
A . 4 mol
B . 2.5 mol
C . 2 mol
D . 0.5 mol
25℃和101kPa时,甲烷、乙炔和乙烯组成的混合烃10mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小17.5mL,原混合烃中乙炔的体积分数为( )
A . 12.5%
B . 25%
C . 50%
D . 75%
铯  可用于超高精度原子钟,下列对于
可用于超高精度原子钟,下列对于  和
和  描述错误的是()
描述错误的是()
 和
和  描述错误的是()
描述错误的是()
A . 互为同位素
B . 化学性质相同
C . 质量数不同
D . 核外电子数不同
分别完全燃烧1molC2H6、C2H4、C2H2、C2H6O,需要氧气最多的是( )
A . C2H6
B . C2H4
C . C2H2
D . C2H6O
最近更新
- 如图所示,在固定正点电荷Q的电场中,一个正检验电荷q沿着一条电场线运动。已知检验电荷经过M点时的加速度是经过N点时的加速
- 大棚中种植的植物其光合作用会受到多种因素的影响,在下曲线图中,有M、N、O、P、Q五个点,对它们的含义的叙述正确的有()
- Some of the scientists held the point ______ the book said w
- 2011年5月1日起,我国实行的道路交通安全法明确规定,醉酒驾车将面临刑事处罚。酒驾容易引发交通事故的主要原因是(
- 下列句子中有错别字的一句是( ) A.宋祖英在钢琴演奏声中缓缓地从舞台下方升起,与8名小演员深情演唱《爱我中华》。
- He’s _______ to fail the exam if he doesn’t do any revision.
- 已知函数,则下列结论正确的是( ) A. 是偶函数 B. 是增函数 C. 的最小值是 D. 的值域为
- 读图,回答25-26题。25.甲、乙两地所在国家分别是
- 分析一个DNA分子时,发现30%的脱氧核苷酸含有腺嘌呤,由此可知,该DNA分子中一条链上鸟嘌呤的含量的最大值可占此链碱基
- 通过宗法制的实行,西周形成一个庞大的宗族网,“大宗能率小宗,小宗能率群弟”。按宗法制的规定,下列在相当范围内一定能成为大
- 构成并保持水化学性质的最小粒子是______;在氧气、二氧化碳、二氧化硫中都含有相同的_______;在它们相同数目的分
- 如图所示,在光滑绝缘的水平轨道上方同时存在着水平向右的匀强电场和垂直纸面向里的匀强磁场,磁场的磁感应强度B=0.1T。一
- 已知f(x)是周期为4的偶函数,当x∈[0,2]时,f(x)=x-1,则不等式xf(x)>0在区间 [-1,3]上
- 近年来,我国部分地区先后遭遇持续干旱,造成人畜饮水困难,各地采取措施积极抗旱。请回答下列问题:(1)自然界中的水都不是纯
- 新中国成立以来科技发展的主要成就不包括 A.克隆羊多利 B.杂交水稻的培育 C.载人航天技术 D.原子弹爆炸
- 由于森林的过量砍伐、草场大面积开垦,土地出现沙漠化,导致我国部分地区时常现雾霾天气。你认为雾霾天气使空气中增加了大量的
- 函数的图像经过四个象限的充要条件A. B. C. D.
- 请以“有一种美丽叫 (坚强、平淡、仁慈、‘实话实说’、永不言弃……)”为题写一篇文章。要求:⑴先将
- Inyour company there are a few machines similar to ________
- 下列叙述正确的是( )A.CO2分子间存在着共价键B.CO2分子内存在着极性共价键C.SO2与H2O反应的产物是离



