高一化学试题
为了测定铁铜合金的组成,将7.6g铁、铜合金加入100mL某浓度的稀硝酸中,待合金完全溶解后,共收集到NO气体2.24L(标准状况下),并测得溶液中H+的浓度为0.5mol•L﹣1 . 若反应前后溶液的体积变化忽略不计,则下列判断正确的是( )
A . 上述反应中金属共失去电子0.1 mol
B . 合金中,铜的质量为2.8 g
C . 原硝酸的浓度:c(HNO3)=4.5 mol•L﹣1
D . 要使溶液中的金属离子完全沉淀,需加5 mol•L﹣1的NaOH溶液60 mL
下列反应中,反应后固体质量减轻的是( )
①氨气通过灼热的CuO粉末
②二氧化碳通过Na2O2粉末
③水蒸气通过灼热的Fe粉
④Zn投入CuSO4溶液.
A . ①②
B . ①④
C . ②③
D . ②④
2020年10月,我国将实施嫦娥五号登月计划,实现月面无人采样返回。月球土壤中含有丰富的  He,则该原子中( )
He,则该原子中( )
 He,则该原子中( )
He,则该原子中( )
A . 质量数为2
B . 中子数为2
C . 核外电子数为2
D . 质子数为3
已知某微粒的结构示意图为:  ( y≠0 ).请回答:
( y≠0 ).请回答:
 ( y≠0 ).请回答:
( y≠0 ).请回答:
-
(1) 当x﹣y=10时,该微粒为(填“原子”、“阳离子”或“阴离子”).
-
(2) 当y=8时,微粒可能为(不少于5种).
-
(3) 写出x+y=12与x+y=16的元素最高价氧化物对应水化物相互反应的离子方程式.
含有0.30g甲醛的水溶液与过量银氨溶液充分反应,生成的银有( )
A . 4.32g
B . 2.16g
C . 0.02g
D . 0.04g
化学与生活息息相关,在研究具体问题的时候会运用很多方法,其中一种就是把体积和压强的影响,转化成盒子进行研究.
I在一密闭气缸内,用不漏气的可滑动的活塞隔成两室(图1),左室充有甲烷(CH4)和氧气的混合气体,右室充有氯气和氢气.已知当氧气足够多时甲烷完全燃烧,生成CO2 , 氧气不足时有CO生成,Cl2+H2═2HCl.在室温下,静止在气缸的“3”处(液体体积忽略不计).

-
(1) 若反应前左室中CH4与O2物质的量之比为1:2,现将左右两室混合气体点燃,完全反应,冷却至原室温,活塞最终静止于气缸处(填具体刻度).
-
(2) 若左室反应前充有一定量的CH4与O2的混合气体,点燃左右两室气体,使其充分反应,在左室中未检测到有毒气体,冷却至室温,活塞最终静止于气缸“2”处,求反应前CH4与O2的物质的量之比为.
-
(3) 室温下,现有20LO2 , 把它通入14L CO和H2的混合气体中,完全燃烧,干燥后恢复到原来的温度.若剩余气体的体积为nL,则原混合气体中V(CO):V(H2)=,n的取值范围是.
-
(4) 若用图2装置进行O2的燃烧反应,其中P是可自由平行滑动的活塞,关闭K,将6molH2充入容器的A室中,将2molCO与8molO2的混合气体充入容器的B室中.已知起始时容器A和B的体积均为a L.试回答:
i点燃B室中的混合气体,恢复到120℃,反应达到平衡时容器B的体积为L.
ii若打开K,点燃混合气体,使CO、H2和O2充分反应,恢复到120℃则反应完全后,容器B的体积为L(连通管中气体体积忽略不计,且不考虑温度的影响).
下列说法正确的是( )
A . a克CH4在氧气中完全燃烧,将其产物全部跟足量的过氧化钠完全反应,反应后固体质量恰好也增加a克
B . 将等物质的量的Na2O和Na2O2分别投入到足量且等质量的水中,得到溶质质量分数相等
C . 1mol Na2O2与2mol NaHCO3固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是Na2CO3
D . 向某溶液中加入氯水,然后再加入KSCN溶液变红色,说明原溶液中含有Fe2+
已知元素R的某种同位素的氯化物RClx为离子化合物,其阳离子所含中子数为y,核外电子数为z,则该同位素的符号为( )
A .  R
B .
R
B .  R
C .
R
C .  R
D .
R
D .  R
R
 R
B .
R
B .  R
C .
R
C .  R
D .
R
D .  R
R
氯元素在自然界有35Cl和37Cl两种同位素,在计算式34.969×75.77%+36.966×24.23%=35.453中( )
A . 75.77%表示35Cl的质量分数
B . 24.23%表示35Cl的丰度
C . 35.453表示氯元素的相对原子质量
D . 36.966表示37Cl的质量数
生态农业涉及农家肥料的综合利用.某种肥料经发酵得到一种含有甲烷、二氧化碳、氮气的混合气体8.96L(标准状况).该气体通过盛有红色CuO粉末的硬质玻璃管,发生的反应为:CH4+4CuO  CO2↑+2H2O↑+4Cu.当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g.将反应后气体通入2L0.1mol/L的澄清Ca(OH)2溶液,充分吸收,生成沉淀10g.求:
CO2↑+2H2O↑+4Cu.当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g.将反应后气体通入2L0.1mol/L的澄清Ca(OH)2溶液,充分吸收,生成沉淀10g.求:
 CO2↑+2H2O↑+4Cu.当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g.将反应后气体通入2L0.1mol/L的澄清Ca(OH)2溶液,充分吸收,生成沉淀10g.求:
CO2↑+2H2O↑+4Cu.当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g.将反应后气体通入2L0.1mol/L的澄清Ca(OH)2溶液,充分吸收,生成沉淀10g.求:
-
(1) 原混合气体中甲烷的体积(标准状况)《写出计算过程)
-
(2) 反应后的气体中CO2的物质的量可能为
-
(3) 原混合气体中氮气的体积为.
将足量的MnO2与含14.6gHCl的浓盐酸共热制取氯气,可制得Cl2的质量是( )
A . 等于7.1g
B . 小于7.1g
C . 大于7.1g,小于14.2g
D . 大于14.2g
14C常用于测定生物遗骸的年份.下列说法中正确的是( )
A . 14C相对原子质量等于14
B . 14C与14N中子数一定不同
C . 14C与C60互为同素异形体
D . 14C与12C是两种不同的元素
甲、乙、丙、丁四个烧杯内分别放人0.1mol的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入100mL水,搅拌,使固体完全溶解,则甲、乙、丙、丁的质量分数大小的顺序是( )
A . 甲<乙<丙<丁
B . 丁<甲<乙<丙
C . 丁<甲<乙=丙
D . 甲=丁<乙=丙
适量CO2通入含0.8gNaOH的碱溶液中,将所得的溶液在减压、低温下蒸干 后得到1.0g固体物质,则该固体物质的成分是( )
A . Na2CO3
B . NaHCO3
C . Na2CO3、NaHCO3
D . Na2CO3、NaOH
15g A物质和10.5g B物质完全反应,生成7.2g C物质,1.8g D物质和0.3mol E物质,则E物质的摩尔质量是( )
A . 100g/mol
B . 100g
C . 55g/mol
D . 55g
将一定量的有机物充分燃烧后的产物通入足量的石灰水中完全吸收,经过滤得沉淀20g,滤液质量比原石灰水减少5.8g,该有机物不可能是( )
A . 乙烷
B . 乙醇
C . 乙二醇
D . 乙烯
将m g镁铝合金投入到500 mL 2 mol/L的盐酸中,固体完全溶解,收集到气体5.6L(标准状况下)。向反应所得溶液中加入4mol/L的氢氧化钠溶液,沉淀达到最大值为13.60 g,则m的值为( )
A . 5.10
B . 8.50
C . 9.35
D . 11.48
将amol NaHCO3和bmol Na2O2固体混合后,在密闭容器中加热到250℃,让其充分反应.当剩余固体为Na2CO3、NaOH,排出气体为O2、H2O时, 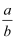 的值可能为( )
的值可能为( )
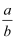 的值可能为( )
的值可能为( )
A . 1.0
B . 1.35
C . 1.5
D . 2.0
画出下列元素的原子结构示意图。
①核电荷数为13的元素:。
②某元素原子的最外层电子数等于次外层电子数: 。
③L 层电子数是M层电子数2倍的元素: 。
把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为( )
A .  mol·L-1
B .
mol·L-1
B .  mol·L-1
C .
mol·L-1
C .  mol·L-1
D .
mol·L-1
D .  mol·L-1
mol·L-1
 mol·L-1
B .
mol·L-1
B .  mol·L-1
C .
mol·L-1
C .  mol·L-1
D .
mol·L-1
D .  mol·L-1
mol·L-1
最近更新
- 如图,已知ABCD是一块边长为100 m的正方形地皮,其中AST是一半径为90 m的扇形小山,其余部分是平地.一开发商想
- 义乌市活鱼塘村原村支书金新华,因一系列违法犯罪行为被义乌市人民法院依法惩处。他在庭审时语出惊人:“做干部就是为了钱。”记
- 从半球位置看,中国位于()A .西半球、北半球B .东半球、北半球C .西半球、南半球D .东半球、南半球
- 乌干达、肯尼亚、坦桑尼亚三国是非洲也是世界主要咖啡出口国之一,该地区生产的咖啡品质优良,是传统的出口产品,同时也是重要的
- 台湾的人口和城市主要分布在( ) A.东部地区 B.南部地区 C.西部地区 D.北部地
- 2004年我国汽车总产量达507万辆,但在各项基础中90%是“舶来品”,而真正具有我国自主产权的技术仅占10%。这表明
- 下列图幅大小相同的四张地图,表示的内容最详细的是( ) A. 世界地图 B. 中
- 穆公亡马 秦穆公①尝出而亡其骏马,自往求之,见人已杀其马,方共食其肉。穆公谓曰:“是吾骏马也。”诸人皆惧而起。穆公曰:“
- 如图6所示,将同一个物体分别沿AB和AC两个光滑斜面匀速拉到顶端。两次的拉力分别为F1和F2,两次做的功分别为W1和W2
- 关于钠及其化合物性质的叙述,正确的是() A.相同条件下,在水中碳酸钠的溶解度小于碳酸氢钠的溶解度 B.氧化钠和过氧化钠
- 当物体从高空下落时,所受阻力会随物体的速度增大而增大,因此经过下落一段距离后将匀速下落,这个速度称为此物体下落的收尾速度
- 关于碳循环的叙述,错误的是A.二氧化碳可以在无机环境和生物群落中被循环使用 B.需要能量驱动 C.是单向流动
- If we work hard,wewill have a to achieve mydream.
- 雄果蝇的一个体细胞经正常的有丝分裂形成两个子细胞(C1、C2),一个初级精母细胞经正常的减数第一次分裂形成两个次级精母细
- 足球运动员把足球踢向空中,若不计空气阻力,则图1是表示足球在空中飞行的受力图,正确的是(G表示重力,F表示脚对球的作用力
- 明朝中后期资本主义萌芽产生的标志是A.手工业的水平超过前代 B.商品经
- 在一定条件下,将A2和B2气体通入1 L密闭容器中,反应按下式进行:mA2+nB22C,2 s内反应速率如下:v(A2)
- 如图,把一块含有45°角的直角三角板的两个顶点放在直尺的对边上.如果∠1=20o,那么∠2的度数是( ) A.3
- 光导纤维的结构如图所示,其内芯和外套材料不同,光在内芯中传播。以下关于光导纤维的说法正确的是A.内芯的折射率比外套大,光
- 右图是A、B、C三种固体物质的溶解度曲线,当它们的溶液接近饱和时,若分别采用升高温度、蒸发溶剂、增加溶质的方法,均可使之



