高一化学下学期下册试题
在某强酸性溶液中因发生氧化还原反应而不能大量共存的离子组是( )
A.K+、Fe2+、Cl-、NO3- B.Al3+、NH4+、OH- 、NO3--
C.Na+、H+、Cl-、CO3- D.Mg2+、Ba2+、SO42-、Cl-
下列各项中表达正确的是( )
A.H、D、T表示同一种核素 B.F-离子结构示意图![]()
C.次氯酸电子式![]() D.用电子式表示HCl形成过程
D.用电子式表示HCl形成过程![]()
![]()
如图是元素周期表的一部分,下列叙述不正确的是( )

A. Pb的最高正价为+4
B. 原子半径比较:Al>F
C. 酸性强弱:H3AsO4<H2SeO4
D. Br的最高价氧化物对应水化物的化学式为HBrO3
下列说法中错误的是( )
A. 在周期表中,原子的核外电子层数等于该元素所在的周期数
B. 元素周![]() 期表中从IIIB族到IIB族10个纵行的元素都是金属元素
期表中从IIIB族到IIB族10个纵行的元素都是金属元素
C. 室温时,零族元素的单质都是气体
D. 位于IA![]() 的元素与位于VIIA的元素组成的化合物都是离子化合物
的元素与位于VIIA的元素组成的化合物都是离子化合物
根据SO2通入不同溶液中实验现象,所得结论不正确的是
| 实验 | 现象 | 结论 | |
| A | 含HCl、BaCl2的FeCl3溶液 | 产生白色沉淀 | SO2 有还原性 |
| B | H2S 溶液 | 产生黄色沉淀 | SO2 有氧化性 |
| C | 酸性KMnO4溶液 | 紫色溶液褪色 | SO2 有漂白性 |
| D | Na2SiO3溶液 | 产生胶状沉淀 | 酸性:H2SO3> H2SiO3 |
A. A B. B C. C D. D
下列关于戊烷的说法正确的是
A.分子中的碳原子在一条直线上 B.其一氯代物共有8种
C.能与溴水发生取代反应 D.同分异构体有2种
图中UZ六种物质在适当条件下能实现图示箭头方向一步转化,且反应①、②均为置换反应,满足条件的物质组是( )
| 序号 | U | W | Y | X |
|
| ① | Na | H2O | Na2O2 | NaOH | |
| ② | Fe | H2O | C | H2 | |
| ③ | HBr | Cl2 | CH4 | HCl | |
| ④ | CuCl2(aq) | Al | HCl(aq) | AlCl3(aq) |
A. ②④ B. ②③ C. ①②④ D. ①②③④
已知2SO2+O2![]() 2SO3为放热反应,关于该反应的下列说法正确的是( )
2SO3为放热反应,关于该反应的下列说法正确的是( )
A. O2的能量一定高于SO2的能量
B. SO2和O2的总能量一定高于SO3的总能量
C. SO2的能量一定高于SO3的能量
D. 因该反应为放热反应,故不必加热反应就可发生
A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,A的单质为密度最小的气体,B、W同周期,A、D同主族,A与W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)E元素在周期表中的位置为__________________。写出E的最高价氧化物的水化物与D的最高价氧化物的水化物反应的离子方程式______________________________。
(2)由A、W元素组成的18电子微粒的分子式为____________________。
(3)D的一种氧化物可与B的最高价氧化物反应生成W的单质,试写出反应的化学方程式_______________。
(4)向含有Fe2+和淀粉KI的溶液中滴入A2W2,观察到溶液呈蓝色并有红褐色沉淀生成。当消耗2mol I-时,共转移3mol电子,该反应的离子方程式是_________________。
(5)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,A-具有与He相同的电子层结构,DA能与水反应放氢气,若将1molDA和1molE单质混合加入足量的水,充分反应后生成气体的体积是_________L(标准状况下)。
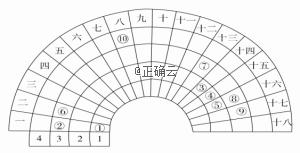
元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是
A.②⑧⑨对应简单离子半径依次减小
B.⑥的氯化物的熔点比⑦的氯化物熔点低
C.元素⑩处于常见周期表第四周期ⅧB族
D.①分别与③④⑤均可形成既含极性键又含非极性键的化合物
反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g)在10L的密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(x)(反应物的消耗速率或产物的生成速率)可表示为( )
A.v(NH3)=0.010mol/(L·s)
B.v(O2)=0.0010mol/(L·s)
C.v(NO)=0.0010mol/(L·s)
D.v(H2O)=0.045mol/(L·s)
下列物质中,能用于厨房除水垢的是
A. 乙醇 B. 乙酸 C. 乙酸乙酯 D. 苯
某元素的微粒37X-的核外电子数为18,则该元素原子的中子数是 ( )
A. 17 B. 18 C. 19 D. 20
验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
| ① | ② | ③ |
|
|
|
|
| 在Fe表面生成蓝色沉淀 | 试管内无明显变化 | 试管内生成蓝色沉淀 |
下列说法不正确的是
A. 对比②③,可以判定Zn保护了Fe
B. 对比①②,K3[Fe(CN)6]可能将Fe氧化
C. 验证Zn保护Fe时不能用①的方法
D. 将Zn换成Cu,用①的方法可判断Fe比Cu活泼
两种气体A、B分别为0.6 mol与0.5 mol。在0.4 L密闭容器中发生反应:3A(g)+B(g) ![]() mC(g)+2D(g),经5 min后达到平衡,此时C为0.2 mol,又知在此反应时间,D的平均反应速率为0.1 mol·(L·min)-1。下列结论正确的是
mC(g)+2D(g),经5 min后达到平衡,此时C为0.2 mol,又知在此反应时间,D的平均反应速率为0.1 mol·(L·min)-1。下列结论正确的是
A. m的值为2 B. 改变压强,该平衡状态发生改变
C. A的平均反应速率为0.1 mol·(L·min)-1 D. 平衡时,反应混合物的总物质的量为1 mol
下列物质性质的变化规律,![]() 与共价键的强弱有关的是 ( )
与共价键的强弱有关的是 ( )
A.F2、Cl2、Br2、I2的熔点、沸点逐渐升高 ![]() B.HF、HCl、HBr、HI的热稳定性依次降低 C.碱金属单质的熔点随原子序数递增依次降低
B.HF、HCl、HBr、HI的热稳定性依次降低 C.碱金属单质的熔点随原子序数递增依次降低
D.NaF、NaCl、NaBr、NaI的熔点依次降低
下列叙述中正确的是
A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数
B.除短周期外,其他周期均有18种元素
C.副族元素中没有非金属元素
D.碱金属元素是指ⅠA族的所有元素
两种微粒含有相同的质子数和电子数,这两种微粒可能是
①互为同位素的两种不同的原子 ②两种不同元素的原子 ③一种原子和一种分子 ④一种原子和一种离子 ⑤两种不同分子 ⑥一种分子和一种离子 ⑦两种不同阳离子 ⑧两种不同阴离子 ⑨一种阴离子和一种阳离子
A.①③⑤⑦⑧ B.①③⑤⑥⑦⑧ C.①③④⑤⑦ D.全部都是
从海带中提取碘单质,成熟的工艺流程如下,下列关于海水制碘的说法中,不正确的是( )

A.实验室在蒸发皿中灼烧干海带,并且用玻璃棒搅拌
B.在含I-的滤液中加入稀硫酸和双氧水后,碘元素发生氧化反应
C.在碘水中加入几滴淀粉溶液,溶液变蓝色
D.在碘水中加入CCl4得到I2的CCl4溶液,该操作为“萃取”
下列属于碱的是
A.NaOH B.CH3COOH C.NH3 D.H2O
- 文化是相对于经济、政治而言的人类全部精神活动及产品。下列属于文化的是 ①物质资料生产方式 ②三个代表重要思想 ③中国古
- “今大道既隐,天下为家,各亲其亲,各子其子,货力为己”文中的“大道”是指( ) ①禅让制
- 右图为某地农业布局和农业产值构成图,读图完成4~5题。 4.该地农业地域类型是 A.大牧场放牧业
- The medical team is made up of 12 people, 4 nurses ______ .
- 高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,其与水的离子反应是4FeO42-+10H2O===4Fe(OH
- 甲物体的质量是乙物体质量的n倍,乙的比热容是甲的K倍,现甲获得的热量是乙获得热量的S倍,则甲物体升高的温度是乙物体升高温
- A、B、C三种元素的原子具有相同的电子层数,而B的核电荷数比A大1,C原子的电子总数比B原子的电子总数多4; 1molA
- 下图所示的化学实验基本操作中,正确的是(▲) A.倾倒液体 B.称量固体 C.检查气密性 D
- (本小题满分12分)已知命题:关于的不等式的解集为;命题:函数的定义域是。若“或”为真命题,“且”为假命题,求实数的取值
- 读下图,分析回答(1)城市化是指 向城市集聚和 地区转变为城市地区的过程。 (2
- 地球上最长的纬线是 A.赤道 B.20°N C.40°N
- 标志着中国结束了靠“洋油”时代的重大事件是( )A.第一个飞机制造厂建成 B.武汉长江大桥
- 依次填入下列各句横线处的词语,恰当的一组是( )①这所古老的建筑正当窗口, 交通。要不要拆除,有关部门正在研究。
- 图7所示的是一种厕所坐便器的自动上水装置示意图。坐便器冲水之后由自来水自动上水,当水箱内的水达到一定深度时,浮标带动杠杆
- 鉴于产品原材料价格上涨、市场供求状况等因素,贵州茅台酒公司决定自2010年1月1日起 适当上调贵州茅台酒出厂价格,平均
- 下列各句中,加点的成语使用恰当的一项是( ) A.有些人拿着纳税人的钱去西方学习,美其名曰“取经”,
- (10分)2010年诺贝尔物理学奖授予英国曼彻斯特大学科学家安德烈·海姆和康斯坦 丁·诺沃肖洛夫,以表彰他们对石墨烯的研
- If you know how to with the seller , you can pay much
- 下列实验操作中,正确的是() A. B. C. D.
- (4分) 儿童缺锌会引起食欲不振、发育不良.右图为某种补锌口服液说明书的一部分.请回答:(1)该口服液中的锌属于 ▲







