原子晶体(共价晶体) 知识点题库
如图所示的是某原子晶体A空间结构的一个单元,A与某物质B反应生成C,其实质是每个A—A键中插入一个B原子,则C物质的化学式为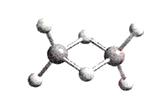
①CO2 ②SiO2 ③晶体Si ④白磷 ⑤氨基乙酸 ⑥固态He
①Al2O3是两性氧化物 ②硬度很大 ③它的熔点为2045℃ ④几乎不溶于水 ⑤自然界中的刚玉有红宝石和蓝宝石
-
(1) LED研究起始于对碳化硅晶体的研究.1907年,英国科学家Henry Joseph Round发现在施加电流时能够在碳化硅晶体中发现发光现象.
(i)碳化硅晶体属于晶体.
(ii)碳化硅的晶胞结构与金刚石的相似,在碳化硅晶体中,碳原子所连接最小的环由个碳原子和个硅原子组成,每个碳原子连接个这样的环.
(iii)碳化硅中,碳原子采取杂化方式,与周围的硅原子形成的键角为.
(iv)请结合原子结构的知识解释发光的原因:.
-
(2) 准现代LED.1962年,GE公司使用磷砷化镓(GaAsxP1﹣x)材料制成了红色发光二极管.这是第一颗可见光LED,被视为现代LED之祖.随后又出现了绿色LED磷化镓(GaP)和黄色LED碳化硅,使光谱拓展到橙光、黄光和绿光.
(i)镓在元素周期表的位置是,其基态原子的价电子排布式为.
(ii)人们发现在磷砷化镓或磷化镓中掺杂氮(利用氮代替磷或砷的位置),可以提高其发光效率.其原因不可能为(多选).
A、氮的半径比磷和砷的半径小,用氮代替部分磷或砷的位置不会影响晶体的构型.
B、N的第一电离能大于磷和砷,容易失去电子,发生电子跃迁.
C、N的电负性大,掺杂后得到的位置中存在氢键.
D、N是与砷、磷具有相同价电子结构的杂质,但对电子束缚能力较磷和砷强,造成等电子陷阱.
-
(3) 1993年,中村修二等人开发出首个明亮蓝光的氮化镓LED.凭借此成就,他获得了2014年诺贝尔物理学奖.
为测试氮化镓绿色LED光强与电流的关系,得到如图,从图中你能得到规律(写一条即可)
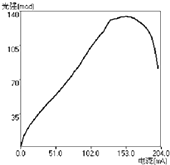
-
(1) C、N、O元素的第一电离能大小为:。
-
(2) Cu的价电子排布式为,基态Fe原子有个未成对电子,Fe3+的价电子排布图为。
-
(3) 基态硫原子中,核外占据最高能级电子的电子云轮廓图形状为。硫的一种同素异形体分子式为S8 , 其结构如图所示,其中S原子的杂化轨道类型为。S8易溶于二硫化碳的原因是。
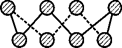
-
(4) 教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
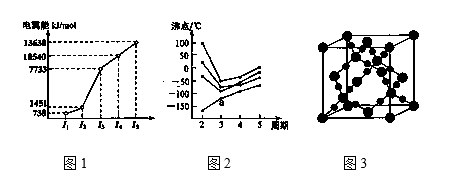
(a)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有种不同运动状态的电子。
(b)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于晶体。
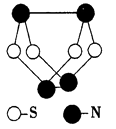
(c)如图2所示,每条折线表示周期表ⅣA到ⅦA 中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是。判断依据。
-
(1) C、O、Si三种元素电负性由大到小的顺序为;第一电离能I1(Si)I1(Ge)(填“>”或“<”)。
-
(2) 基态Ge原子价电子排布式为;SiO2、GeO2具有类似的晶体结构,SiO2熔点较高,其原因是
-
(3) 如图为硼酸晶体的片层结构,其中硼原子的杂化方式为。该晶体中存在的作用力有。
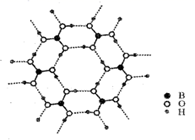
A.共价键 B.离子键 C.氢键
-
(4) Fe和Cu可分别与氧元素形成低价态氧化物FeO和Cu2O。
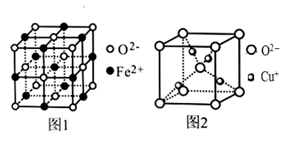
①FeO立方晶胞结构如图1所示,则Fe2+的配位数为。
②Cu2O立方晶胞结构如图2所示,若晶胞边长为acm,则该晶体的密度为g·cm-3。(用含a、NA的代数式表示,NA代表阿伏加德罗常数)
-
(1) A元素原子的半径最大,写出A在元素周期表中的位置,其原子核外电子排布式为,A与上述元素中原子半径最小的元素B形成的化合物晶体类型为。
-
(2) C元素的单质能溶解于C与D形成的化合物中,写出该化合物的分子式,推断该化合物(难、微、易)溶于水。
-
(3) C、D元素均可与B元素形成化合物,此2种化合物都可与水反应形成对应的酸,2种酸的分子式相似,写出2种酸的分子式,简述证明2种酸酸性相对强弱的方法。
Cu2S和CuS均可被KMnO4酸性溶液氧化,在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
①
 + Cu2S +
+ Cu2S +  →
→  + SO2↑ +
+ SO2↑ +  + H2O(未配平)
+ H2O(未配平)②
 + CuS +
+ CuS +  →
→  + SO2↑ +
+ SO2↑ +  + H2O(未配平)
+ H2O(未配平) -
(4) 下列关于反应①的说法中错误的是(选填编号)。
a.还原性的强弱关系是:
 > Cu2S
> Cu2Sb.氧化剂与还原剂的物质的量之比为
c.生成2.24L(标况下)SO2 , 转移电子的物质的量是0.8mol
d.被氧化的元素是正一价的Cu和负二价的S
-
(5) 写出反应②中反应物配平后的系数并标出电子转移方向和数目:
_
 +_CuS +_
+_CuS +_ 
已知:KMnO4在稀硫酸存在下能将H2O2氧化为O2 , KMnO4被还原为
 ;H2O2在前面反应生成
;H2O2在前面反应生成  的催化下能发生分解反应生成H2O和O2。
的催化下能发生分解反应生成H2O和O2。 -
(6) 稀硫酸中,某KMnO4和H2O2发生氧化还原反应方程式如下:
2KMnO4 + 7H2O2 + 3H2SO4 → K2SO4 + 2MnSO4 + 6O2↑ + 10H2O,反应中1mol KMnO4氧化H2O2的物质的量是mol, 反应中的氧化剂是,氧化剂与还原剂的物质的量比为。
 、SO
、SO  为正面体结构,可推测CCl4、PH
为正面体结构,可推测CCl4、PH  、PO
、PO 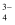 也为正四面体结构
D . C2H6是碳链为直线形的非极性分子,可推测C3H8也是碳链为直线形的非极性分子
也为正四面体结构
D . C2H6是碳链为直线形的非极性分子,可推测C3H8也是碳链为直线形的非极性分子
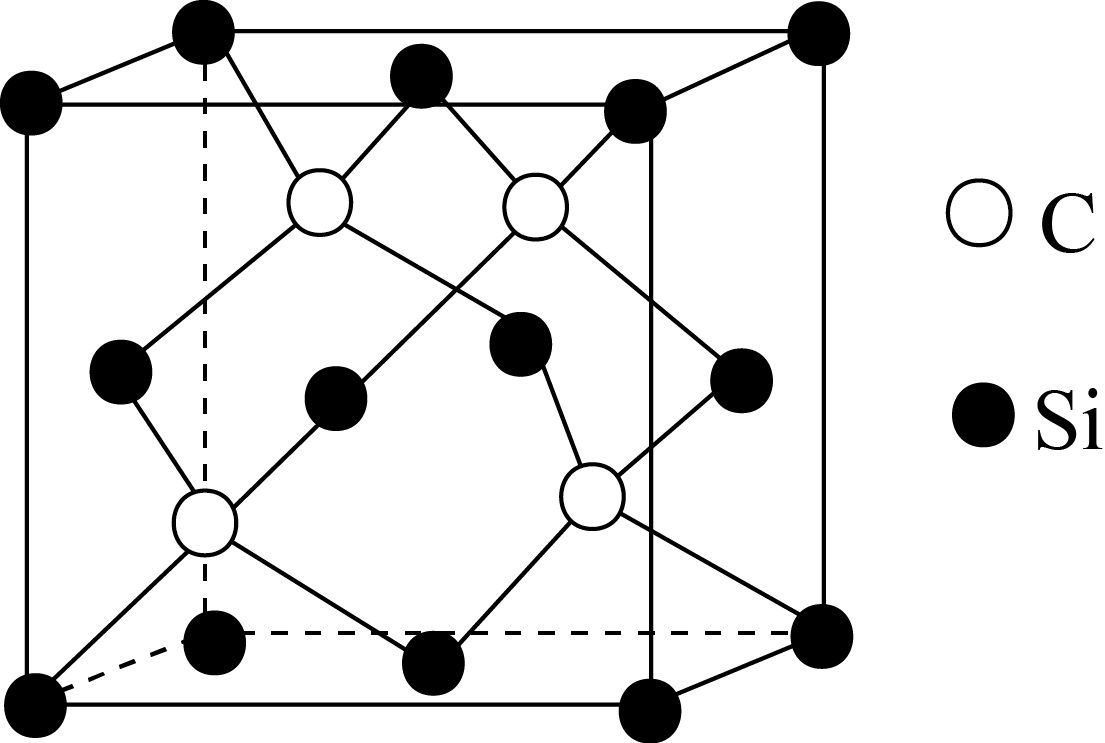
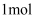 碳化硅中含
碳化硅中含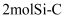 键
D . 碳和硅原子的杂化方式相同
键
D . 碳和硅原子的杂化方式相同
- 下边函数图像描述的是某商品在半年中的价格走势,对该图理解正确的是 ①该商品很可能处于卖方市场 ②该商品的互
- 下列化学式既能表示物质的组成,又能表示物质的一个分子的是( ) A.NaOH B.Si
- 菱形的两条对角线长分别是6和8,则此菱形的边长是() A.10 B.8 C.6 D.5
- 母亲是一棵树…… 要求:扩句,可以写是“一棵柳树”“一棵枣树”“一棵红枫”“一棵冬青”等等。
- 下列叙述正确的是A.因为NH3·H2O是弱碱,所以不能用氨水与FeCl3溶液反应制取Fe(OH)3B.向FeI2溶液中通
- 对生活中下列现象的解释错误的是 现 象 解 释 A 湿衣服在夏天比在冬天干得快 温度升高,分子运动速率加快 B 60
- 补写出下列名篇名句的空缺部分。(只选3小题) (1)俨骖騑于上路, 。临帝子之长洲,
- 下列各组中的离子,能在溶液中大量共存的是 A.H+ Na+ CO32- Cl- B.Ba2+
- . 每年的7月11日被定位“世界人口日”,人口问题越来越受到国际社会的重视,下图表示三种可能的人口增长曲线,下列说法错误
- 双曲线的中心在原点,右焦点为,渐近线方程为 . (Ⅰ)求双曲线的方程; (Ⅱ)设直线:与双曲线交于
- 3月1日,2010年第一期凭证式国债正式开卖。尽管春寒料峭,但国债销售依然火爆,某一银行营业网点几百万元的额度尚未开门即
- )对于,将表示为,当时,当时为0或1,定义如下:在的上述表示中,当,中等于1的个数为奇数时,;否则。 (1)_
- “北风乱/夜未央/你的影子剪不断/徒留我孤单/在湖面/成双/”是《菊花台》中的一段歌词。以下对“成双”的理解,正确的是【
- 甲醇的化学式为CH4O,某甲醇溶液中甲醇所含氢原子数与水所含的氢原子数相等,则该溶液中溶质的质量分数是( ) A.
- 写出的一个同类项_______________________.
- 复方篙甲醚(C16H26O5)是一种治疗疟疾的有效药品.下列说法正确的是() A.复方篙甲醚属于有机物 B.复方篙甲醚由
- 常温下,有甲、乙两份体积为1 L,浓度均为0.1 mol·L-1的醋酸溶液,其pH为3,①甲用蒸馏水稀释100倍后,溶液
- 已知i为虚数单位, 则复数ii在复平面内对应的点位于 ( ) A.第一象限 B.第二象
- 宋代哲学家朱熹在一首题为“泛舟”的小诗里这样写道:“昨夜江边春水生,艨艟巨舰一毛轻,向来枉费推移力,此日中流自在行。”这
- 在R上定义的函数f(x)是偶函数,且f(x)=f(2-x).若f(x)在区间[1,2]上是减函数,则f(x)



