原子晶体(共价晶体) 知识点题库
碳化硅(SiC)晶体有类似金刚石的结构,其中碳原子和硅原子的位置是交替的。它与晶体硅和金刚石相比较,正确的是( )
A . 熔点从高到低的顺序是碳化硅>金刚石>晶体硅
B . 熔点从高到低的顺序是金刚石>晶体硅>碳化硅
C . 三种晶体中的单元都是正四面体结构
D . 三种晶体都是原子晶体且均为电的绝缘体
下列有关物质性质的比较,错误的是( )
A . 溶解度:小苏打 < 苏打
B . 密度:溴乙烷 > 水
C . 硬度:晶体硅 < 金刚石
D . 碳碳键键长:乙烯 > 苯
一定条件下,CO2分子晶体可转化为具有类似SiO2结构的原子晶体.从理论上分析,下列说法正确的是( )
A . 该转化过程是物理变化
B . 1molCO2原子晶体中含2molC﹣O键
C . CO2原子晶体的熔点高于SiO2
D . CO2的原子晶体和分子晶体互为同分异构体
下列关于SiO2和金刚石的叙述正确的是( )
A . SiO2晶体结构中,每个Si原子与2个O原子直接相连
B . 通常状况下,60gSiO2晶体中含有的分子数为NA(NA表示阿伏加德罗常数)
C . 金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子
D . 1mol金刚石含4NAC﹣C键
下列说法中正确的是( )
A . 同族元素的氧化物不可能形成不同类型的晶体
B . SiO2晶体网状结构的最小的环上,Si和O原子数之比为1:2
C . 满足难溶于水,熔点高,固体不导电,熔化时导电的晶体为离子晶体
D . 同分异构体中,燃烧热数值越大,该物质越稳定
硅是构成矿物和岩石的主要成分,单质硅及其化合物具有广泛的用途。完成下列填空:
-
(1) 某些硅酸盐具有筛选分子的功能。一种硅酸盐的组成为:M2O·R2O3·2SiO2·nH2O,已知元素M、R均位于元素周期表的第3周期,两元素原子的质子数之和为24。
①写出M原子核外能量最高的电子的电子排布式:。
②常温下,不能与R单质发生反应的是(选填序号)。
a.CuCl2溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
-
(2) 氮化硅(Si3N4)陶瓷材料硬度大、熔点高。可由下列反应制得:SiO2+C+N2
 Si3N4+CO
Si3N4+CO ①Si3N4中氮元素的化合价为-3,请解释Si3N4中氮元素化合价为负价的原因。
②C3N4的结构与Si3N4相似,请比较二者熔点高低,并说明理由:。
③配平上述反应的化学方程式,并标出电子转移的数目和方向。。
-
(3) 一种用工业硅(含少量铁、铜等金属的氧化物)制备Si3N4的主要流程如下:
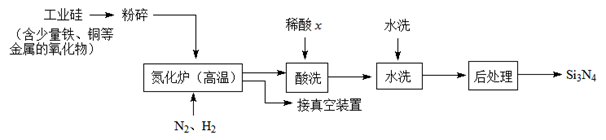
①将工业硅粉碎的目的是。
②适量的H2是为了排尽设备中的空气,但H2在高温下也能还原工业硅中的某些金属化物。
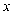 可能是(选填:“盐酸”“硝酸”或“硫酸”),理由是。
可能是(选填:“盐酸”“硝酸”或“硫酸”),理由是。
下列叙述正确的是( )
A . 氯化铯晶体中,每1个Cs+与其他8个Cs+等距离紧邻
B . 金刚石网状结构中,由共价键构成的碳原子环中,最小的环上有4个碳原子
C . 熔点由高到低的顺序是:金刚石>碳化硅>晶体硅
D . PCl3和了BCl3分子中所有原子的最外层都达到8电子稳定结构
下列有关晶体的说法正确的是( )
A . 分子晶体中一定不含离子键
B . 分子晶体中一定含有共价键
C . 离子晶体中一定只含离子键
D . 离子晶体的熔点一定比共价化合物高
下列物质的性质与应用对应关系正确的是( )
| 物质的性质 | 应 用 | |
| A | 次氯酸有酸性 | 可用于漂白、杀菌消毒 |
| B | 纯碱能与酸反应 | 可用作治疗胃酸过多的药物 |
| C | 液氨汽化时要吸收大量的热 | 工业上可用作制冷剂 |
| D | 晶体硅的熔点高、硬度大 | 可用于制作半导体材料 |
A . A
B . B
C . C
D . D
下列描述中正确的是( )。
A . 原子晶体中只含共价键
B . 离子晶体中只含离子键,不含有共价键
C . 分子晶体中只存在分子间作用力,不含其它化学键
D . 任何晶体中,若含阳离子也一定还有阴离子
下列关于晶体的说法中,错误的是( )
①晶体中原子呈周期性有序排列,有自范性;而非晶体中原子排列相对无序,无自范性 ②含有金属阳离子的晶体一定是离子晶体 ③共价键可决定分子晶体的熔、沸点 ④MgO的晶格能远比NaCl大,这是因为前者离子所带的电荷数多,离子半径小 ⑤晶胞是晶体结构的基本单元,晶体内部的微粒按一定规律作周期性重复排列 ⑥晶体尽可能采取紧密堆积方式,以使其变得比较稳定 ⑦干冰晶体中,一个CO2分子周围有12个CO2分子紧邻;CsCl和NaCl晶体中阴、阳离子的配位数都为6
A . ①②③
B . ②③④
C . ④⑤⑥
D . ②③⑦
共价键、离子键和范德华力是粒子之间的三种作用力。下列晶体①Na2O2、②SiO2、③石墨、④金刚石、⑤NaCl、⑥白磷中,含有以上其中两种作用力的是( )
A . ①②③
B . ①③⑥
C . ②④⑥
D . ①②③⑥
下列推测正确的是( )
A . Mg2+半径比Ca2+半径小,可推测金属镁的熔点比钙的低
B . Si原子半径比Ge原子半径小,可推测晶体硅的硬度大于晶体锗
C . 某物质在熔融状态下能导电,可推测该物质在固态时为离子晶体
D . N-H键比P-H键牢固,可推测NH3的沸点高于PH3
下列说法正确的是( )
A . 金刚石与碳化硅晶体结构相似.金刚石的硬度小于碳化硅
B . PH3和NH3分子中均含有孤电子对,且NH3提供孤电子对的能力强于PH3
C . BeO的晶格能大于MgO,可推测BeCO3的分解温度低于MgCO3
D . 向1mol[Cr(H2O)4Cl2]Cl中加入足量AgNO3溶液,可以得到3mol AgCl沉淀
下列物质的性质变化规律与与键能无关的是( )
A . 与硅相比,金刚石的硬度大、熔点高
B . HF、HCl、HBr、HI热稳定性依次减弱
C . F2、Cl2、Br2、I2的沸点逐渐升高
D . H2、O2、H2S在水中的溶解性依次为难溶、微溶、可溶
石墨晶体的层状结构如图所示。下列说法正确的是( )
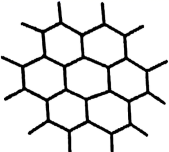
A . 石墨晶体只有分子晶体和原子晶体的特征
B . 石墨中碳原子数和C-C个数之比为1:2
C . 每个六元环完全占有的碳原子数是3
D . 石墨中的C原子均为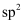 杂化
杂化
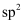 杂化
杂化
下列是典型晶体的结构示意图,从①到⑥对应正确的是( )
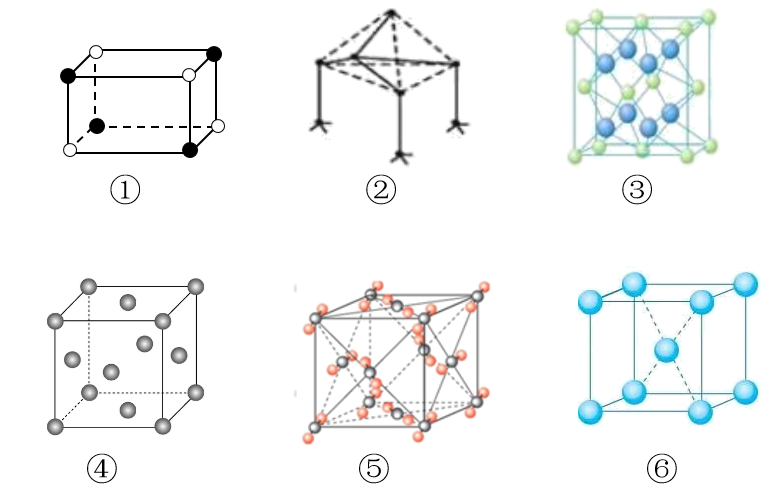
A . CsCl 金刚石 CaF2 Cu CO2 Fe
B . CaF2 SiC 金刚石 Cu CO2 CsCl
C . NaCl 单质硅 CaF2 Au CO2 K
D . NaCl BN Au CaF2 CO2 Na
石墨晶体是层状结构。以下有关石墨晶体的说法正确的有( )
①石墨晶体只有分子晶体和共价晶体的特征;②石墨是混合型晶体;③石墨中碳原子数和C-C键个数之比为1:2;④石墨和金刚石的硬度相同;⑤石墨层内碳原子核间距比金刚石碳原子核间距大;⑥石墨的导电性只能沿着石墨平面的方向
A . 2项
B . 3项
C . 4项
D . 5项
关于反应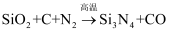 (未配平),下列说法错误的是( )
(未配平),下列说法错误的是( )
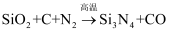 (未配平),下列说法错误的是( )
(未配平),下列说法错误的是( )
A .  既不是氧化剂也不是还原剂
B . 氧化剂与还原剂的物质的量之比为
既不是氧化剂也不是还原剂
B . 氧化剂与还原剂的物质的量之比为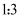 C .
C .  具有耐高温耐磨等特点
D . 每转移
具有耐高温耐磨等特点
D . 每转移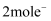 , 产生
, 产生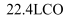 气体
气体
 既不是氧化剂也不是还原剂
B . 氧化剂与还原剂的物质的量之比为
既不是氧化剂也不是还原剂
B . 氧化剂与还原剂的物质的量之比为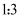 C .
C .  具有耐高温耐磨等特点
D . 每转移
具有耐高温耐磨等特点
D . 每转移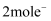 , 产生
, 产生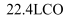 气体
气体
BeCl2熔点较低,易升华,溶于醇和醚,其化学性质与AlCl3相似。由此可推测BeCl2( )
A . 熔融态不导电
B . 水溶液呈中性
C . 熔点比BeBr2高
D . 不与氢氧化钠溶液反应
最近更新
- 下列词语中加点字的读音全都正确的一组是( ) A.纰漏( bǐ ) 炽热(zhì) 供销社(gōng
- 2010年广州亚运会的足球赛时,球员踢球瞬间,在突触小体上完成的信息转换模式为() A.电信号→电信号 B.电信号→化学
- 在并联电路中,下列哪个说法是正确的A.电阻越大的支路,电流越大B.电阻越大的支路,两端的电压越大C.各支路中消耗的电功率
- 用如图19所示的滑轮组将重3×103N的物体匀速提高2m,拉力所做的功为104J,所用的时间为100s。求:(6分)(1
- 下列关于小康社会的建设,说法正确的是( ) ①
- 某工厂排出的废水,经测定含0.012mol·L-1的游离Br2和8×10-4mol·L-1的H+离子。若用加Na2SO3
- 美丽的鲜花是由什么发育成的?
- 关于平原和山区公路建设的叙述,不正确的是
- 下列取代基或微粒中,碳原子都满足最外层为8电子结构的是A.乙基(—CH2CH3) B.碳正
- (10分) 如图所示,半径为R的圆盘绕垂直于盘面的中心轴匀速转动,其正上方h处沿OB方向水平抛出一小球,要使球与盘只碰一
- 将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )A.两烧杯中铜片表面均无气泡产生
- 下列化学反应中属于分解反应的是 A、高锰酸钾—加热→ 锰酸钾+二氧化锰+氧气 B、甲烷+氧气—点燃→水+二氧化碳
- 下面加点字的注音有误的一项是( ) A.楠木(nán) 陆蠡(lí) 淅沥(xī) 馨香(xī
- 下列物态变化的过程中,吸收热量的是: (1)春天,冰雪融化 (2)夏天,从冰箱里面拿出来的饮料罐“出汗
- 下列各句中,加点的词语运用错误的一项是( ) A.去年相继发生的“天安舰”事件、延坪岛炮击事件并导
- .......
- 补写出下列名、句名篇中的空缺部分(10分) 17.时维九月,序属三秋。_____________,___________
- 有人认为,博客完全属于自己的地盘,用户把日记搬到网上,并拥有管理权,任何人都不可以干涉。这一观点 (
- (CN)2、(SCN)2、(OCN)2称“类卤素”,与卤素单质的性质相似,而其阴离子性质也相似,如:2Fe+3(SCN)
- ,杨花愁杀渡江人。



