原子晶体(共价晶体) 知识点题库
①SiC是 晶体,键角是 .
②如果我们以一个硅原子为中心,设SiC晶体中硅原子与其最近的碳原子的最近距离为d,则与硅原子次近的第二层有 个原子,离中心原子的距离是
A.干冰B.金刚石C.氦D.过氧化钠E.二氧化硅F.氯化铵
(1)通过极性键形成的原子晶体是: .
(2)由分子直接构成的晶体是: .
(3)含有离子键、共价键、配位键的化合物是: .
(4)含有非极性键的离子化合物是: .
(5)已知微粒间的作用力包括离子键、共价键、金属键、范德华力、氢键.氯化钠熔化,粒子间克服的作用力为 ;二氧化硅熔化,粒子间克服的作用力为 ;干冰气化,粒子间克服的作用力为
(1)其中代表金刚石的是(填编号字母) ,
(2)其中表示NaCl的是(填编号字母) ,
(3)代表CsCl的是 ,它属于 晶体,
(4)代表干冰的是(填编号字母) ,它属于 晶体,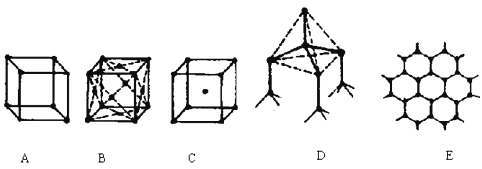
-
(1) 写出上述制备硅的化学反应方程式
-
(2) 二氧化硅与二氧化碳物理性质差别很大,原因是
-
(3) 盐X的溶液能与Al2(SO4)3溶液反应生成一种白色沉淀和气体.写出此反应的离子反应方程式
-
(1) 下列是钠、碘、金刚石、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是;(请用相应的编号填写)
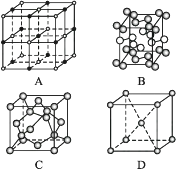
-
(2) 已知:晶体二氧化硅可由晶体硅衍生得到;下图是晶体硅及二氧化硅的晶胞示意图:
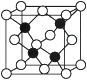
图1 晶体Si的晶胞
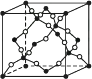
图2 晶体SiO2的晶胞
由图示可知两者形成的晶体的类型是,请写出与晶体SiO2化学键及晶体类型完全相同的两种物质的名称:;
-
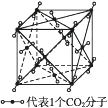
(3) 干冰晶体是一种面心立方结构,如图所示,即每8个CO2构成立方体,且在6个面的中心上又各有1个CO2分子,在每个CO2周围紧邻(其中a为立方体棱长)的CO2有个。
 。上述反应中的物质涉及的晶体类型共有( )
。上述反应中的物质涉及的晶体类型共有( )
 只与2个价电子存在强烈的相互作用
B . 在二氧化硅晶体中,原子未排列成紧密堆积结构的原因是共价键具有方向性和饱和性
C . 熔点为2700℃,导电性好、延展性强的晶体一定是共价晶体
D . 离子晶体中晶格能的大小仅与阴、阳离子之间的距离有关
只与2个价电子存在强烈的相互作用
B . 在二氧化硅晶体中,原子未排列成紧密堆积结构的原因是共价键具有方向性和饱和性
C . 熔点为2700℃,导电性好、延展性强的晶体一定是共价晶体
D . 离子晶体中晶格能的大小仅与阴、阳离子之间的距离有关
-
(1) 基态N原子的价层电子排布图为。
-
(2) 上述物质中所含第二周期元素的第一电离能由大到小的顺序为(填元素符号,下同),电负性由大到小的顺序为。
-
(3) 氨硼烷(NH3·BH3)是一种具有潜力的固体储氢材料。NH3·BH3分子中属于sp3杂化的原子有(填元素符号)。H—N—H键角:NH3NH3·BH3(填“>”“<”或“=”),理由是。
-
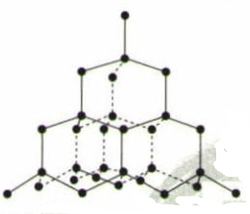
(4) 已知:BC(碳化硼)、BN(氮化硼)的熔点依次为2450℃、3000℃, BN的熔点较高的主要原因是。
-
(5) 已知TiO2的晶胞如图1所示,“黑球”代表 (填“钛”或“氧")。
-
(6) 钛晶体有两种结构,如图2和图3所示。
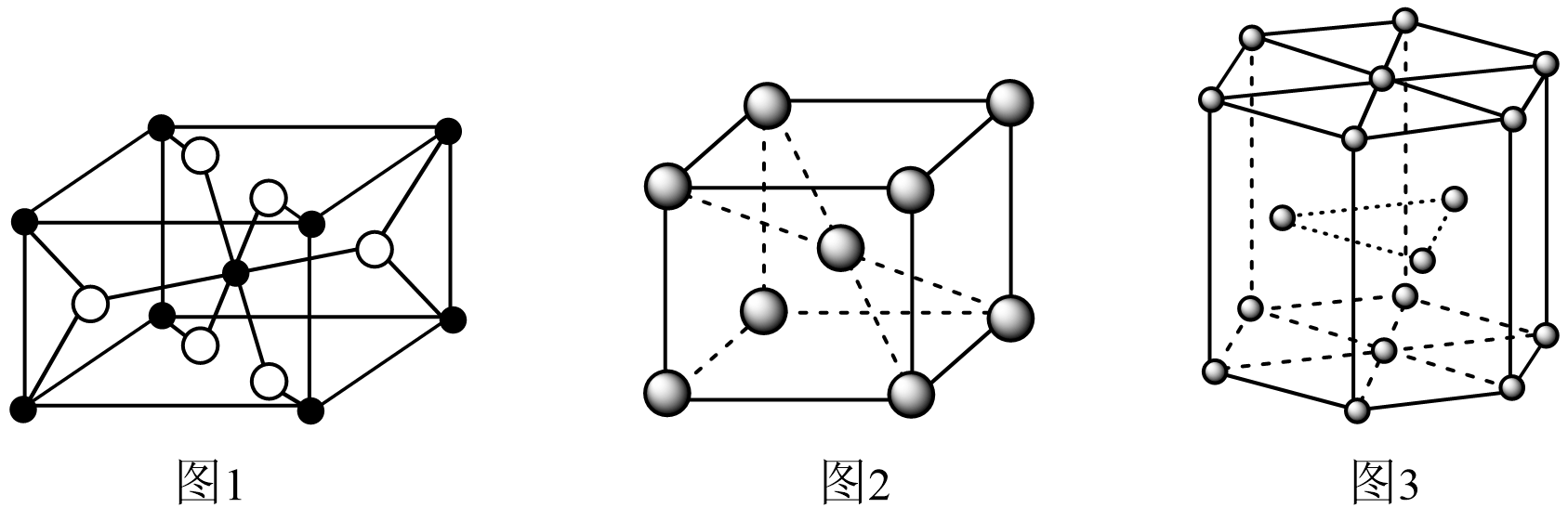
图2结构中空间利用率(φ)为 (用含π的代数式表示);已知图3结构中底边长为a nm,高为c nm,NA代表阿伏加德罗常数的值,则该钛晶体的密度为g·m-3(用含a、c、NA的代数式表示)。
A.干冰 B.金刚石 C.氦 D.过氧化钠 E.二氧化硅 F.溴化铵 G. H2O2 H.氢氧化钠
-
(1) 通过非极性键形成的原子晶体是:。
-
(2) 含有极性键的离子化合物是:。
-
(3) 含有离子键、共价键、配位键的化合物是:。
-
(4) A,B,C,D四种物质的熔点从低到高的顺序为。
①SiO2和SO3 ②金刚石和白磷 ③CO2和SO2 ④晶体硅和金刚石⑤晶体氖和晶体氮 ⑥硫黄和单质碘
 。下列说法正确的是( )
。下列说法正确的是( )
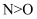 B .
B .  分子中C原子为
分子中C原子为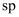 杂化
C . 单质硫属于共价晶体
D .
杂化
C . 单质硫属于共价晶体
D . 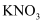 中化学键只有
中化学键只有 键
键
- 中华民族的发明创造为人类文明进步做出了巨大贡献.下列不涉及化学变化的是() A. 侯氏制碱 B. 蚕丝纺织
- 如图1,2015年 12月11日,市民戴着口罩在合肥天鹅湖边散步。当日凌晨合肥空气质量污染指数以294排行全国城市第一。
- 作文。(1)阅读下面的文字,根据要求写一篇不少于800字的文章。自由开放的网络,风起云涌的媒体选秀,低门槛、快速度,犹如
- 取植物材料观察细胞的有丝分裂得到右图示,对其分析不正确的是 A.CD段染色体的数目不发生变化 B.处于AC时期的细胞远多
- 在长为12cm的线段AB上任取一点M,并以线段AM为边作正方形,则这个正方形的面积介于36cm2与81cm2之间的概率
- 等差数列{an}中,an≠0,n∈N*,有2a3-a72+2a11=0,数列{bn}是等比数列,且b7=a7,则b6b8
- 美国航空航天局(NASA)于2009年2月11日晚宣布,美国一颗通信卫星10日与一颗已报废的俄罗斯卫星在太空中相撞,撞击
- 一个质量不计的轻弹簧,竖直固定在水平桌面上,一个小球从弹簧的正上方竖直落下,从小球与弹簧接触开始直到弹簧被压缩到最短的过
- 若,则的值是( ) A. B. C. D.
- 下列图片中,能反映罗斯福为摆脱经济危机而采取的增加就业、扩大内需的措施有 A.①③
- 甲比乙大岁的意义是 .
- 阅读顾振威的《带着感激上路》一文,完成19—22题。(16分) ①上初三时,我常常迟到。我的迟到与羊有关。每天上学时,我
- 两个伏特表V1和V2是由完全相同的电流表改装而成.V1的量程是5 V,V2的量程是15 V,为了测量15—20 V的电压
- We areat your service. Don’t ________ to turn to us if you
- I have no dreams ____ to have a happy life. A. rather than
- 下列 词语中加点的字,读音全部相同的一组是 A.围歼信笺缄默草菅人命兼收并蓄 B.汲取亟待慰藉嫉恶如仇估屈聱牙 C.惬意
- Cheating can happenin a lot of different ways. When people c
- 阅读下图,回答问题。 (1)从自然环境角度,评价两河通航的优势。 (2)简要说明荷兰鹿特丹港成为世界级大港的社会经济
- 如图,该程序运行后的输出结果为() A. 0 B. 3 C. 12 D. ﹣2
- 如图,为⊙的直径,弦于点,已知,则⊙的半径为 .



