极性分子和非极性分子 知识点题库
已知N、P同属元素周期表的ⅤA族元素,N在第二周期,P在第三周期,NH3分子呈三角锥形,N原子位于锥顶,三个H原子位于锥底,N—H键间的夹角是107°。
-
(1) PH3分子与NH3分子的构型关系是(填“相同”“相似”或“不相似”), 填“有”或“无”)P—H键,PH3分子是(填“极性”或“非极性”)分子。
-
(2) NH3和PH3相比,热稳定性更强的是 , 原因 。
-
(3) NH3和PH3在常温、常压下都是气体,但NH3比PH3易液化,其主要原因是( )。A . 键的极性N—H比P—H强 B . 分子的极性NH3比PH3强 C . 相对分子质量PH3比NH3大 D . NH3分子之间存在特殊的分子间作用力
均由两种短周期元素组成的A、B、C、D化合物分子,都含有18个电子,它们分子中所含原子的数目依次为2、3、4、6。A和C分子中的原子个数比为1:1,B和D分子中的原子个数比为1:2。D可作为火箭推进剂的燃料。请回答下列问题。
-
(1) A、B、C、D分子中相对原子质量较大的四种元素第一电离能由大到小排列的顺序为(用元素符号回答)。
-
(2) A与HF相比,其熔、沸点较低,原因是。
-
(3) B分子的立体构型为形,该分子属于分子(填“极性”或“非极性”)。由此可以预测B分子在水中的溶解度较(“大”或“小”)。
-
(4) A、B两分子的中心原子的最高价氧化物对应的水化物的酸性强弱为(填化学式)。
若设A的中心原子为X,B的中心原子为Y,比较下列物质的酸性强弱(填“>”“<”或“=”):
HXOHXO3HXO4;
H2YO3H2YO4。
-
(5) D分子中心原子的杂化方式是,由该原子组成的单质分子中包含个π键,与该单质分子互为等电子体的常见分子的分子式为。
下列各组物质中,都是由极性键构成的极性分子的一组是( )
A . CH4和Br2
B . NH3和H2O
C . H2S和CCl4
D . CO2和HCl
下列叙述正确的是( )
A . C2H2分子内含有极性键,但C2H2分子是非极性分子
B . 分子晶体、原子晶体一定含有共价键,离子晶体一定含有离子键
C . 气态氢化物的稳定性随着其相对分子量的增大而增强
D . 某非金属元素从游离态变成化合态时,该元素一定被还原
下列有关分子结构与性质的叙述中正确的是( )
A . CS2、H2O、C2H2都是直线形分子
B . 非极性键只存在于双原子的单质分子(如Cl2)中
C . CH2=CH2和CH≡CH分子中含有的π键个数相等
D . CH4、CCl4、SiH4都是含有极性键的非极性分子
已知PCl3的熔点为﹣93.6℃,沸点为76.1℃,露置于空气中有白雾生成.下列叙述正确的是( )
A . PCl3属于离子晶体
B . PCl3中心磷原子为sp2杂化
C . PCl3分子属于非极性分子
D . PCl3水解可以生成盐酸
常温下S2Cl2是橙黄色液体,其分子结构如图所示.少量泄漏会产生窒息性气味,遇水易水解,并产生酸性悬浊液.下列关于S2Cl2的说法错误的是( )
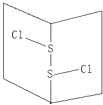
A . 为非极性分子
B . 分子中既含有极性键又含有非极性键
C . 与S2Br2结构相似,熔沸点S2Br2>S2Cl2
D . 与水反应的化学方程式可能为2S2Cl2+2H2O→SO2↑+3S↓+4HCl
氯仿 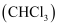 常因保存不慎而被氧化,产生剧毒物光气
常因保存不慎而被氧化,产生剧毒物光气 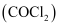 :
: 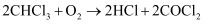 ,下列说法错误的有
,下列说法错误的有 

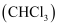 常因保存不慎而被氧化,产生剧毒物光气
常因保存不慎而被氧化,产生剧毒物光气 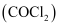 :
: 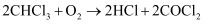 ,下列说法错误的有
,下列说法错误的有 

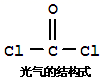
A . 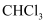 分子为含极性键的非极性分子
B .
分子为含极性键的非极性分子
B . 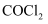 分子中含有3个
分子中含有3个  键、一个
键、一个  键,中心C原子采用
键,中心C原子采用 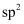 杂化
C .
杂化
C . 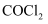 分子中所有原子的最外层电子都满足8电子稳定结构
D . 使用前可用硝酸银稀溶液检验氯仿是否变质
分子中所有原子的最外层电子都满足8电子稳定结构
D . 使用前可用硝酸银稀溶液检验氯仿是否变质
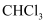 分子为含极性键的非极性分子
B .
分子为含极性键的非极性分子
B . 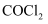 分子中含有3个
分子中含有3个  键、一个
键、一个  键,中心C原子采用
键,中心C原子采用 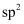 杂化
C .
杂化
C . 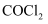 分子中所有原子的最外层电子都满足8电子稳定结构
D . 使用前可用硝酸银稀溶液检验氯仿是否变质
分子中所有原子的最外层电子都满足8电子稳定结构
D . 使用前可用硝酸银稀溶液检验氯仿是否变质
关于CO2说法正确的是( )
A . 碳原子采取sp3杂化
B . CO2是直线形结构
C . C-O键为非极性键
D . CO2为极性分子
下列分子中,属于含有极性键的非极性分子的是( )
A . C2H4
B . H2S
C . Cl2
D . NH3
-
(1) ①为了纪念元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。Fe在元素周期表中的位置为。科学家在研究金属矿物质组分的过程中。发现了Cu-Ni-Fe等多种金属互化物。确定某种金属互化物是晶体还是非晶体的方法是。
②已知:r(Fe2+)为61 pm,r(Co2+)为65 pm。在隔绝空气条件下分别加热FeCO3和CoCO3 , 实验测得FeCO3的分解温度低于CoCO3 , 原因是。
③下表是Fe和Cu的部分电离能数据,请解释I2(Cu)大于I2(Fe)的主要原因是。
元素
Fe
Cu
第一电离能I1/kJ·mol-1
759
746
第一电离能I2/kJ·mol-1
1561
1958
-
(2) 原子序数依次增大的五种元素A、B、C、D、E分别处于第一至第四周期,A是前四周期中原子半径最小的元素,B原子核外电子有6种不同的运动状态,常温下C的单质是空气中含量最多的成分,D最高价氧化物对应水化物的酸性最强,E的基态原子的最外能层只有一个电子,其他能层均已充满电子。请回答下列问题:
①B2A2的电子式是,D所在主族的前四种元素分别与A形成的化合物,其共价键的极性由强到弱的顺序是(填化学式)。
②A和C形成的简单化合物遇到D单质出现白烟现象,写出有关反应的化学方程式为。
③向E的硫酸盐溶液中滴加过量氨水,观察到的现象是首先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液,请写出最后-步得到深蓝色透明溶液对应的离子方程式。
-
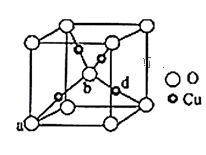
(3) 铜与氧元素可形成如图所示的晶胞结构,其中Cu均匀地分散在立方体内部,a、b的坐标参数依次为(0,0,0)、(
 ,
,  ,
,  ),则d的坐标参数为,已知该品体的密度为ρg/cm3 , NA是阿伏加德罗常数值,则晶胞参数(晶胞棱长)为cm(列出计算式即可)。
),则d的坐标参数为,已知该品体的密度为ρg/cm3 , NA是阿伏加德罗常数值,则晶胞参数(晶胞棱长)为cm(列出计算式即可)。
关于 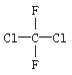 (商品名称为氟利昂-12)的叙述正确的是( )
(商品名称为氟利昂-12)的叙述正确的是( )
 (商品名称为氟利昂-12)的叙述正确的是( )
(商品名称为氟利昂-12)的叙述正确的是( )
A . 有两种同分异构体
B . 只有一种结构
C . 是平面型分子
D . 是非极性分子
一百多年来,科学家首次合成甲二醇(HOCH2OH)。下列有关甲二醇的说法正确的是( )
A . 甲二醇分子是非极性分子
B . 甲二醇易溶于水
C . 1mol甲二醇分子中含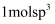 杂化的原子
D . 键能大小决定甲二醇的熔点和沸点
杂化的原子
D . 键能大小决定甲二醇的熔点和沸点
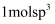 杂化的原子
D . 键能大小决定甲二醇的熔点和沸点
杂化的原子
D . 键能大小决定甲二醇的熔点和沸点
下列说法正确的是( )
A . NCl3常用于漂白,是由极性键构成的非极性分子
B . 氮族元素气态氢化物NH3、PH3、AsH3的键角逐渐减小
C . CH3Cl分子和COCl2分子中,中心C原子均采用sp3杂化
D . 元素M的基态原子的核外电子排布式为 , M是一种过渡元素
, M是一种过渡元素
 , M是一种过渡元素
, M是一种过渡元素
实验室制备Na2S2O3的反应原理:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2。下列有关说法正确的是( )
A . SO2为非极性分子
B . Na2S的电子式为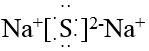 C .
C .  为三角锥形
D . 基态O原子的轨道表示式:
为三角锥形
D . 基态O原子的轨道表示式: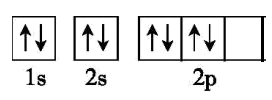
 为三角锥形
D . 基态O原子的轨道表示式:
为三角锥形
D . 基态O原子的轨道表示式:
化合物M(NH4CuSO3)为难溶于水的白色固体,取少量M进行如下实验,下列推断正确的是( )
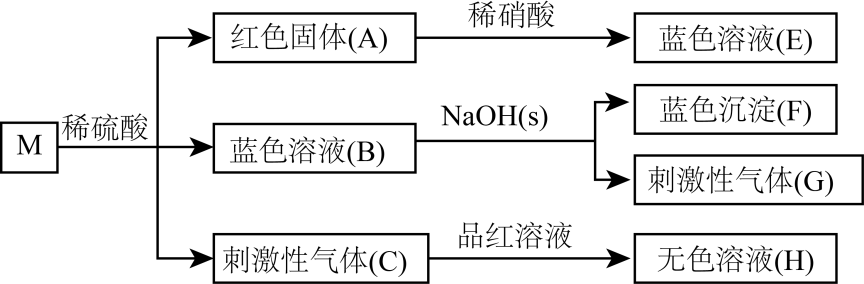
A . 化合物M中Cu的化合价为+2价
B . 红色固体(A)为氧化铜
C . G为含极性共价键的极性分子
D . 加热H无明显现象
镍钴锰三元材料LiNixCoyMnzO2是一类新型锂离子电池正极材料,具有容量高、循环稳定性好等优点。
-
(1) 锰元素基态原子的电子排布式为,镍钴锰三种基态原子中未成对电子数最多的是。
-
(2) 镍可以形成多种配合物,如Ni(CO)4、[Ni(NH3)6]SO4等。
①上述两种配合物都存在的化学键的是
a. 离子键 b. 配位键 c. 极性键 d. 非极性键。
②Ni(CO)4常温下难溶于水,易溶于CCl4中,可推知其为。(填“极性分子”或“非极性分子”)
③[Ni(NH3)6]SO4中阴离子的空间构型为。
-
(3) MnO和CoO具有相同的晶体构型,其熔点大小顺序为
-
(4) 锂离子电池目前广泛采用溶有LiPF6的碳酸酯作为电解液。
①LiPF6各元素的第一电离能从大到小的顺序为。
②常见溶剂碳酸乙烯酯(
 )中碳原子的杂化方式是。
)中碳原子的杂化方式是。 -
(5) LiCoO2的晶胞是六棱柱,其结构如图所示,镍钴锰三元材料中Ni和Mn取代了部分Co的位置:
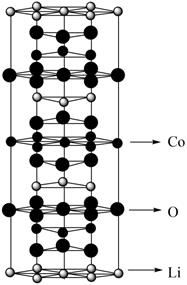
晶胞中含Li原子数为,若晶胞的底边边长为a nm,高为c nm,x:y:z=1:1:1,则LiNixCoyMnzO2晶胞的密度为g/cm3(列出计算式)。
反应SiO2+4HF=SiF4↑+2H2O可用于雕刻玻璃。下列有关说法正确的是( )
A . Si在周期表中位于第3周期VIA族。
B . HF的的电子式为H:F
C . SiF4是非极性分子
D . H2O中氧原子轨道杂化类型为sp2
我国科学家发现一种名为“Methanoliparia”的微生物,能以石油为食物产生甲烷和二氧化碳。下列不属于甲烷和二氧化碳共性的是( )
A . 非电解质
B . 非极性分子
C . 温室气体
D . 平面型分子
尿素,又称碳酰胺,其合成原理为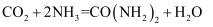 。下列说法正确的是( )
。下列说法正确的是( )
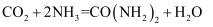 。下列说法正确的是( )
。下列说法正确的是( )
A .  是含有极性键的极性分子
B .
是含有极性键的极性分子
B . 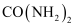 的核磁共振氢谱图中只有一组吸收峰
C .
的核磁共振氢谱图中只有一组吸收峰
C .  分子中氮原子采取
分子中氮原子采取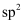 杂化
D .
杂化
D . 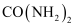 与氰酸铵(
与氰酸铵( )互为同分异构体,组成晶体微粒中作用力类型相同
)互为同分异构体,组成晶体微粒中作用力类型相同
 是含有极性键的极性分子
B .
是含有极性键的极性分子
B . 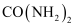 的核磁共振氢谱图中只有一组吸收峰
C .
的核磁共振氢谱图中只有一组吸收峰
C .  分子中氮原子采取
分子中氮原子采取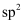 杂化
D .
杂化
D . 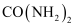 与氰酸铵(
与氰酸铵( )互为同分异构体,组成晶体微粒中作用力类型相同
)互为同分异构体,组成晶体微粒中作用力类型相同
最近更新
- 下列选项中不属于化学研究的是( ) A、研发氢能源 B、合成新材料 C、编写电脑程序 D、用石油生产化工
- 如图,在矩形ABCD中,AB=4,AD=6,M,N分别是AB,CD的中点,P是AD上的点,且∠PNB=3∠CBN. (1
- 下图是生物膜的流动镶嵌模型及物质跨膜运输示意图,其中离子通道是一种通道蛋白,是横跨磷脂分子 层的亲水性通道,允许适当大小
- 下列没有错别字的一项是 A.据世界杯组委会提供的材料,德国队和苏格兰裁判在世界杯上颇有一段渊原。 B.仪征市充分利用本地
- Why not ________ an order ________ a TV set of this new type
- 某化学兴趣小组进行铁生锈的实验探究活动.[探究一]铁生锈的条件 (1)该兴趣小组将洁净无锈的铁钉分别置于如图所示装置中,
- 函数 ,若f(1)+f(a)=2,则a的所有可能值为( )A.1 B.- C.1, - D.1,
- 乙肝疫苗的接种需在一定时期内间隔注射三次,其目的是 A.使机体积累更多数量的疫苗 B.使机体产生更多种类的淋巴细胞 C.
- 小红家电能表上标有“220V,10A”字样,她家原有用电器的总功率是1500W,最近新买了一个电热水器,铭牌上,部分数据
- 翻译句子 1.我昨天花了20分钟在字典里查这些单词。 I spent twenty minutes _________
- 从自然菌样筛选较理想生产菌种的一般步骤是:采集菌样→富集培养→纯种分离→性能测定。(1)不同微生物的生存环境不同,获得理
- 如图1-5,已知△ABC中,AD是BC边上的中线,E是AD的中点.BE的延长线交AC于点F,求证:AF=AC.图1-5
- 按要求补写出下列名篇名句中的空缺部分。(两题任选一题)(5分)(1)外无期功强近之亲,_______________ ,
- 生活中有着各种各样的桥。通道上,石桥、板桥、人行天桥;公园里,廊桥、花桥、九曲桥;以至编结人际关系,缔结美好情缘的“心桥
- 下列有关镁和铝的叙述,正确的是( )A.因为铝可失去3个电子,镁只失去2个电子,故铝比镁活泼B.铝的原子半径及离子
- 2010年7月22日,冯小刚执导的《唐山大地震》震撼上映。这部电影所展示出的唐山人民战胜灾害,重建家园的坚韧、乐观、向上
- 1.下列词语中加点的字,每对读音都不相同的一组是() A.通缉/编辑部 胡诌/邹衍 吁请/长吁短叹 结实/相互攻讦
- 下列说法中正确的是:() A.只要物体吸收了热量,温度就一定会升高 B.只要物体的温度升高,物体就一定吸热 C.只要物体
- Have you ever received a gift that was so clearly not your t
- 设A(x1,y1),B(x2,y2)是椭圆=1(a>b>0)上的两点,已知向量m() ,n(),若m·n=0



