极性分子和非极性分子 知识点题库
-
(1) 一定条件下给水施加一个弱电场,常温常压下水结成冰,俗称“热冰”,其计算机模拟图如图.

采用“弱电场”的条件使水结成“热冰”,说明水分子是 分子(填“极性”或“非极性”).请你展开想象,给“热冰”设计一个应用实例
-
(2) 用高能射线照射液态水时,一个水分子能释放出一个电子,同时产生一种阳离子.
①释放出来的电子可以被若干水分子形成的“网”捕获而形成水合电子,你认为水分子间能形成“网”的原因是 .
②由水分子释放出电子时产生的一种阳离子具有较强的氧化性,试写出该阳离子与SO2的水溶液反应的离子方程式 ;该阳离子还能与水分子作用生成羟基,经测定此时的水具有酸性,写出该过程的离子方程式
-
(3) 写出元素组成与水相同的物质W的电子式 ,写出W与FeCl2在酸性溶液中反应的离子方程式
-
(4) 水溶液中存在H3O+离子,写出该微粒的结构式 (标出配位键).
-
(1) 下列有关石墨烯说法正确的是________________。A . 键长:石墨烯>金刚石 B . 石墨烯分子中所有原子可以处于同一平面 C . 12g石墨烯含
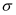 键数为NA
D . 从石墨剥离得石墨烯需克服石墨层与层之间的分子间作用力
键数为NA
D . 从石墨剥离得石墨烯需克服石墨层与层之间的分子间作用力
-
(2) 化学气相沉积法是获得大量石墨烯的有效方法之一,催化剂为金、铜、钴等金属或合金,含碳源可以是甲烷、乙炔、苯、乙醇或酞菁等中的一种或任意组合。
①铜原子在基态时,在有电子填充的能级中,能量最高的能级符号为;第四周期元素中,最外层电子数与铜相同的元素还有。
②乙醇的沸点要高于相对分子质量比它还高的丁烷,请解释原因。
③下列分子属于非极性分子的是。
a.甲烷 b.二氯甲烷 c.苯 d.乙醇
④酞菁与酞菁铜染料分子结构如图,酞菁分子中碳原子采用的杂化方式是;酞菁铜分子中心原子的配位数为。
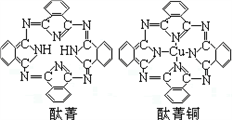
⑤金与铜可形成的金属互化物合金(如图,该晶胞中,Au占据立方体的8个顶点):
它的化学式可表示为;在Au周围最近并距离相等的Cu有个,若2个Cu原子核的最小距离为d pm,该晶体的密度可以表示为g/cm3。(阿伏加德罗常数用NA表示)
反应:P4+ NaOH+H2O→ NaH2PO2 +PH3(未配平)制得的次磷酸钠(NaH2PO2)可作食品防腐剂,也可用于化学镀镍。
请回答下列问题:
-
(1) 磷原子的核外电子排布式:;磷原子核外有种能量不同的电子。
-
(2) 上述反应的反应物和生成物中含有非极性键的分子是。(写出物质的化学式)
-
(3) 将Na、O、P三种原子的原子半径大小按由大到小的顺序排列。
-
(4) NH3的稳定性比PH3的(填“强”或“弱”),判断理由是。
-
(5) A、配平上述反应,并标出电子转移方向与数目
P4+ NaOH+H2O→ NaH2PO2 + PH3
B、上述反应中每生成1 mol 氧化产物,转移电子的数目为。
请回答下列问题:
-
(1) 基态硒原子的价电子排布式为;硒所在主族元素的简单氢化物中沸点最低的是。
-
(2) 电还原法制备甲醇的原理为2CO2+4H2O
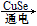 2CH3OH+3O2。
2CH3OH+3O2。 ①写出该反应中由极性键构成的非极性分子的结构式;
②标准状况下,V L CO2气体含有个π键。
-
(3) 苯分子中6个C原子,每个C原子有一个2p轨道参与形成大π键,可记为(π
 右下角“6”表示6个原子,右上角“6”表示6个共用电子)。已知某化合物的结构简式为
右下角“6”表示6个原子,右上角“6”表示6个共用电子)。已知某化合物的结构简式为 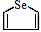 ,不能使溴的四氯化碳溶液褪色,由此推知,该分子中存在大π键,可表示为,Se的杂化方式为。
,不能使溴的四氯化碳溶液褪色,由此推知,该分子中存在大π键,可表示为,Se的杂化方式为。
-
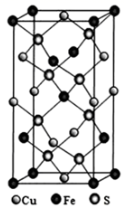
(4) 黄铜矿由Cu+、Fe3+、S2-构成,其四方晶系晶胞结构如图所示。则Cu+的配位数为;若晶胞参数a=b=524pm,c=1032pm,用NA表示阿伏加德罗常数的值,该晶系晶体的密度是g·cm-3(不必计算或化简,列出计算式即可)。
![]()
| 元素 | X | Y | Z | W | R | T |
| 最低负化合价 | -4 | -2 | -3 | -1 | -2 | -1 |
| 电负性 | 2.55 | 2.58 | 3.04 | 3.16 | 3.44 | 4.00 |
 的空间构型为三角锥形
的空间构型为三角锥形
-
(1) 由以上元素组成的分子:DE2、DA4、AJ中,属于极性分子的是。(填真实化学式)。
-
(2) A2E和DJ4是两种常见溶剂,真实化学式分别为 和,D2A4在前者中的溶解度(填“大于”或“小于”)在后者中的溶解度。
-
(3) GA4的沸点(填“高于”或“低于”)DA4的沸点,GE2的熔点(填“高于”或“低于”)DE2的熔点。
 与一定量的水形成
与一定量的水形成  ,一定条件下
,一定条件下  可发生如下转化:
可发生如下转化: 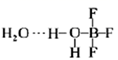
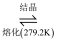
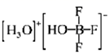
下列说法中正确的是( )
 熔化后得到的物质属于离子晶体
B .
熔化后得到的物质属于离子晶体
B .  分子间只存在着配位键和氢键
C .
分子间只存在着配位键和氢键
C .  是含极性共价键的极性分子
D . 基态B原子核外电子的空间运动状态有5种
是含极性共价键的极性分子
D . 基态B原子核外电子的空间运动状态有5种
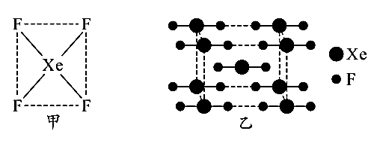
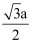 (a为晶胞边长)
(a为晶胞边长)
-
(1) 它们的元素符号分别为:A;B;C;
-
(2) 用电子式表示A2C的形成过程;
-
(3) BC2是由键组成的(填“极性”或“非极性”)分子;BC2分子中B原子采用杂化类型。
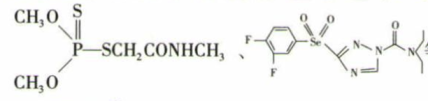 等。
等。
-
(1)
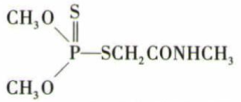 , 中所含元素H、O、P、S的电负性从大到小的顺序为 ;CH3NH2的沸点是-6.8℃,CH3CH3的沸点是-88.6℃ ,CH3NH2的沸点远高于CH3CH3的沸点的原因是。
, 中所含元素H、O、P、S的电负性从大到小的顺序为 ;CH3NH2的沸点是-6.8℃,CH3CH3的沸点是-88.6℃ ,CH3NH2的沸点远高于CH3CH3的沸点的原因是。
-
(2) H2O、H2S、H2Se中最稳定的是(填化学式,下同),还原性最强的是,键角最大的是。
-
(3) SO3和O3的混合气体经光解作用可生成一种新分子
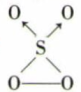 。
。①SO3中S的杂化轨道与O的2p轨道重叠形成σ键。
②下列分子中属于非极性分子的是 (填序号)。
a.SO3
b.O3
c.
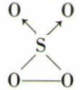
d.CH3F
e.P4
-
(4) 已知酸性:ClCH2COOH>CH3COOH。推测酸性:ClCH2COOH(填“>”或“<")FCH2COOH。
选项 | M组 | N组 |
A | Br2易溶于CCl4 | Br2和CCl4均为非极性分子 |
B | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是共价晶体 |
C | 通常状况下,H2O为液态,NH3为气态 | H2O分子间存在氢键,而NH3分子间不存在氢键 |
D | HI的沸点比HCl的高 | H-I键的键能大于H-Cl键的键能 |
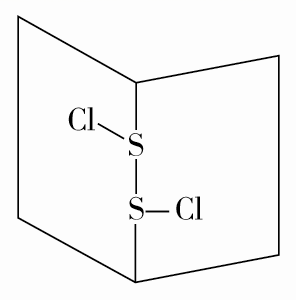
 可用于制备照相业定影剂硫代硫酸钠
可用于制备照相业定影剂硫代硫酸钠 。下列说法正确的是( )
。下列说法正确的是( )
 是非极性分子
B .
是非极性分子
B .  既含离子键又含共价键
C .
既含离子键又含共价键
C .  和
和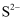 具有相同的电子层结构
D .
具有相同的电子层结构
D .  的电子式为
的电子式为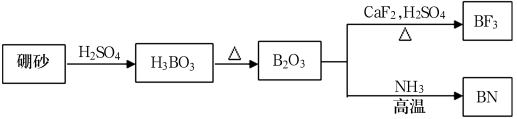
选项 | 实验操作 | 现象 | 结论 |
A | 将用皮毛摩擦过的橡胶棒靠近三氯甲烷液流 | 三氯甲烷的流动方向未发生改变 | 三氯甲烷是非极性分子 |
B | 将 | 有白色絮状沉淀产生 | 结合质子的能力: |
C | 向盛有丙烯醛的试管中加入溴水 | 溴水褪色 | 丙烯醛中含有碳碳双键 |
D | 将铜粉加入稀硫酸中,加热;再加入少量硝酸钾固体 | 加热时无明显现象,加入硝酸钾后溶液变蓝 | 硝酸钾起催化作用 |
- 下图为巴斯德的“鹅颈瓶实验”,该实验说明()A.微生物只能来自空气中的微生物 B.微生物必须在有氧条件下才能产生 C.微
- 在西北地区荒漠化土地面积中,导致荒漠化的第一大人为因素是: A.过度放牧 B.过度开垦 C.过度樵采
- 第二次工业革命期间新兴的工业部门有( ) ①汽车制造业;②钢铁工业;③电力工业;④电讯 工业;⑤化学工业 A.①②
- 阅读下面一段文章,用一句话概括其要点。(不超过20个字) 小说不是论文,它的主题思想不能直说,也不能硬贴上去。好的小说总
- 已知△ABC的面积S=,a=2,b=2,解三角形.
- 23.请简要概括下表所包含的主要信息,表述中不得出现具体数字。
- 请对下面两个病句提出修改意见(或作出修改)。(4分) (1)父亲从头到脚凝视着儿子,激动得热泪盈眶,一句话也说不出
- 如图6所示,边界MN与PQ平行,其间有垂直纸面向里的匀强磁场,矩形导线框框面与磁场方向垂直,其边与边界MN平行,若导线
- 短文改错(共10小题;每小题1分,满分10分) 下面短文中有10处语言错误。请在有错误的地方增加、删除或修改某个单词。
- 如图是“东南亚部分区域图”,读后回答下列问题:(共8分)(1)A国居民中绝大部分是________人。这里属______
- 已知a2-a-1=0,则a3-2a+2011=_______.
- 我舰在敌岛A南偏西50°相距12海里的B处,发现敌舰正由岛沿北偏西10°的方向以10海里/时的速度航行.问我舰需以多大速
- After the mew technique was introduced ,the factory produced
- 给汽车加油时,能闻到汽油味,这是 现象;汽车发动机用水作冷却剂,这是利用了水的 大的性质。
- 在国内通胀压力加大及国家紧缩货币政策大背景下,2011年吉林省十几万户民营企业、中小企业普遍遭遇“三荒”——由于贷款难、
- 如图所示,已知△ABC的周长是21,OB,OC分别平分∠ABC和∠ACB,OD⊥BC于点D,且OD=3,则△ABC的面积
- 、下列说法中正确的是( )两个平行四边形一定相似 B.两个菱形一定相似C. 两个矩形一定相似
- 正态总体N(1,1)在区间(-3,1)和(1,3)上取值的概率分别为m、n,问m与n之间的大小关系是什么?
- 下列各项中,不属于对种群数量特征描述的是() A.2010年,某地区的人口死亡率为8.65‰ B. 我国的人口将逐渐步入
- 1997年,英国的“克隆羊”备受世界关注。“克隆羊”的关键技术之一是找到一些特殊的酶,这些酶能激活普通体细胞,使之像生殖
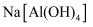 溶液与
溶液与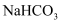 溶液混合
溶液混合



