极性键和非极性键 知识点题库
下列物质中,只含有极性键的是( )
A . HClO
B . Ba(0H)2
C . Na2O2
D . H2O2
按要求填空:有下列物质:①O2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦CaBr2 ⑧H2O2 ⑨NH4Cl⑩HBr,回答下列问题:
-
(1) 只含有极性键的是;
-
(2) 只含有非极性键的是;
-
(3) 含有极性键和非极性键的是;
-
(4) 只含有离子键的离子化合物是;
-
(5) 含有非极性键的离子化合物是.
下列物质中,既含有极性共价键又含有非极性共价键的是( )
A . NH4Cl
B . Na2O2
C . H2O2
D . CH4
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子。N4分子结构如图所示,下列说法正确的是( )
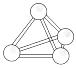
A . N4分子属于一种新型的化合物
B . N4分子中只含有非极性键
C . 1 mol N4分子所含共价键数为4NA
D . N4沸点比P4(白磷)高
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为 ( )
A . 两种分子的中心原子杂化轨道类型不同,NH3是sp2型杂化,而CH4是sp3型杂化
B . NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强
C . NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道
D . 氨气分子是极性分子,而甲烷是非极性分子
下列物质中属于含有非极性键的离子晶体是 ( )
①醋酸钠 ②氢氧化钾 ③过氧化钠 ④金刚石
⑤乙醇 ⑥碳化钙
A . ①②③⑥
B . ①③⑥
C . ①③④⑤
D . ①②⑥
下列关于化学键的说法中正确的是( )
A . H2O2中既有极性键又有非极性键
B . 阴、阳离子间通过静电引力而形成的化学键叫做离子键
C . 非金属元素之间只能形成共价化合物
D . 所有盐、碱和金属氧化物中都含有离子键
下列关于化学键的说法正确的是( )
A . C,N,O,H四种元素形成的化合物一定既有离子键,又有共价键
B . 不同元素的原子构成的分子不一定只含极性共价键
C . 含极性键的共价化合物一定是电解质
D . HF的分子间作用力大于HCl,故HF比HCl更稳定
一定条件下,某容器中各微粒在反应前后变化的示意图如下,其中●和○代表不同元素的原子。
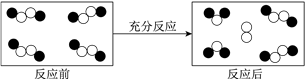
关于此反应的说法错误的是( )
A . 反应物总能量一定低于生成物总能量
B . 一定属于可逆反应
C . 一定有非极性共价键断裂
D . 一定属于氧化还原反应
下列说法正确的是( )
A . 双原子分子中的共价键一定是非极性键
B . 任何原子的原子核都是由质子和中子构成的
C . 非极性键可能存在于离子化合物中
D . 质子数相同的微粒,它们的化学性质基本相同
下列物质中,既含有离子键又含有极性共价键的是( )
A .  B .
B . 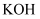 C .
C . 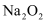 D .
D . 
 B .
B . 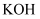 C .
C . 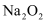 D .
D . 
有下列物质:①Cl2②Na2O2③NaOH
④HCl ⑤H2O2⑥MgF2⑦NH4Cl
-
(1) 只由离子键构成的物质是
-
(2) 只由极性键构成的物质是
-
(3) 只由非极性键构成的物质是
-
(4) 只由非金属元素组成的离子化合物是
-
(5) 由极性键和非极性键构成的物质是
-
(6) 由离子键和极性键构成的物质是、
-
(7) 由离子键和非极性键构成的物质是
美国科学家合成了含有N5+的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈V形,如图所示(图中箭头代表单键)。下列有关该物质的说法中正确的是( )
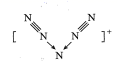
A . 每个Ns+中含有35个质子和36个电子
B . 该离子中只含有非极性键
C . 该离子中含有2个π键
D .  与
与 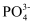 互为等电子体
互为等电子体
 与
与 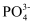 互为等电子体
互为等电子体
下列叙述正确的是( )
A . PCl3 和 BCl3 分子中所有原子的最外层都达到 8 电子稳定结构
B . H2S 和 CS2分子都是含极性键的极性分子
C . (CN)2为直线形分子,含有 3 个σ键和 4 个π键
D . NF3 与 NH3 的空间构型都是三角锥形,都易与 Cu2+形成配离子
T、W、X、Y、Z是原子序数依次增大的五种短周期主族元素且分布于三个周期,W元素可形成硬度最大的单质,X是地壳中含量最多的元素,Y与X同主族。下列说法不正确的是( )
A . 原子半径:r(Z)>r(Y)>r(X)>r(W)>r(T)
B . Y、Z的最高价氧化物对应水化物的酸性:Y<Z
C . 第一电离能:W<X
D . W、X可分别与T形成含有非极性键的极性分子
下列各组物质中,都是非极性分子且只含极性键的是( )
A . CO2 BF3
B . CS2 H2O2
C . S8 PCl5
D . CH4 C2H2
肼(N2H4)又称为联氨,熔、沸点分别为1.4℃、113.5℃,可用如下方法制备肼:CO(NH2)2+ClO- +2OH- =N2H4+Cl-+CO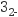 +H2O。下列有关说法正确的是( )
+H2O。下列有关说法正确的是( )
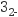 +H2O。下列有关说法正确的是( )
+H2O。下列有关说法正确的是( )
A . N2H4中只存在极性键
B . CO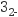 的空间构型为三角锥形
C . CO(NH2)2中C,N,O三种元素第一电离能大小顺序是:C<N<O
的空间构型为三角锥形
C . CO(NH2)2中C,N,O三种元素第一电离能大小顺序是:C<N<O
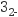 的空间构型为三角锥形
C . CO(NH2)2中C,N,O三种元素第一电离能大小顺序是:C<N<O
的空间构型为三角锥形
C . CO(NH2)2中C,N,O三种元素第一电离能大小顺序是:C<N<O
下列物质中,由极性键构成的非极性分子是( )
A .  B .
B . 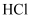 C .
C .  D .
D . 
 B .
B . 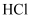 C .
C .  D .
D . 
下列说法正确的是( )
A . 最外层只有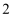 个电子的元素原子性质一定相似
B . 离子键和共价键都有方向性和饱和性
C . 碘单质升华破坏的主要是范德华力
D . 由极性键构成的分子都是极性分子
个电子的元素原子性质一定相似
B . 离子键和共价键都有方向性和饱和性
C . 碘单质升华破坏的主要是范德华力
D . 由极性键构成的分子都是极性分子
 个电子的元素原子性质一定相似
B . 离子键和共价键都有方向性和饱和性
C . 碘单质升华破坏的主要是范德华力
D . 由极性键构成的分子都是极性分子
个电子的元素原子性质一定相似
B . 离子键和共价键都有方向性和饱和性
C . 碘单质升华破坏的主要是范德华力
D . 由极性键构成的分子都是极性分子
Ni可活化C2H6放出CH4 , 其反应历程如下图所示:
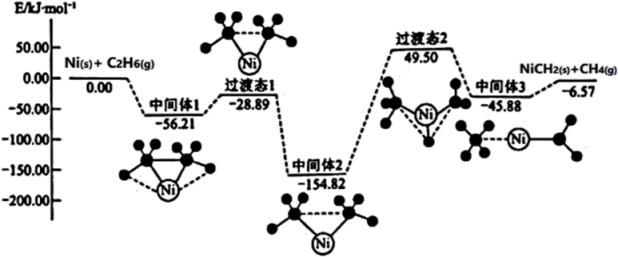
下列关于活化历程的说法错误的是( )
A . 此反应的决速步骤:中间体2→中间体3
B . 只涉及极性键的断裂和生成
C . 在此反应过程中Ni的成键数目发生变化
D . Ni(s)+C2H6(g)=NiCH2(s)+CH4(g) ∆H=−6.57 kJ·mol-1
最近更新
- 如图,AB为半圆的直径,点P为AB上一动点,动点P从A点出发,沿AB匀速运动到点B,运动时间为t,分别以AP与PB的直径
- 1931年底,中华苏维埃共和国临时中央政府成立于( ) A.南昌 B.延安 C.遵义
- 下列各句中,没有错别字的一项是() A. 近日《甄嬛传》收视火爆,好评如潮。饰演太医的张晓龙本身对古典礼仪研究甚深,又将
- 除去CO2 中混有的少量CO,可使混合气体通过 ;除去CO中混有少量CO2,可使混合气体通过
- 下图为“厄尔尼诺发生时太平洋表层水温异常现象示意图”,读图回答据图判断,“≥5℃”的海区在赤道上延伸约:A.3500km
- 如图,在等腰Rt△OAA1中,∠OAA1=90°,OA=1,以OA1为直角边作等腰Rt△OA1A2,以OA2为直角边作等
- 水平飞行的子弹打穿固定在水平面上的木块,经历时间△t1,机械能转化为内能的数值为△E1。同样的子弹以同样的速度击穿放在光
- 某烃结构式如下:-C≡C-CH=CH-CH3,有关其结构说法正确的是( ) A.所有原子可能在同一平面上 B
- 移栽植物的时候,适当剪除一些叶片有利于被移栽植物的成活,其主要原因是( ) A.呼吸作用对有机物的消耗
- 已知木炭还原氧化铜实验中发生的主要反应:C + 2 CuO 高温 2 Cu + CO2↑,某化学兴趣小组对该实验红色
- 美国总统奥巴马在出席亚太经合组织第17次领导人非正式会议之后,前往中国进行国事访问。在与奥巴马会谈中强调,中美两国国情不
- 阅读下列图表,完成下列问题。(1O分)表1 2000年中国跨省人口流动的地区构成流出 省(市) 贵州 四川 湖南 江
- 展开式中的系数是________.
- 甲乙两辆汽车在平直的公路上沿同一方向作直线运动,t=0时刻同时经过公路旁的同一个路标。在描述两车运动的v-t图中(如图)
- 已知:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890.3kJ•mol﹣1,OH﹣(aq)+H+(
- 已知函数,其中 (1)若为偶函数,求a的值; (2)命题p:函数上是增函数,命题q:函数是减函数
- 学生要称量16.8克固体药品的质量,称量后,发现天平指针向左偏,此时,正确的操作应该是( )
- 函数y=lg的定义域是____________.
- 在25 ℃时,向100 mL含氯化氢14.6 g的盐酸溶液中,放入5.6 g纯铁粉,反应进行到2 min末收集到氢气1
- 32. His composition won first prize, ______ made him too hap



