极性键和非极性键 知识点题库
下列各组分子中都属于含极性键的非极性分子的是( )
A . CO2、H2S
B . C2H4、CH4
C . Cl2、C2H2
D . NH3、HCl
(1)根据下列七种物质,回答问题:
A、干冰;B、氧化镁;C、氯化铵;D、固态碘;E、烧碱;F、冰;G、过氧化钠;
①含非极性键的是 ;②只含有极性键的是 ;
③既有离子键又有共价键的是 ;④只含有离子键的是 ;
(2)温度、固体表面积、气体压强、溶液的浓度、催化剂等都能改变化学反应速率,下列各项分别与哪个影响化学反应速率因素的关系最为密切.
①同质量的铁片和铁粉与足量的同浓度的盐酸反应,后者先反应完.
②镁粉在冷水中反应仅有微量气泡逸出,但加热时则有大量气泡产生.
③两支装有相同H2O2的试管,向其中一支加入MnO2 , 有大量气泡冒出
下列物质中,既含有离子键又含有非极性键的是( )
A . CO2
B . MgCl2
C . KOH
D . Na2O2
现代无机化学对硫﹣氮化合物的研究是最为活跃的领域之一.其中图是已经合成的最著名的硫﹣氮化合物的分子结构.下列说法正确的是( )
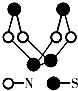
A . 该物质的分子式为SN
B . 该物质的分子中既有极性键又有非极性键
C . 该物质具有很高的熔、沸点
D . 该物质与化合物S2N2互为同素异形体
C60、金刚石、石墨、二氧化碳和氯化铯的结构模型如图所示(石墨仅表示出其中的一层结构):
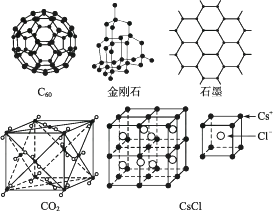
-
(1) C60、金刚石和石墨三者的关系是互为 。A . 同分异构体 B . 同素异形体 C . 同系物 D . 同位素
-
(2) 固态时,C60属于(填“原子”或“分子”)晶体,C60分子中含有双键的数目是。
-
(3) 晶体硅的结构跟金刚石相似,1 mol晶体硅中含有硅—硅单键的数目约是NA。
-
(4) 石墨层状结构中,平均每个正六边形占有的碳原子数是。
-
(5) 观察CO2分子晶体结构的一部分,试说明每个CO2分子周围有个与之紧邻且等距的CO2分子;该结构单元平均占有个CO2分子。
-
(6) 观察图形,CsCl晶体中两距离最近的Cs+间距离为a,则每个Cs+周围与其距离为a的Cs+数目为;每个Cs+周围距离相等且第二近的Cs+数目为,距离为;每个Cs+周围距离相等且第三近的Cs+数目为,距离为;每个Cs+周围紧邻且等距的Cl-数目为。
下列各组物质中,都是由极性键构成极性分子的一组是( )
A . CH4和Br2
B . NH3和H2O
C . H2S和CCl4
D . CO2和HCl
SiCl4的分子结构与CCl4类似,对其作出如下推断,其中正确的是( )
①SiCl4晶体是分子晶体 ②常温、常压下,SiCl4是液体 ③SiCl4分子是由极性键形成的非极性分子 ④SiCl4的熔点高于CCl4的
A . ①
B . ①②
C . ②③
D . ①②③④
已知:H2(g)+Cl2(g) = 2HCl(g)反应的能量变化示意图如下:
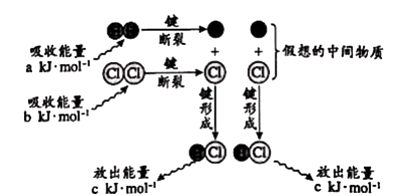
下列说法正确的是( )
A . 点燃条件和光照条件下,反应的ΔH不同
B . 反应的ΔH约为[2c- (a+b)]kJ·mol-1
C . “假想的中间物质”的总能量低于起始态H2和Cl2的总能量
D . 反应涉及的物质中,既有含极性键的物质,也有含非极性键的物质
下列说法正确的是( )
A . 分子晶体中一定存在分子间作用力,不一定存在共价键
B . 分子中含两个氢原子的酸一定是二元酸
C . 非极性分子中一定含有非极性键
D . 元素的非金属性越强,其单质的活泼性一定越强
中科院理化技术研究所张铁锐等人成功制备了超薄LDH纳米片光催化剂,实现了在常温常压和可见光或直接太阳辐射下N2和H2O合成氨,其原理示意图如下。下列说法正确的是( )
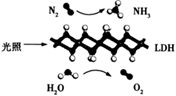
A . 在该合成氨反应条件下,每转移2NA个电子需要22.4L的H2O
B . 反应前后极性键的数目不变
C . LDH是反应的催化剂,并不参与反应
D . 反应中氧化产物与还原产物的物质的量之比为4∶3
下列说法错误的是( )
A . 离子键是一种静电作用力
B . 极性键就是共用电子对发生偏移的共价键
C . 氢键是一种比较弱的化学键
D . 水结冰时体积膨胀、密度减小就是因为氢键的存在
下列说法中错误的是( )
A . 单质中不存在离子键
B . 含有离子键的化合物一定是离子化合物
C . 含有共价键的化合物一定是共价化合物
D . 在一种物质中可能同时含有离子键、极性键和非极性键
三硫化磷(P4S3)可用于制造火柴,分子结构如图所示。下列说法错误的是( )
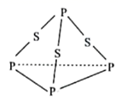
A . P4S3中磷元素为+3价
B . P4S3属于共价化合物
C . P4S3含有非极性键
D . 1molP4S3分子含有9mol共价键
X、Y、Z、W是原子序数依次增大的短周期主族元素。X的原子核内只有一个质子,液态ZX3常用作制冷剂,Y原子L层比W原子M层多1个电子,W的单质在常温下能被浓硫酸钝化。下列说法正确的是( )
A . 最简单氢化物沸点:Z>Y
B . X、Y形成的化合物中只含有极性键
C . 最高正价:W>Z>Y>X
D . 最高价氧化物对应水化物的酸性:Y>Z
下列说法正确的是( )
A . 2p和3p轨道形状均为哑铃形,能量也相等
B . 乙醇分子中O-H键的极性强于C-H键的极性
C . CH4和SO2分子中心原子上的孤电子对数均为1
D . 同一原子中,2p、3p、4p能级轨道数依次增多
下列物质中既含有离子键又含有共价键的是( )
A . BaCl2
B . H2SO4
C . KOH
D . Na2O
下列分子中,既含有极性键又含有非极性键的是( )
A . CH2Cl2
B . HCHO
C . H2O
D . CH2=CH-CH3
已知N、P同属于元素周期表的第VA族元素,N在第二周期,P在第三周期。NH3分子呈三角锥形,N原子位于锥顶,3个H原子位于锥底,N-H键间的夹角是107.3°。
-
(1) 氮原子最外层电子排布式为;氮离子(N3- )核外有种运动状态不同的电子;N4分子的空间结构为
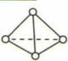 , 它是一种(填“极性"或“非极性")分子。
, 它是一种(填“极性"或“非极性")分子。
-
(2) PH3分子与NH3分子的空间结构关系: (填“相同”或“不相同”),P-H键 (填“有”或“无")极性,PH,分子(填“有"或“无" )极性。
如表为元素周期表的一部分,其中的编号代表对应的元素。
① | |||||||||||||||||
② | ③ | ④ | |||||||||||||||
⑤ | ⑥ | ⑦ | |||||||||||||||
⑧ | ⑨ | ⑩ |
请回答下列问题:
-
(1) 元素②形成的含氧酸中,酸根离子呈正三角形的酸是(填化学式)。
-
(2) 元素②③⑧的第一电离能由大到小的顺序是(填元素符号)。
-
(3) 元素④⑥⑦的简单气态氢化物中最稳定的是(填化学式),元素⑤⑧的最高价氧化物对应水化物反应的离子方程式为。
-
(4) 写出元素⑨的基态原子的价电子排布式:。
-
(5) 将元素⑩的无水硫酸盐溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子,写出该配合离子的结构简式(必须将配位键表示出来)。
-
(6) 元素①和②③形成的:二元共价化合物中,分子呈三角锥形的化合物为(填化学式);分子中既含有极性共价键,又含有非极性共价键的化合物有(填化学式,写一种)。
黑火药是中国古代四大发明之一,其爆炸原理为2KNO3+S+3C=K2S+N2↑+3CO2↑。下列说法正确的是( )
A . 每消耗0.1molS,同时生成6.72LCO2
B . 氧化剂与还原剂的总物质的量之比为1:2
C . 每生成0.5molN2 , 反应转移电子的物质的量为6mol
D . 该反应过程中只有极性键和离子键的形成
最近更新
- 马克思主义哲学不是离开世界文明大道而独立产生的,它是人类历史根本转折时代的产物。马克思主义哲学产生的阶级基础是 A.无产
- 如图所示,四边形ADEF为正方形,△ABC为等腰直角三角形,D在BC边上,连接CF. (1)求证:BC⊥CF; (2)若
- 右图是A、B两种物质的溶解度曲线(1)当温度低于t℃时,溶解度A B(填“>”,“<”或“=
- You can’t imagine___________more embarrassing scene when you
- It is in the room _____our meeting will be held. A. where
- 据统计,在我国网民中染有网瘾的的未成年人高达250万人。要戒除网瘾就应该( )A. 关注现实,控制消极情绪
- 下列命题正确的是A.A={整数},B={奇数},则一定不能建立从A到B的映射B.若A为无限集,B为有限集,则一定不能建立
- Our hometown is quite different from _______before. A. that
- 分子式为C5H7Cl的有机物,其结构不可能是()A.只含有1个双键的直链有机物B.含2个双键的直链有机物C.含1个双键的
- This is the nurse who____to me when I was ill in hospital. A
- 在下面一段话的空缺处依次填入词语,最恰当的一组是()眼科医生证实,长期玩手机游戏,会对视网膜造成__________,如
- 人体的血液中,钾元素含量偏低会影响肌肉和神经的功能.一种医用含钾化合物的溶液能跟 硝酸银溶液反应生成不溶于稀硝酸的白色沉
- 唐朝全盛时期国家强盛,经济空前繁荣,此时在位的皇帝是 ( ) A.唐高祖 B.唐太宗 C.武则天
- 下表反映了上海:上海外白渡桥通行的交通工具变化表(据《上海研究资料》)年份 人力车 马车 轿子 马 自行车 摩托车 汽车
- 中国十七届六中全会2011年10月15日至18日在北京召开。全会审议通过了《中共中央关于深化文化体制改革、推动社会主义文
- 地质灾害是指在自然或者人为因素的作用下形成的,对人类生命财产、环境造成破坏和损失的地质作用(现象).地势灾害主要发生在(
- 材料一:2010年年初原油价格承2009年年末的国际原油市场走势,截至3月26日,2010年一季度原油最低价格为71.1
- .The negotiation between the two countries broke down, _____
- 下列不属于向性运动的是() A.植物向光生长B.根向地生长 C.茎背地生长D.蛾类向灯光飞翔
- 每一种生物的细胞内,染色体数量是一定的 ( )



