无机物的推断 知识点题库
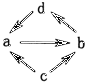
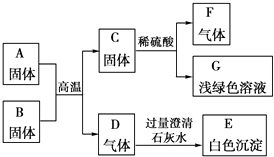
A是某工厂废旧机械表面上红色固体的主要成分Fe2O3 , B、C、F都是单质,D、F都是无色无味的气体,它们之间的相互转化关系如图所示:
请回答:
-
(1) 写出下列物质的化学式:B,C,F.
-
(2) 写出气体D和过量澄清石灰水反应的离子方程式:.
-
(3) 写出A和B反应的化学方程式:.
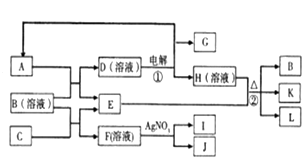
如图表示有关物质之间的转化关系,A,C,E,G为非金属单质,其中A,G常温常压下为气态,E遇淀粉变蓝,K是一种常用食品添加剂,L是常见的无色无味液体,I为淡黄色固体,J的焰色反应呈浅紫色(透过蓝色钴玻璃).
-
(1) B,I代表的物质化学式分别为、.
-
(2) 写出反应①②的离子方程式:
①
②
-
(3) 选出实验室保存C单质的注意事项(A.无色瓶B.棕色瓶C.橡胶塞D.玻璃塞),除此之外还采取了什么特殊保存方法:.
-
(4) 已知A,C,E均能与G反应,按其反应条件要求由高到低顺序为(用化学式表示)
-
(5) A与H溶液反应,其氧化产物和还原产物的物质的量的比为1:1,写出此反应的化学反应方程式:.
甲、乙、丙、丁均为中学化学常见的物质,它们之间的转化关系如图(反应条件及其它产物已略去).下列说法不正确的是( )
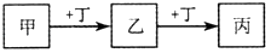
A . 若甲是AlCl3溶液,则丁可能是NaOH溶液
B . 若甲是Fe,则丁可能是Cl2
C . 若丁是CO2 , 则甲可能为Mg
D . 若丁是O2 , 则乙、丙的相对分子质量可能相差16
甲、乙、丙、丁四种物质的转化关系如图所示,其中甲、乙为单质,丙、丁为化合物.
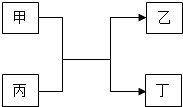
-
(1) 若工业上用该反应制粗硅写出该反应的化学方程式: .
-
(2) 若该反应可用于焊接铁轨且丙为红棕色固体则该反应的化学方程式为:.
-
(3) 若丁为具有磁性的黑色晶体写出该反应的化学方程式:.
-
(4) 若甲为黄绿色气体,且该反应用来检验工业上甲是否泄漏,写出该反应的化学方程式:.
现有金属单质A、B、C和气体乙、丙及物质D、E、F、G、H,它们之间发生如下反应(图中有些反应的产物和反应的条件没有全部标出).
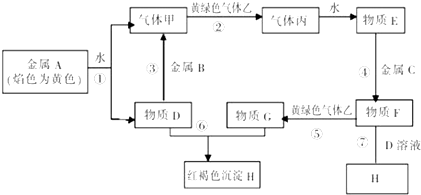
请根据以上信息回答下列问题:
-
(1) 物质F的化学式为.
-
(2) 说出黄绿色气体乙的一种用途
-
(3) 区别E、F两种溶液最简单的方法是,实验室检验G中所含的金属离子时,常在G的溶液中加入溶液.
-
(4) 反应①的离子方程式为.
-
(5) 物质F→H的转化需经过两个连续进行的反应,请写出这两个反应的化学方程式:、.
有关物质的转化关系如图所示(部分物质和条件已略去),A是一种淡黄色粉末,B是某种矿物中的主要成分,D、Y是空气含量最多的两种气体,J是一种紫红色金属,X是最常见的无色液体.
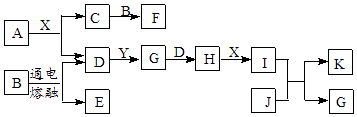
-
(1) A的化学式为
-
(2) Y的电子式为
-
(3) I与J反应的化学方程式为
-
(4) C与B在溶剂X中反应的离子方程式为.
给定条件下,下列选项中所示的物质间转化均能一步实现的是( )
A . 粗硅  SiCl4
SiCl4  Si
B . Mg(OH)2
Si
B . Mg(OH)2  MgCl2(aq)
MgCl2(aq)  Mg
C . Fe2O3
Mg
C . Fe2O3  FeCl3(aq)
FeCl3(aq)  无水FeCl3
D . AgNO3(aq)
无水FeCl3
D . AgNO3(aq) 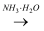 [Ag(NH3)2]OH(aq)
[Ag(NH3)2]OH(aq)  Ag
Ag
 SiCl4
SiCl4  Si
B . Mg(OH)2
Si
B . Mg(OH)2  MgCl2(aq)
MgCl2(aq)  Mg
C . Fe2O3
Mg
C . Fe2O3  FeCl3(aq)
FeCl3(aq)  无水FeCl3
D . AgNO3(aq)
无水FeCl3
D . AgNO3(aq) 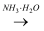 [Ag(NH3)2]OH(aq)
[Ag(NH3)2]OH(aq)  Ag
Ag
已知A是生产生活中用量最大的金属,B为淡黄色粉末。在常温下C为无色液体,E、G、H、I、J为气体,其中H为黄绿色,其它为无色.J能使湿润的红色石蕊试纸变蓝(图中部分产物已略去)。
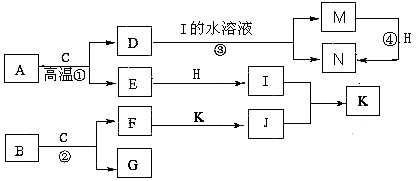
请填写下列空白
-
(1) 写出化学式:M,K。
-
(2) 写出①的化学方程式;写出③的离子方程式。
-
(3) 反应④属于下列何种反应类型______(填字母序号)。A . 化合反应 B . 氧化还原反应 C . 离子反应 D . 置换反应
-
(4) 若要确定③反应后所得溶液中含有M物质,所选试剂为______(填序号)。A . KSCN溶液和氯水 B . 铁粉和KSCN C . 浓氨水 D . 酸性高锰酸钾溶液
-
(5) 常温下,H与过量的J反应产生浓厚的白烟,另一生成物是空气的主要成分之一,请写出该反应的化学方程式。
现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为FeSO4溶液,G为CuSO4溶液,它们之间存在如图所示关系:
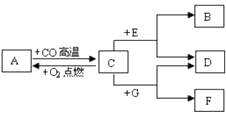
-
(1) 推测下列物质的化学式A,B,F。
-
(2) 写出A→C转化的化学方程式。
-
(3) 写出C+G→D+F转化的离子方程式。
在葡萄糖溶液中加入新制氢氧化铜悬浊液加热.会产生色沉淀.说明葡萄糖具有性.(填“氧化”或“还原”)在淀粉中加入碘水溶液呈.色.以此来检测淀粉的存在,在装有淀粉溶液的烧杯中通过一束光线,在侧面可以看到一条光亮的通路,由此可判断该分散系属于。
草酸钴可用于指示剂和催化剂的制备。用水钴矿(主要成分为Co2O3 , 含少量Fe2O3、Al2O3、MnO、MgO、CaO、SiO2等)制取CoC2O4·2H2O工艺流程如下图所示:
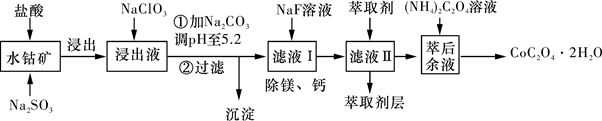
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②酸性条件下,ClO3-不会氧化Co2+ , ClO3-转化为Cl-;
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
-
(1) 浸出过程中加入Na2SO3的主要目的是。
-
(2) 向浸出液中加入NaClO3的离子反应方程式:。
-
(3) 已知:常温下NH3·H2O
 NH4++OH- Kb=1.8×10-5
NH4++OH- Kb=1.8×10-5 H2C2O4
 H++HC2O4- Ka1=5.4×10-2
H++HC2O4- Ka1=5.4×10-2HC2O4-
 H++C2O42- Ka2=5.4×10-5
H++C2O42- Ka2=5.4×10-5则该流程中所用(NH4)2C2O4溶液的pH7(填“>”或“<”或“=”)。
-
(4) 加入(NH4)2C2O4 溶液后析出晶体,再过滤、洗涤,洗涤时可选用的试剂有___(填字母代号)。A . 蒸馏水 B . 自来水 C . 饱和的(NH4)2C2O4溶液 D . 稀盐酸
-
(5) 萃取剂对金属离子的萃取率与pH的关系如图1所示,萃取剂的作用是;其使用的适宜pH范围是(填字母代号)。
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5
-
(6) CoC2O4·2H2O热分解质量变化过程如图2所示。其中600℃以前是隔绝空气加热,600℃以后是在空气中加热。A、B、C均为纯净物;C点所示产物的化学式是。
下列各组物质之间不能通过一步就能实现如图所示转化的是( )
| 物质编号 | 物质转化关系 | a | b | c | d |
| A | | SiO2 | Na2SiO3 | Si | H2SiO3 |
| B | Na2O | Na2O2 | Na | NaOH | |
| C | Al2O3 | NaAlO2 | Al | Al(OH)3 | |
| D | FeCl2 | FeCl3 | Fe | CuCl2 |
A . A
B . B
C . C
D . D
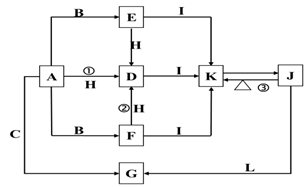
下列各物质中只有A,B,C三种单质,A的焰色反应为黄色,主要以G形式存在于海水中,F是一种淡黄色的固体,H是一种常见的无色液体,I是造成温室效应的“元凶”,各物质间的转化关系图如下:
回答下列问题:
-
(1) A是:,C是:,L是:,I是:(填化学式)。
-
(2) 写出反应①②③的化学反应方程式:
①:;
②:;
③:;
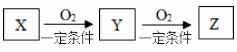
已知物质X、Y、Z之间存在如下转化关系,将装满气体Z的试管倒扣在水槽中,溶液最终充满的试管体积的2/3。则X是( )
A . Na
B . S
C . CH4
D . NH3
图中“—”表示相连的物质间在一定条件下可以反应,“→”表示丁在一定条件下可以转化为乙。下面四组选项中,符合图示要求的是( )
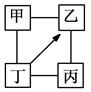
| 甲 | 乙 | 丙 | 丁 | |
| A | H2SO4 | Na2SO4 | NaOH | NaCl |
| B | KCl | K2CO3 | KOH | HCl |
| C | O2 | CO | CuO | C |
| D | Zn | FeCl2 | Cu | HCl |
A . A
B . B
C . C
D . D
-
(1) I.化合物A由三种元素组成,气体B是含氢量最高的烃。固体E既能溶于盐酸,又能溶于氢氧化钠溶液。按如下流程进行实验:
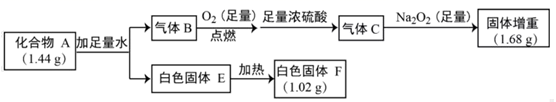
E的化学式为:,气体C与Na2O2反应的化学方程式为:
-
(2) A的化学式为:,A与足量盐酸反应的化学方程式为:
-
(3) Ⅱ.将ClO2通入NaOH和H2O2的混合溶液中,可制得一种高效漂白剂亚氯酸钠(NaClO2),实验装置如图所示:
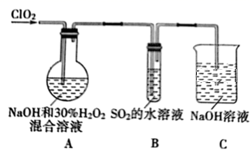
请回答:
写出A装置中发生反应的离子方程式
-
(4) 请设计实验方案探究通入足量的ClO2后,B装置溶液中存在的含有硫元素的微粒
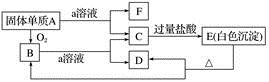
在如图所示的物质相互转化关系中,A是一种固体单质,E是一种白色不溶于水的物质。据此填空。
-
(1) 写出各物质的化学式:
A.、B、C、
D.、E、F。
-
(2) B与a溶液反应的离子方程式是。
-
(3) A与a溶液反应的离子方程式是。
已知常温下,A是黑色固体;B是无色浓溶液;通常状况下,D是黄绿色气体;E是一种常见金属单质;I为红褐色沉淀;G能使品红溶液褪色,加热又恢复红色。物质A~I之间的转化关系如下图所示:
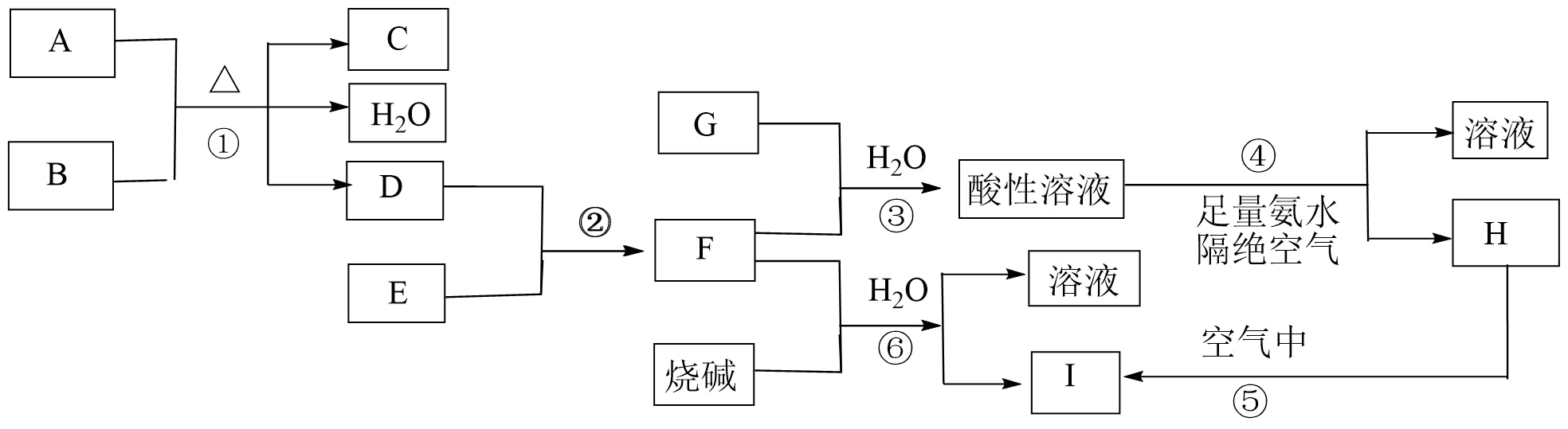
请回答下列问题:
-
(1) 推断出下列物质(用化学式作答):C,G。
-
(2) 请写出下列反应的方程式:反应①的离子方程式;反应③的离子方程式;反应⑤的化学方程式。
-
(3) 欲从反应⑥的体系中得到沉淀I的系列操作是、、恒温干燥(均填操作名称)。
-
(4) 实验室配制90 mL2 mol/L的烧碱溶液,需选用mL容量瓶。用托盘天平称取g烧碱。若定容时,俯视刻度线,配制的溶液的浓度(填“偏大”“偏小”或“无影响”)。
以电石渣[主要成分为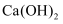 , 含少量
, 含少量 等杂质]为原料制备纳米碳酸钙的一种工艺流程如下:
等杂质]为原料制备纳米碳酸钙的一种工艺流程如下:
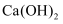 , 含少量
, 含少量 等杂质]为原料制备纳米碳酸钙的一种工艺流程如下:
等杂质]为原料制备纳米碳酸钙的一种工艺流程如下: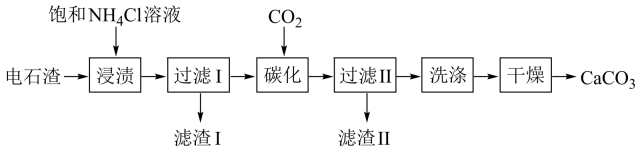
下列说法错误的是( )
A . “浸渍”时,适当提高温度,有利于提高 浸取率
B . 滤液II中主要成分是
浸取率
B . 滤液II中主要成分是 , 可以循环使用
C . “碳化”中反应的离子方程式为
, 可以循环使用
C . “碳化”中反应的离子方程式为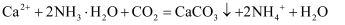 D . 已知
D . 已知 , 则滤液II中
, 则滤液II中 沉淀完全时,
沉淀完全时, 小于
小于
 浸取率
B . 滤液II中主要成分是
浸取率
B . 滤液II中主要成分是 , 可以循环使用
C . “碳化”中反应的离子方程式为
, 可以循环使用
C . “碳化”中反应的离子方程式为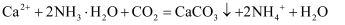 D . 已知
D . 已知 , 则滤液II中
, 则滤液II中 沉淀完全时,
沉淀完全时, 小于
小于
固体M可能含有Cu、Fe2O3、Na2SO3、Na2SO4、KNO3中的几种,进行如图实验:
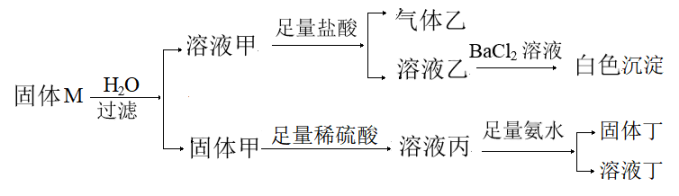
下列说法错误的是( )
A . 溶液甲中一定含有Na2SO3 , 可能含有Na2SO4
B . 若气体乙是单一气体,则M中一定不含有KNO3
C . 固体甲中n(Cu):n(Fe2O3)≤1:1
D . 取少许溶液丙,滴加KMnO4溶液,若溶液不褪色,则固体丁一定是纯净物
最近更新
- 已知函数f(x)=2x3-3(a-1)x2+4x+6a(a∈R),g(x)=4x+6.(Ⅰ)若函数y=f(x)的切线斜率
- “消失的旧时光一九四三,在回忆的路上时间变好慢,老街坊小弄堂,是属于那年代白墙黑瓦的淡淡的忧伤……”以上是周杰伦的歌曲《
- (广东卷)2.下面语段中画线的词语,使用不恰当的一项是 与连篇累牍的电视剧本身相比,剧中翻书的动作、人物的坐姿等,只是一
- ______ met, it won’t be easily forgotten. A. If you B. when
- On the River Thames there are a number of boat races ever
- 2008北京奥运会中,大家关注的焦点曾集中在刘翔身上,阿丘就有自己独特的看法:“其实不必要求刘翔硬撑,为了一场比赛让运动
- 如图13所示,竖直向上的匀强磁场,开始时磁感应强度B=0.5 T,并且以=0.1 T/s在变化,水平轨道电阻不计,且不计
- “多难兴邦”,汶川大地震使我国遭受了重大损失,但抗震救灾让我们整个国家的凝聚力空前提升。这体现的辩证法道理是A.意识对物
- 神经递质的主要作用机制,是通过与细胞膜上的受体结合,直接或间接调节细胞膜上离子通道的开启或关闭,造成离子通透性的改变,进
- 下列现象或应用不能用胶体的知识解释的是() A. 清晨,人们经常看到阳光穿过茂密的树木枝叶所产生的美丽景象 B. 土壤表
- 下列关于先秦时期的表述,正确的是() A.禹用王位世袭制代替禅让制 B.国人暴动使商朝由盛而衰 C.葵丘会盟确
- 第三部:阅读理解 (共两节,满分40分) 第一节:阅读短文(共15小题,每小题2分,满分30分) About
- 对下面语段内容概括最恰当的一项是( )(2分) 正如今天人们对生活质量的要求和对事物的评价一样,追求本色、原色和自
- 阅读下面的文字,完成后面题。 天坛传说 天坛是明清两朝皇室举行祭天大典的祭坛,是天子向天帝表达敬意,祈求国泰民安、国运长
- 下表是用单摆测定重力加速度实验中获得的有关数据:①利用上述数据在图B-6中描出l-T2图象.②利用图象,T2取5.2时,
- 如图所示,处于真空中的匀强电场与水平方向成15°角,AB直线与强场E互相垂直。在A点,以大小为vo的初速度水平抛出一质量
- 从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是()
- 第二节 完型填空(共20小题;每小题1.5分,满分30分) 阅读下面短文,掌握其大意,然后从36—55各题所给的四个选项
- 利用图6-4所示装置,可进行若干实验。
- Theweather in my hometown in summer is usually very hot but