氧化还原反应方程式的配平 知识点题库
-
(1) 配平反应的离子方程式:
XeO3+Mn2++H2O→ MnO4﹣+Xe↑+H+
-
(2) 反应现象为:①有气泡产生;②.
-
(3) 被氧化的元素是.
-
(4) 将适量的XeO3投入30mL 0.1mol•L﹣1 Mn2+的水溶液中,刚好完全反应.
①此时转移电子总数为.
②将反应后的溶液稀释至90mL,所得溶液的pH=.
资料:K2FeO4为紫色固体,微溶于KOH溶液:具有强氧化性,在酸性或中性溶液中快速产生O₂,在碱性溶液中较稳定。
-
(1) 制备K2FeO4(夹持装置略)
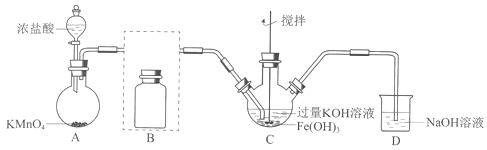
①A为氯气发生装置。A中反应方程式是(锰被还原为Mn2+)。
②将除杂装置B补充完整并标明所用试剂 。
③C中得到紫色固体和溶液。C中Cl2发生的反应有3Cl2+2Fe(OH)3+10KOH=2K2FeO4+6KCl+8H2O,另外还有。
-
(2) 探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2 , 为证明是否K2FeO4氧化了Cl-而产生Cl2 , 设计以下方案:
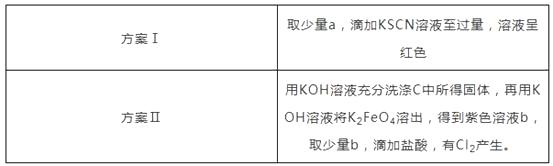
Ⅰ.由方案Ⅰ中溶液变红可知a中含有离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由产生(用方程式表示)。
Ⅱ.方案Ⅱ可证明K2FeO4氧化了Cl- , 用KOH溶液洗涤的目的是。
②根据K2FeO4的制备实验得出:氧化性Cl₂
 (填“>”或“<”),而方案Ⅱ实验表明,Cl2和
(填“>”或“<”),而方案Ⅱ实验表明,Cl2和  的氧化性强弱关系相反,原因是。
的氧化性强弱关系相反,原因是。③资料表明,酸性溶液中的氧化性
 >MnO4- , 验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性
>MnO4- , 验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性  > MnO4- , 若能,请说明理由;若不能,进一步设计实验方案。理由或方案:。
> MnO4- , 若能,请说明理由;若不能,进一步设计实验方案。理由或方案:。
-
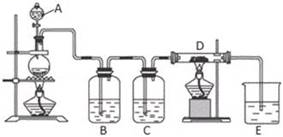
(1) 仪器A的名称是,烧瓶中反应的化学方程式是。
-
(2) 装置B中盛放液体是,气体通过装置B的目的是。装置C中盛放的液体是。
-
(3) D中反应的化学方程式是。
-
(4) 烧杯E中盛放的液体是,反应的离子方程式是。
-
(5) 资料表明D中产物有以下性质:①受热易升华,冷却后易凝华;②遇H2O(g)剧烈反应。为收集D中产物,在D与E之间,除增加收集装置外,还需要增加装置。
回答下列问题
-
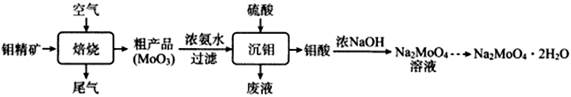
(1) 完成下列反应:MoS2+O2
 SO2+ MoO3在焙烧炉中,空气从炉底进入矿石经粉碎后从炉顶进入,这样处理的目的是。
SO2+ MoO3在焙烧炉中,空气从炉底进入矿石经粉碎后从炉顶进入,这样处理的目的是。
-
(2) 浓氨水浸取粗产品获得(NH4)2MoO4溶液,其化学反应方程式为_;该反应说明MoO3(填“有”或“没有”)酸性氧化物的性质。
-
(3) 常温下,沉钼阶段所得废液为(NH4)2SO4稀溶液。若(NH4)2SO4稀溶液的pH=a,则
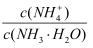 =(用含a的代数式表示,NH3·H2O的Kb=1.8×10-5),若将此稀溶液蒸发浓缩,
=(用含a的代数式表示,NH3·H2O的Kb=1.8×10-5),若将此稀溶液蒸发浓缩, 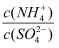 将(填“变大”“不变”或“变小”)。
将(填“变大”“不变”或“变小”)。
-
(4) 已知钼酸钠在一定温度范围内的析出物质及相应物质的溶解度如下表所示,获得Na2MoO4·2H2O的操作为。
温度(℃)
0
4
9
10
15.5
32
51.5
100
析出物质
Na2MoO4·10H2O
Na2MoO4·2H2O
溶解度
30.63
33.85
38.16
39.28
39.27
39.82
41.27
45.
结晶得到的母液可以在下次结晶时重复使用,但达到一定次数后必须净化处理,原因是。
-
(5) 空气中钼酸盐对碳钢的缓蚀原理是在钢铁表面形成FeMoO4-Fe2O3保护膜,在密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入钼酸盐外还需加入的物质是 (填选项字母)。A . NaNO2 B . 通入适量N2 C . 油脂 D . 盐酸
-
(1) 写出新制氯水中含量最多的微粒的化学式(水分子除外)
-
(2) 写出漂白粉中有效成分的名称
-
(3) 描述检验溶液中K+离子的实验操作过程
-
(4) 配平下列化学方程式
()Cu+()HNO3(稀)=()Cu(NO3)2+()NO↑+()H2O
-
(5) 按照物质的分类,次磷酸(H3PO2)属于二元酸,其与足量的NaOH溶液反应的化学方程式为
-
(1) 请用上述物质填空,并配平化学方程式:
C++ H2SO4——++Cr2(SO4)3+H2O
-
(2) 上述反应中氧化剂是(填化学式),被氧化的元素是(填元素符号)。
-
(3) H2SO4在上述反应中表现出来的性质是(填选项序号) 。A . 氧化性 B . 氧化性和酸性 C . 酸性 D . 还原性和酸性
-
(4) 若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为。
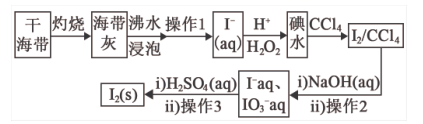
下列有关说法正确的是( )
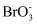 +Cl2=Br2+2
+Cl2=Br2+2 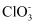 ②
② 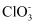 +5Cl-+6H+=3Cl2+3H2O ③2FeCl2+Cl2=2FeCl3 。根据上述反应,判断下列结论中错误的是( )
+5Cl-+6H+=3Cl2+3H2O ③2FeCl2+Cl2=2FeCl3 。根据上述反应,判断下列结论中错误的是( )
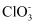 >
> 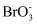 > Cl2 >Fe3+
D . 溶液中可发生:
> Cl2 >Fe3+
D . 溶液中可发生: 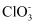 +6Fe2++6H+=Cl-+6Fe3++3H2O
+6Fe2++6H+=Cl-+6Fe3++3H2O
-
(1) Ⅰ. SO2易溶于水,能部分与水化合生成一种二元酸,写出该反应的化学方程式。
-
(2) 根据硫元素化合价预测,SO2应具有的化学性质是。
-
(3) 已知:SO2不能与盐酸和硫酸反应,但可以与硝酸反应,配平该反应: SO2 + NO
 + H2O = SO
+ H2O = SO  +NO + H+
+NO + H+
-
(4) Ⅱ.现在小新和小关同学对SO2与漂白粉的反应进行实验探究:
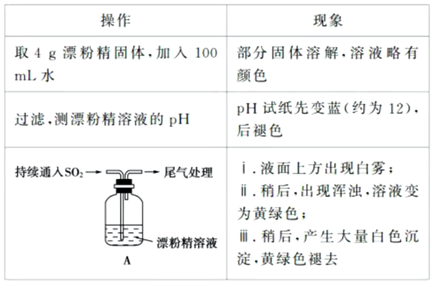
Cl2和Ca(OH)2制取漂白粉的化学方程式
-
(5) pH试纸颜色的变化说明漂白粉溶液具有的性质是
-
(6) 小新推测现象i的白雾是盐酸小液滴,并进行如下实验,请写出相应的现象:
a.用湿润的紫色石蕊试纸检验白雾,
b.用硝酸酸化的AgNO3溶液检验白雾,
小新同学认为可以得出结论:白雾是盐酸小液滴。但是小冠同学查阅资料,发现Ag2SO4 , 为白色固体,微溶于水,不溶于硝酸,小冠结合SO2的性质,分析小新的实验,他认为小新的结论不可靠,小冠的理由是:白雾中可能也含有SO2 , 。
-
(7) 现象ⅱ中溶液变为黄绿色的可能原因:随溶液酸性增强,漂白粉的主要成分发生反应,请写出离子方程式。
-
(8) 将反应后A瓶中混合物过滤、洗涤,得到沉淀X和滤液Y。
①取滤液Y,加入稀HCl无明显变化,再加入BaCl2溶液,产生白色沉淀,则说明液Y中含有的离子是,沉淀X为。
②用离子方程式解释现象ⅲ中黄绿色褪去的原因。

①请配平偏二甲肼燃烧的化学方程式
C2H8N2 +N2O4  CO2 + H2O +N2
CO2 + H2O +N2
②氧化剂与还原剂的质量之比为。
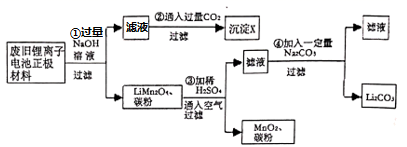
已知:Li2CO3在不同温度下的溶解度
| 温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
| Li2CO3 | 1.593 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
-
(1) 第①步反应中会有气体生成,该气体为:,若要增大第①步反应的浸取率,可以采取的措施有: (写两条)。
-
(2) 第②步反应得到的沉淀X的化学式为,上述流程中四步实验都包含过滤,实验室过滤时要使用的玻璃仪器有:。
-
(3) 工业上洗涤Li2CO3用的是热水而不是冷水,其原因是。
-
(4) 写出第③步反应“酸溶”过程中反应的离子方程式:。
-
(5) 固相法制备LiMn2O4的实验过程如下:将MnO2和Li2CO3按4:1的物质的量之比配料,球磨3-5小时,然后高温加热,保温24小时,冷却至室温。
①写出该反应的化学方程式:。
②LiMn2O4中锰元素的平均价态为+3.5。在不同温度下,合成的LiMn2O4中Mn2+、Mn3+和Mn4+的含量与温度的关系见表。
T/℃
w(Mn2+)(%)
w(Mn3+)(%)
w(Mn4+)(%)
700
5.56
44.58
49.86
750
2.56
44.87
52.57
800
5.50
44.17
50.33
850
6.22
44.40
49.38
由此可以确定:在上述温度范围内,锰元素的平均价态的变化趋势是:随温度升高(填选项)
A.增大 B减小 C.先增大后减小 D.先减小后增大
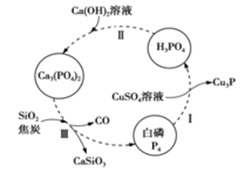
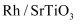 为载体,激发产生电子(e-)—空穴(h+),反应机理如图所示。下列说法错误的是( )
为载体,激发产生电子(e-)—空穴(h+),反应机理如图所示。下列说法错误的是( ) 
 在
在  上发生还原反应
C . 在
上发生还原反应
C . 在  表面,每生成
表面,每生成 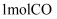 ,向空穴转移电子数为
,向空穴转移电子数为  D . 该反应可表示为
D . 该反应可表示为 
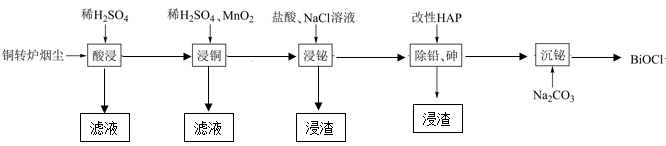
已知:①BiOCl难溶于水;
②“浸铋”所得浸取液中含BiCl3、AsCl3等物质。
回答下列问题:
-
(1) “浸铜”时有单质硫生成,发生反应的离子方程式为。
-
(2) “沉铋”时需控制溶液的pH=3.0,此时BiCl3发生反应的化学方程式为。“沉铋”所得滤液可导入到中使用(填流程中操作单元名称)。
-
(3) 工业生产中还可采用铁盐氧化法除砷。向“浸铋”所得浸取液中加入
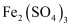 ,和H2O2 , 并调节pH,生成FeAsO4沉淀,发生反应的离子方程式是。欲使溶液中
,和H2O2 , 并调节pH,生成FeAsO4沉淀,发生反应的离子方程式是。欲使溶液中 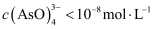 且不产生
且不产生 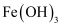 ,沉淀,应控制pH的范围为。(已知:
,沉淀,应控制pH的范围为。(已知: 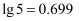 ;
; 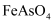 、
、 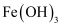 的Ksp分别
的Ksp分别 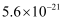 ,
, 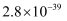 ,计算结果保留2位小数)
,计算结果保留2位小数)
-
(4) 氯氧化铋(BiOCl)可用作钾离子电池(有机物作离子导体)的负极材料,充电时嵌入K+ , BiOCl被还原为Bi,电极反应式是。研究发现,充电过程中,除上述反应外,还包括
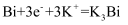 ,该反应的发生使得电池的储能(填“增大”“减小”或“不变”)。
,该反应的发生使得电池的储能(填“增大”“减小”或“不变”)。
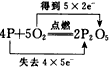 B .
B . 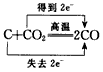 C .
C . 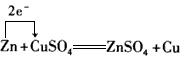 D .
D .  )是一种新型绿色消毒剂,主要用于饮用水处理。工业上一种制备高铁酸钠的方法的化学原理可用离子方程式
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上一种制备高铁酸钠的方法的化学原理可用离子方程式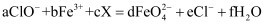 表示。下列说法正确的是( )
表示。下列说法正确的是( )
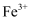 是氧化剂,
是氧化剂, 是氧化产物
B . a、b、c、d、e、f的数值分别是3、2、10、2、3、5
C .
是氧化产物
B . a、b、c、d、e、f的数值分别是3、2、10、2、3、5
C .  是
是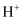 D .
D . 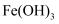 胶体可以吸附水中杂质达到净水的目的,含
胶体可以吸附水中杂质达到净水的目的,含 个
个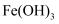 胶粒的氢氧化铁胶体中铁元素的质量为
胶粒的氢氧化铁胶体中铁元素的质量为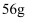

-
(1) K2FeO4中铁元素的化合价为。
-
(2) 制备 K2FeO4需要在(填“酸性”、“碱性”或“中性”)环境中进行。
-
(3) 下列关于K2FeO4的说法中,错误的是。
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快、安全性好、无异味
-
(4) 将K2FeO4与水反应的化学方程式补充完整:4K2FeO4+_H2O=_Fe(OH)3(胶体)+ _+ _KOH,。
-
(5) 消毒净化500 m3水,至少需要K2FeO4的质量为kg。
 ,还含有
,还含有  及钠、铝、铜的氧化物等杂质),一种以锆矿石为原料制备工业纯
及钠、铝、铜的氧化物等杂质),一种以锆矿石为原料制备工业纯  的工艺流程如图所示:
的工艺流程如图所示: 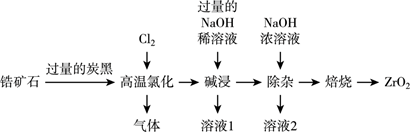
已知:  易溶于水,390℃会升华;
易溶于水,390℃会升华; 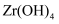 难溶于水,受热易分解。
难溶于水,受热易分解。
回答下列问题:
-
(1) 为使氯化得更充分,一般采用的措施有(只填一条)。
-
(2) “高温氯化”过程中,
 的产率与温度的关系如图所示,试分析随温度升高
的产率与温度的关系如图所示,试分析随温度升高  产率降低的原因:;“高温氯化”结束前会通一段时间氧气,其目的是。
产率降低的原因:;“高温氯化”结束前会通一段时间氧气,其目的是。 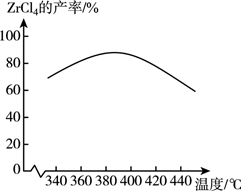
-
(3) “高温氯化”可以把氧化物转化为氯化物,写出
 在“高温氯化”时发生反应的化学方程式:。
在“高温氯化”时发生反应的化学方程式:。
-
(4) “过量的NaOH稀溶液”的作用是;得到“溶液1”的操作名称为,该操作所用的玻璃仪器有。
-
(5) “溶液2”中含
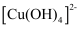 ,写出生成该离子的离子方程式:。
,写出生成该离子的离子方程式:。
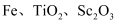 等多种成分,用酸化后的钛白废水富集钪,并回收氧化钪(Sc2O3)的工艺流程如下:
等多种成分,用酸化后的钛白废水富集钪,并回收氧化钪(Sc2O3)的工艺流程如下:
回答下列问题:
-
(1) “萃取”时
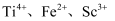 均进入有机相中,则在“洗涤”时加入
均进入有机相中,则在“洗涤”时加入 的目的是。
的目的是。
-
(2) “滤渣1”的主要成分是
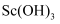 、(写化学式)。
、(写化学式)。
-
(3) 在“调pH”时先加氨水调节
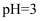 , 此时过滤所得滤渣主要成分是;再向滤液中加入氨水调
, 此时过滤所得滤渣主要成分是;再向滤液中加入氨水调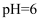 , 此时滤液中
, 此时滤液中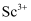 的浓度为
的浓度为 ;检验含
;检验含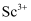 滤液中是否含
滤液中是否含 的试剂为(写化学式)。(已知:
的试剂为(写化学式)。(已知: ;
; )。
)。
-
(4) “沉钪”时用到草酸。已知草酸的
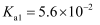 ;
;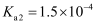 ;则在
;则在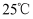 时
时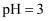 的草酸溶液中
的草酸溶液中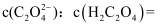 。
。
-
(5) 写出草酸钪在空气中“焙烧”时反应的化学方程式。
-
(6) 钛白酸性废水中
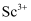 含量
含量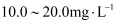 , 该工艺日处理钛白酸性废水
, 该工艺日处理钛白酸性废水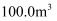 , 理论上能生产含
, 理论上能生产含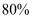 氧化钪的产品最多kg(保留2位有效数字)。
氧化钪的产品最多kg(保留2位有效数字)。
- —Do you really want to go out? —It may rain.
- 近期统计数据显示,癌症已经成为我国城乡居民的首要死因。请根据提供法的材料回答问题:(1)体外分别培养某癌细胞和正常体细胞
- 一定条件下,在密闭容器内发生反应,测得反应前后各物质的质量如下表所示,下列说法正确的是物 质 CO2 O2 H2O W
- 下列行为中,不利于人与自然和谐相处的是( ) A.退耕还林,植树造林 B.大量捕杀青蛙 C.建立自然保护区
- 苯酚和苯甲醇共同的化学性质是有酸性 B.与钠反应放出氢气C.遇三氯
- 某地为低山丘陵区,山地占36.62%,丘陵占39.7%,平原占20.78%,洼地占2.90%,山丘起伏和缓,沟壑纵横交错
- 已知两个羧基之间在浓硫酸作用下脱去一个水分子生成酸酐, ,某酯类化合物A是广泛使用的塑料增塑剂。A在酸性条件下能够生成B
- (1)等差数列{an}中,a2+a7+a12=24,求S13.(2)已知等差数列{an}的前4项和为25,后4项和为63
- 沁尿系统各部分的功能是什么?
- 等比数列前项的和为,则数列前项的和为______________。
- A harrowing competition is underway in England, with billion
- 21.观察下面的图画,根据要求作文。 (60分) 。这幅图画引发了你哪些联想或思考?请自选角度写一篇不少于800字的文章
- 实验室常利用以下装置完成气体制备及性质实验。请回答:(1)指出编号仪器的名称:①_ __,②__ _。 (2)以上_(从
- 关于元素周期表,下列叙述中不正确的是 ( ) A.在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的
- 27.某实验小组设计了如图(a)所示的实验装置,通过改变重物的质量,利用计算机可得滑块运动的加速度a和所受拉力F的关系图
- 下列各组物质中,熔点由高到低的是 A.HI、HBr、HCl、HF B.石英、食盐、干冰、钾C.CI4、CB
- 不同膜结构的膜之间可以相互转化。下列各项中,以囊泡的方式进行转化的是( ) A.核膜和内质网膜 B.细胞
- 下列四组生物中,细胞结构最相似的一组是A.肾蕨、水绵、香菇 B.酵母菌、灵芝、豌豆 C.小麦、番茄、大豆 D.水稻
- 我们把两组邻边相等的四边形叫做“筝形”.如图,四边形是一个筝形,其中,.对角线,相交于点,,,垂足分别是,.求证.
- 如图,已知AB∥CD∥EF,则x、y、z三者之间的关系是()A.x+y+z=180° B.x+y﹣z=180°



