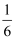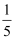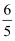氧化还原反应方程式的配平 知识点题库
编号 | a的取值范围 | 产物的化学式(或离子符号) |
① | a≤ | I2Br﹣ |
② |
| I2Br﹣Br2 |
③ |
| I2 IO3﹣ Br2 |
④ | a≥ | IO3﹣ Br2 |
-
(1) 将这6种物质分别填入下面对应的横线上,组成一个未配平的化学方程式:
+Na2SO3+→+++H2O
-
(2) 反应物中发生氧化反应的物质是(填化学式).
-
(3) 反应中1mol氧化剂得到mol电子.
-
(1) 配平下列化学方程式:并用单线桥标出电子转移的方向和数目.
Fe3O4+CO=Fe+CO2
-
(2) 检验SO42﹣所需要用的试剂和.
-
(3) 三硅酸镁(Mg2Si3O8•11H2O)用氧化物表示.
-
(4) 0.3mol NH3 分子中所含质子数与个H2O分子中所含质子数相等.
-
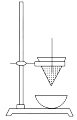
(1) 取磁性氧化铁按图所示装置进行铝热反应,引发铝热反应的实验操作是。取少许反应生成的“铁块”溶于盐酸,向其中滴加KSCN溶液,发现溶液变为血红色。出现这种现象,一方面可能因为“铁块”中混有没反应的磁性氧化铁,另一方面可能因为。
-
(2) 请写出此铝热反应的化学方程式:,1 mol Al参与反应,转移的电子数为。
-
(3) 设计一个简单的实验方案,证明上述所得的“铁块”中含有金属铝。该实验所用试剂是,反应的离子方程式为。
-
(4) 除了磁性氧化铁可做铝热反应实验,下列试剂也可以发生铝热反应的是________(填字母,双选)。A . CuO B . Na2O2 C . MnO2 D . MgO
-
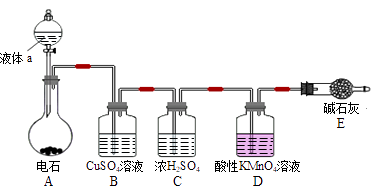
(1) 实验室制取乙炔时,分液漏斗中的液体a通常是。
-
(2) CuSO4溶液的作用是。
-
(3) 配平乙炔与酸性KMnO4溶液反应的化学方程式(请在方框中填计量系数):
□C2H2+□KMnO4+□H2SO4—□K2SO4+□MnSO4+□CO2↑+□H2O
-
(4) 若该小组实验原理及所有操作均符合题意,则下列各因素对所测乙炔的相对分子质量没有影响的是(填选项)____________。A . 装置A中产生的气体直接通入酸性KMnO4溶液 B . 乙炔通过酸性KMnO4溶液的速率过快,少量乙炔未被氧化而逸出 C . 将E装置(盛有碱石灰的干燥管)换成盛有浓硫酸的洗气瓶
-
(5) 另一课外小组认为,该课外小组的实验装置及实验操作存在不足,请用简明文字说明,应采取何种措施或改进?答:。
-
(1) 工业采用高温分解H2S制取氢气,2H2S(g)
 2H2(g) + S2(g),在膜反应器中分离出H2。在容积为 2L 的恒容密闭容器中,控制不同温度进行此反应。H2S的起始物质的量均为 1mol,实验过程中测得H2S的转化率如图所示。曲线 a 表示H2S的平衡转化率与温度的关系,曲线 b 表示不同温度下反应经过相同时间时H2S的转化率。
2H2(g) + S2(g),在膜反应器中分离出H2。在容积为 2L 的恒容密闭容器中,控制不同温度进行此反应。H2S的起始物质的量均为 1mol,实验过程中测得H2S的转化率如图所示。曲线 a 表示H2S的平衡转化率与温度的关系,曲线 b 表示不同温度下反应经过相同时间时H2S的转化率。 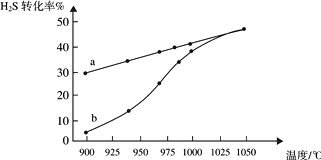
①反应2H2S(g)
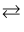 2H2(g) + S2(g)的ΔH(填“>”“<”或“=”)0。
2H2(g) + S2(g)的ΔH(填“>”“<”或“=”)0。②985℃时,反应经过5 s达到平衡状态,此时H2S的转化率为40%,则用H2表示的反应速率为v(H2) =。
③随着H2S分解温度的升高,曲线b向曲线a逐渐靠近,其原因是。
-
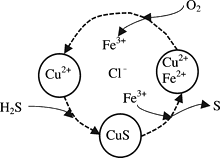
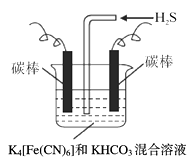
(2) 将H2S和空气的混合气体通入FeCl3 、FeCl2 、CuCl2的混合溶液中反应回收S,其物质转化如下图所示。
①在图示的转化中,化合价不变的元素是。
②在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施有。
-
(3) 工业上常采用上图电解装置电解K4[Fe(CN)6]和KHCO3混合溶液,电解一段时间后,通入H2S 加以处理。利用生成的铁的化合物K3[Fe(CN)6]将气态废弃物中的H2S 转化为可利用的S,自身转化为K4[Fe(CN)6]。
①电解时,阳极的电极反应式为。
②当有16 g S析出时,阴极产生的气体在标准状况下的体积为。
③通入H2S 时发生如下反应,补全离子方程式:
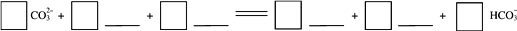
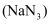 和硝酸钾
和硝酸钾 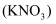 。汽车发生猛烈撞击时,
。汽车发生猛烈撞击时, 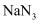 会迅速分解产生
会迅速分解产生 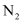 和Na,Na单质可与
和Na,Na单质可与 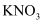 继续反应。完成下列填空:
继续反应。完成下列填空:
-
(1) 原子最外层电子的电子排布式为,氮气的电子式为。
-
(2) 请将
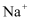 、
、  、
、  按照离子半径由大到小的顺序排列
按照离子半径由大到小的顺序排列 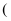 填离子符号
填离子符号 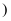 。
。
-
(3)
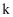 的金属性强于Na,用一个事实说明。
的金属性强于Na,用一个事实说明。
-
(4) 配平Na与
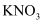 反应的化学方程式,并标出电子转移的方向与数目:
反应的化学方程式,并标出电子转移的方向与数目: 
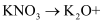

 ,若标准状况下生成
,若标准状况下生成 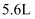 氮气,转移的电子数目为
氮气,转移的电子数目为  。
。 -
(5) 请解释
 晶体比
晶体比  晶体熔点低的原因。
晶体熔点低的原因。
-
(1) 配平下述化学反应方程式(请将配平的计量数依次填入上式)
其反应式为:C+K2Cr2O7+H2SO4═CO2↑+Cr2(SO4)3+K2SO4+H2O
-
(2) H2SO4在上述反应中表现出来的性质是 (填选项编号)。A . 酸性 B . 氧化性 C . 吸水性 D . 脱水性
-
(3) 上述反应中若产生0.2mol CO2 , 则转移电子的物质的量是mol。
-
(4) 上述反应中氧化剂与还原剂的物质的量比为:。
-
(1) 将上述化学方程式配平并改写为离子方程式。
-
(2) 浓盐酸在反应中显示出来的性质是。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
-
(3) 若产生0.5 mol Cl2 , 则被氧化的HClmol,转移的电子的数目约为。
-
(4) 一定条件下,KMnO4还可以氧化其他还原性物质。
MnO4-+C2O42-+=Mn2++CO2↑+完成上述离子方程式,此反应中,发生氧化反应的物质是;若转移1 mol电子,生成标准状况下CO2L。
-
(1) I、KClO3和浓盐酸在一定温度下反应,还原产物为黄绿色的易爆物二氧化氯。其变化可以表示为:□KClO3+□HCl(浓)→□KCl+□ClO2↑+□Cl2↑+□H2O+□_
请配平该化学方程式。
-
(2) 浓盐酸在反应中显示出来的性质是(填编号)。
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
-
(3) Ⅱ、已知反应:2H2CrO4+3H2O2=2Cr(OH)3↑+2H2O该反应中H2O2只发生如下变化过程H2O2→H2O
①该反应中的还原剂是。
②该反应中被还原的元素是,还原产物是。
③若产生的气体在标准状况下体积为3.36L,则反应中转移了mol电子
-
(1) 亚硝酰氯(C—N=O)气体是有机合成中的重要试剂,它可由Cl2和NO在通常条件下反应制得,该反应的热化学方程式为。
相关化学键的键能如下表所示:
化学键
Cl—Cl
N≡O(NO气体)
Cl—N
N=O
键能/(kJ·mol-1)
243
630
200
607
-
(2) 为研究汽车尾气转化为无毒无害的物质的有关反应,在某恒容密闭容器中充入4molCO和4 mol NO,发生反应2CO+2NO
 2CO2+N2 , 平衡时CO的体积分数与温度(T1<T2)压强的关系如图所示:
2CO2+N2 , 平衡时CO的体积分数与温度(T1<T2)压强的关系如图所示: 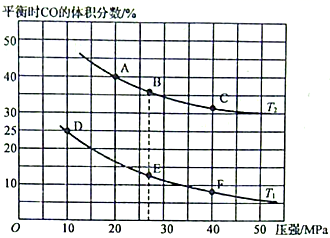
①该可逆反应达到平衡后,为在提高反应速率的同时提高NO的转化率,可采取的措施有(填标号)。
a.按体积比1:1再充入CO和NO b.改用高效催化剂
c.升高温度 d.增加CO的浓度
②由图可知,压强为20MPa、温度为T2下的平衡常数Kp=MPa-1(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数。保留4位小数)。
③若在B点对反应容器降低温度至T1的同时缩小体积至体系压强增大,达到新的平衡状态时,可能是图中A~F点中的点(填标号)。
-
(3) 有人设想采用下列方法减少SO2、NO2对环境的污染:用CH4还原SO2 , 从产物中分离出一种含硫质量分数约为94%的化合物,并用这种化合物来还原NO2。这种含硫化合物和NO2反应的化学方程式为。
-
(4) 用NaOH溶液吸收SO2也是减少大气污染的一种有效方法。25℃时,将一定量的SO2通入到NaOH溶液中,两者完全反应,若溶液中
 ,则该混合溶液的pH=(25℃时,H2SO3的电离平衡常数Ka1=1.0×10-2 , K a2=1.0×10-7)。
,则该混合溶液的pH=(25℃时,H2SO3的电离平衡常数Ka1=1.0×10-2 , K a2=1.0×10-7)。
-
(5) 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下:
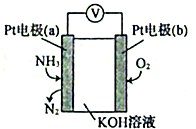
①电极b上发生的是反应(填“氧化”或“还原”)。
②电极a的电极反应为。
 2H2O+O2↑
D . 总反应为:2H2O
2H2O+O2↑
D . 总反应为:2H2O
 2H2↑+O2↑
2H2↑+O2↑
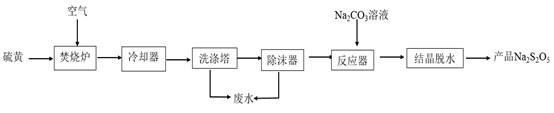
已知:NaHSO3的过饱和溶液经结晶脱水可生成Na2S2O5。
回答下列问题:
-
(1) 为便于焚烧,可对硫黄采取的措施是。
-
(2) 废水中含有硫单质,其中一种分子组成为S8 , 可与KOH溶液发生如下反应:3S8+48KOH
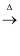 16K2S+8K2SO3+24H2O,该反应中氧化剂与还原剂的物质的量之比为。
16K2S+8K2SO3+24H2O,该反应中氧化剂与还原剂的物质的量之比为。
-
(3) 反应器中发生反应的离子方程式为。
-
(4) Na2S2O5是强还原剂,很容易被O2氧化,同时放出一种有刺激性气味的气体,该反应的化学方程式为。
-
(5) Na2S2O5生产过程中会产生SO2 , SO2在空气中的含量超过0.02 mg·L-1就会危害人类健康。可用如下装置测定空气中SO2的含量。
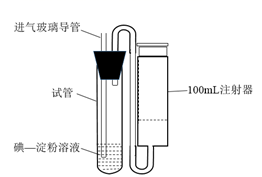
①取5 mL 5×10-4 mol·L-1的碘溶液E入试管中,再加入2~3滴淀粉溶液,在测定地点慢慢抽气,每次抽气100 mL,直到试管中的溶液 (填写现象)。
②记录抽气次数n。n≥,说明气体符合安全标准(假设气体均处于标准状况)。
③抽气时应慢慢抽拉活塞,原因是。
①将沉淀全部放入锥形瓶中,加入足量的10%H2SO4和适量的蒸馏水,使沉淀完全溶解,溶液呈酸性,加热至75℃,趁热用0.0500mol·L-1KMnO4溶液进行滴定,记录所用KMnO4溶液的体积。
②过滤并洗涤沉淀。
③准确称取氯化钙样品0.2400g,放入烧杯中,加入适量6mol·L-1的盐酸和适量蒸馏水使样品完全溶解,再滴加35.00mL0.2500mol·L-1(NH4)2C2O4溶液,水浴加热,逐渐生成CaC2O4沉淀。经检验,Ca2+已沉淀完全。
④再重复以上操作2次并进行数据处理。
完成下列各题:
-
(1) 上面的实验步骤合理的顺序是(填序号)。
-
(2) 写出步骤①中加入KMnO4溶液后发生反应的离子方程式。
-
(3) 滴定终点判断的依据是。
-
(4) 某次实验滴定结束时滴定管内的液面见图,则此时液面读数为mL。

-
(5) 实验最终测得氯化钙样品中钙元素的质量分数38.00%(样品中不含其它含有钙元素的杂质),下列说法能合理解释该实验结果的是___。A . 酸性高锰酸钾溶液已部分变质 B . 滴定过程中,用蒸馏水冲洗锥形瓶内壁上的KMnO4溶液 C . 滴定时有部分高锰酸钾溶液滴在了实验台上 D . 酸式滴定管用蒸馏水洗过后又用所要盛装的溶液润洗
-
(1) 已知反应:
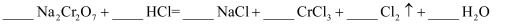 。
。 配平该化学反应方程式。
-
(2) 如果反应中转移
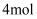 电子,则生成的
电子,则生成的  在标准状况下的体积为L。
在标准状况下的体积为L。
-
(1) 酸浸:用硫酸溶液浸取烧渣中的铁元素。若其他条件不变,下列措施中能提高单位时间内铁元素浸出率的有____(填序号)。A . 适当升高温度 B . 适当加快搅拌速率 C . 适当减小硫酸浓度
-
(2) 沉铁:取10mL“酸浸”后的滤液并加入9gNH4HCO3 , 改变氨水用量,测得铁的沉淀率随氨水用量的变化如图。
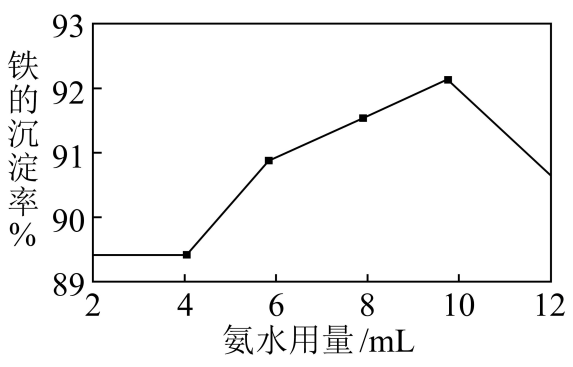
①为提高铁的沉淀率,应控制氨水用量为。②氨水用量小于4mL时,铁的沉淀率几乎无变化,其原因可能为。
-
(3) 过滤:“沉铁”后过滤,滤渣中含有FeOOH和FeCO3 , 滤液中浓度最大的阳离子是(填化学式)。
-
(4) 焙烧:FeOOH和FeCO3高温焙烧后均可得到铁红,写出FeCO3高温焙烧的化学方程式。
 溶液能被
溶液能被 溶液还原成
溶液还原成 而使溶液褪色。欲使20.00mL
而使溶液褪色。欲使20.00mL 酸性
酸性 溶液恰好褪色,需消耗25.00mL
溶液恰好褪色,需消耗25.00mL 溶液,则该
溶液,则该 溶液的物质的量浓度(单位:
溶液的物质的量浓度(单位: )为( )
)为( )
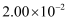 B .
B . 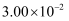 C .
C . 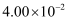 D .
D . 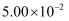
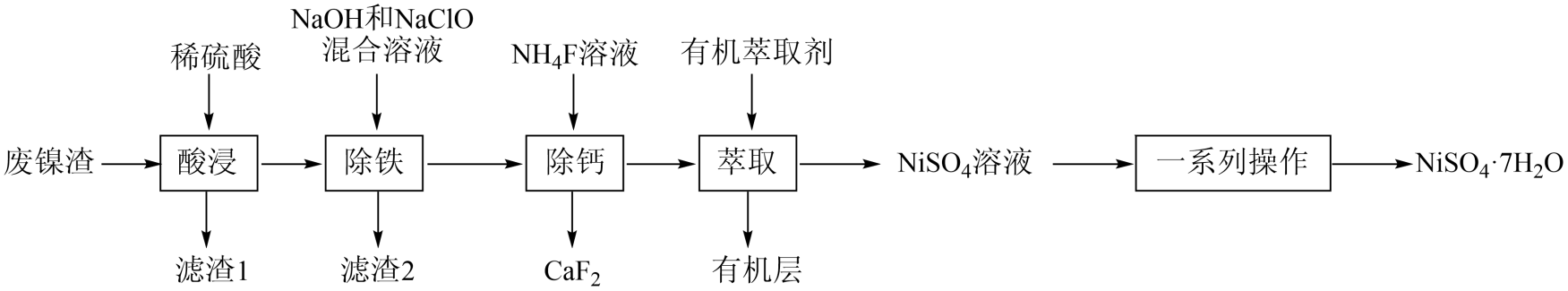
请回答下列问题:
-
(1) 滤渣1的主要成分是(填化学式);“酸浸”中硫酸溶液质量分数不宜高于49%,主要原因是。
-
(2) “一系列操作”是蒸发浓缩降温结晶、过滤、洗涤、低温干燥,采用“低温干燥”的原因是。
-
(3) “除铁”的离子方程式为。
-
(4) 已知:常温下,Ksp(CaF2)=1.5×10-10。在“除钙”中,溶液中c(F-)=0.01mol·L-1'时,c(Ca2+)=mol·L-1。
-
(5) 测定NiSO4·7H2O产品纯度:取wgNiSO4·7H2O产品于溶水配制成250mL溶液,量取配制的溶液25.00mL于维形瓶中,用cmol·L-1EDTA(用Na4Y表示)溶液滴定:Ni2++Y4-=NiY2- , 固定至终点时,消耗滴定液VmL。假设杂质不与EDTA反应,该产品的纯度为(用含c、w、V的代数式表示)。
-
(1) 高铁酸钾的制备,装置如图1所示。
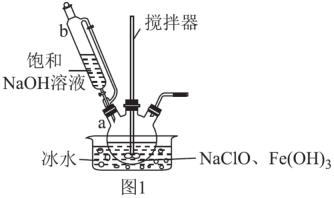
步骤一:将b中饱和NaOH溶液全部逐滴滴入a中,充分反应;
步骤二:由b向a中反应后液体中加入饱和KOH溶液;
步骤三:将a中所得浊液移出,分离提纯。
①仪器b的名称是,其侧管的作用为。
②a中制备Na2FeO4反应的离子方程式为。
③K2FeO4悬浊液经过滤、洗涤,可得粗产品。粗产品中的可溶性杂质可通过方法进一步提纯。
-
(2) K2FeO4遇水转化为Fe(OH)3 , 则其能用于净水的原理为:。
-
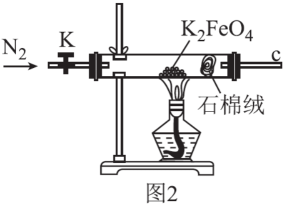
(3) 用图2所示装置探究K2FeO4受热分解的产物。设计实验方案证明完全分解后的固体产物中不含Fe(II):取完全分解后的少量固体,溶于稀硫酸,。
-
(4) 实验室可用间接碘量法测定含少量KCl杂质的K2FeO4样品的纯度:称取0.9000gK2FeO4样品溶于碱性KI溶液中,调节pH使混合液充分反应。用1.000mol·L-1的Na2S2O3标准溶液进行滴定,消耗Na2S2O3标准溶液15.00mL。请计算K2FeO4样品的纯度:。
已知:
 +4I-+8H+=Fe2++2I2+4H2O;I2+2
+4I-+8H+=Fe2++2I2+4H2O;I2+2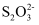 =
=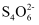 +2I-。
+2I-。
- 物理兴趣小组的同学想探究物体受到浮力大小随浸入深度的变化规律,选用了一个底面积为30cm2、高为10cm的实心合金圆柱体
- 计算
- 下列结论错误的是( ) A.命题“若x2-3x-4=0,则x=4”的逆否命题为“若x≠4,则x2-3x-4≠0” B.“
- 1919年6月20日,来中国访问的杜威在写给他女儿的信中说:“要使我们国家14岁多能孩子领导人们展开一场大清扫的政治改革
- 下图为甲、乙、丙、丁4种遗传性疾病的调查结果.根据系谱图分析、推测这4种疾病最可能的遗传方式以及一些个体最可能的基因型是
- 下面事例中,属于内能转化为机械能的是() A. 用锤子敲打钉子时,钉子发热 B. 古代人们的
- “文革”中我国国民经济遭受严重破坏,1973年却出现复苏局面,这是因为( )A.周恩来主持中央日常工作,着手恢复国
- 是的,我们的命运被安排定了,在这个充满车辆与烟囱的城市里,我们的存在只是一种悲凉的点缀。但你们尽可以节省下你们的同情心,
- Jane often helps her mum wash the ______ inthe kitchen after
- 已知2MOyx-+5S2-+16H+=2M2+ +5S↓+ 8H2O,则下列选项正确的是 A.x=2
- 下列反应中①2KClO32KCl+3O2↑②C+CO22CO③HgS+O2Hg+SO2④2KMnO4K2MnO4+MnO
- 阅读下面的文言文,完成后面题目。 陈庆之,字子云,义兴国山人也。幼而随从高祖。高祖性好棋,每从夜达旦不辍,等辈皆倦寐,惟
- 为了减少汽车对城市大气的污染,1998年6月,我国成功地开发出以新燃料作能源的“绿色汽车”,这种汽车可避免有毒的有机铅,
- 今有四种粒子的结构示意图,下列说法不正确的是()A.它们表示四种元素 B.④表示的元素在化合物通常显+3价 C.①表示的
- 鉴别稀盐酸、稀硫酸、Ba(OH)2、Na2CO3、FeCl3五瓶无标签的溶液。(1)通过观察溶液的 直接鉴别出
- 如图,AB是半圆O的直径,弦AD、BC相交于P,那么等于( ) A、sin∠BPD B、cos∠BPD
- (16分)(15分)质量为M=10kg的B板上表面上方,存在一定厚度的相互作用区域,如图中划虚线的部分,当质量为m=1k
- 下列结论正确的是 ① 微粒半径:S2->Cl->S>F ②
- 阅读下列材料,完成各题: 材料一:因马尔维纳斯群岛的归属问题,1982年4月阿、英爆发了“马岛战争”,10星期后战争结束
- 下列有关秦郡县制的表述,正确的是 A.皇帝任免郡县长官 B.郡县长官拥有自己的