氧化还原反应方程式的配平 知识点题库
-
(1) NaOH的电子式为.
-
(2) 工业上常用焦炭还原二氧化硅制备粗硅,用化学方程式表示.
-
(3) FeSO4溶液与稍过量的NH4HCO3溶液混合,有FeCO3白色沉淀生成和明显的无色气泡现象,写出相关离子方程式.
-
(4) 完成以下氧化还原反应的离子方程式:
() Cr2O2﹣7+() H2O2+()═() Cr3++()H2O+().
-
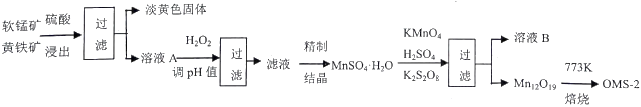
(1) FeS2中硫元素的化合价是。“调pH并过滤”主要除去元素。
-
(2) Mn12O19中氧元素化合价均为-2价,锰元素的化合价有两种,则Mn (Ⅲ)、Mn (Ⅳ) 物质的量之比为。生产过程中的原料KMnO4、K2S2O8、MnSO4·H2O按物质的量比1:1:5反应,产物中硫元素全部以SO42-的形式存在,该反应的离子方程式为。
-
(3) 溶液B可进一步分离出两种主要化合物,一种可在该工艺中循环使用,化学式是;另一种为盐类,在农业生产中可用作。
-
(4) OMS-2是一种纳米级的分子筛。分别用OMS-2和MnOx对甲醛进行催化氧化,在相同时间内甲醛转化率和温度的关系如图:
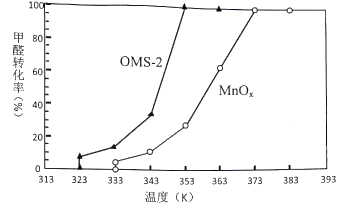
由图可知,OMS-2与MnOx相比,催化效率较高是,原因是。
-
(5) 甲醛(HCHO)在OMS-2催化氧化作用下生成CO2和H2O,现利用OMS-2对某密闭空间的甲醛进行催化氧化实验,实验开始时,该空间内甲醛含量为1.22mg/L,CO2含量为0.590mg/L,一段时间后测得CO2含量升高至1.25mg/L,该实验中甲醛的转化率为。
-
(1) 肼(N2H4)是发射航天飞船常用的高能燃料。将NH3和NaClO按一定物质的量比混合反应,生成肼、NaCl和水,该反应的化学方程式是。
-
(2) 在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂过氧化氢,当它们混合时,即产生大量气体,并放出大量热。已知:H2O(l)
①请写出液态肼与过氧化氢反应生成液态水的热化学方程式。
②则16 g 液态肼与足量过氧化氢反应生成液态水时放出的热量是。
实验Ⅰ:制取NaClO2晶体按右图装置进行制取。
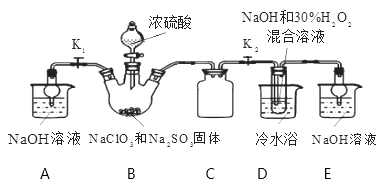
已知:NaClO2饱和溶液在低于38℃时析出NaClO2•3H2O,38-60℃时析出NaClO2 , 高于60℃时NaClO2分解成NaClO3和NaCl。
-
(1) 用50%双氧水配制30%的H2O2溶液,需要的玻璃仪器除玻璃棒、胶头滴管、烧杯外,还需要(填仪器名称);装置C的作用是。
-
(2) B中产生ClO2的化学方程式。
-
(3) 装置D中反应生成NaClO2的化学方程式为 。反应后的溶液中阴离子除了ClO2-、ClO3-、Cl-、ClO-、OH—外还可能含有的一种阴离子是,检验该离子的方法是。
-
(4) 请补充从装置D反应后的溶液中获得NaClO2晶体的操作步骤。
①减压,55℃蒸发结晶;②;③;④;得到成品。
-
(5) 如果撤去D中的冷水浴,可能导致产品中混有的杂质是;
-
(6) 实验Ⅱ:样品杂质分析与纯度测定
测定样品中NaClO2的纯度。测定时进行如下实验:
准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2-+ 4I-+4H+ =2H2O+2I2+Cl- , 将所得混合液稀释成100mL待测溶液。
取25.00mL待测溶液,加入淀粉溶液做指示剂,用c mol·L-1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL(已知:I2 +2S2O32-=2I-+S4O62-)。
①确认滴定终点的现象是。
②所称取的样品中NaClO2的物质的量为mol(用含c、V的代数式表示)。
则被水还原的BrF3的物质的量是( )
-
(1) 对于反应:NH4NO2 ═ N2↑+2H2O,NH4NO2 中 N 元素的化合价为;反应生 成 1 mol N2 , 转移的电子数的物质的量为mol。
-
(2) 氧化还原反应中实际上包含氧化和还原两个过程。下面是一个发生还原过程的反应式: NO3-+4H++3e- → NO↑+2H2O 和发生氧化过程 KI→I2(未配平),向 KI 溶液中滴加少量稀 硝酸能使上述氧化还原过程发生,该氧化还原反应的方程式:。
-
(3) 砷及其化合物有毒,如砒霜(As2O3)有剧毒,环境监测和法医学分析砒霜中毒的反应 原理:As2O3+6Zn+6H2SO4 ═ 2AsH3↑+6ZnSO4+3H2O。
①若生成的气体在标准状况下的体积为 4.48 L,则参加反应 Zn 的质量为g。
②用双线桥法标出上述反应中电子转移的方向和数目。
 2Na2S+Na2SO3+3H2O。关于该反应的说法错误的是( )
2Na2S+Na2SO3+3H2O。关于该反应的说法错误的是( )
-
(1) 配平下列离子方程式:
 +H2C2O4+H+ =Mn2+++H2O
+H2C2O4+H+ =Mn2+++H2O -
(2) 3.4 gOH-含有的电子数目是。
-
(3) 2CuH+2HCl=Cu+CuCl2+2H2↑,反应产生4.48 LH2(标准状况)时,转移的电子数为。
-
(4) 物质的量浓度相同的三种盐NaX、NaY和NaZ的溶液中,其pH分别为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是。
-
(5) 用原子符号表示中子数为11的Na原子。
-
(6) 30 gHCHO和CH3COOH含有的共价键数目为。
-
(7) C4H8ClBr有种同分异构体。
-
(1) I 高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾、次氯酸等还强。工业上制取铁酸钠的化学方程式是(未配平):Fe(NO3)3+ NaOH + Cl2→ Na2FeO4+ NaNO3+ NaCl + H2O
铁酸钠中,铁元素的化合价是;上述制取铁酸钠的反应中,铁元素被(填“还原”或“氧化”)。
-
(2) 高铁酸钠溶解于水,立即与水发生剧烈反应,放出氧气,正是这些在水中新产生出的氧原子发挥其极强的氧化能力给水杀菌消毒的。高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂原因铁元素转化为Fe(OH)3胶体,使水中悬浮物沉聚,Fe(OH)3胶体微粒直径的范围是nm,铁酸钠的电离方程式是。
-
(3) II 次磷酸(H3PO2)是一种精细磷化工产品,是一元中强酸,具有较强还原性。回答下列问题:
H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①利用H3PO2进行化学镀银反应中,氧化剂(Ag+)与还原剂(H3PO2)的物质的量之比为4∶1,则氧化产物为(填化学式)。
②从分类来看,NaH2PO2属于
a.正盐 b.酸式盐 c.钠盐 d.氧化物
-
(4) H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2 , 后者再与H2SO4反应。配平白磷与Ba(OH)2溶液反应的化学方程式
P4 +Ba(OH)2 + H2O —— Ba(H2PO2)2+PH3↑
-
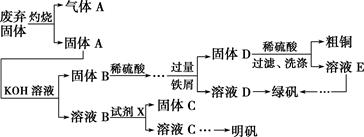
(1) 试剂X是(写化学式)。
-
(2) 配平下列方程式:
 +SO2+H2O===Mn2++
+SO2+H2O===Mn2++  +H+
+H+
-
(3) 为了分析产品(绿矾)中铁元素的含量,某同学称取 20.0 g样品配成100 mL溶液,移取25.00 mL于锥形瓶中,用0.100 0 mol·L-1的KMnO4标准溶液进行滴定(
 被还原为Mn2+)。
被还原为Mn2+)。 请回答下列问题:
①滴定时,KMnO4标准溶液应盛放在中(填仪器名称)。
②若到达滴定终点消耗KMnO4标准溶液的体积为25.00 mL,则该产品中铁元素的质量分数为。
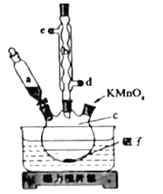
I.将浓H2SO4、NaNO3、石墨粉末在c中混合,置于冰水浴中。剧烈搅拌下,分批缓慢加入KMnO4粉末,塞好瓶口。
II.转至油浴中,35℃搅拌1小时,缓慢滴加一定量的蒸馏水。升温至98℃并保持1小时。
III.转移至大烧杯中,静置冷却至室温。加入大量蒸馏水,而后滴加H2O2至悬浊液由紫色变为土黄色。
IV.离心分离,稀盐酸洗涤沉淀。
V.蒸馏水洗涤沉淀。
VI.冷冻干燥,得到土黄色的氧化石墨烯。
回答下列问题:
-
(1) 装置图中,仪器a、c的名称分别是、,仪器b的进水口是(填字母)。
-
(2) 步骤I中,需分批缓慢加入KMnO4粉末并使用冰水浴,原因是.
-
(3) 步骤II中的加热方式采用油浴,不使用热水浴,原因是_.
-
(4) 步骤III中,H2O2的作用是(以离子方程式表示).
-
(5) 步骤IV中,洗涤是否完成,可通过检测洗出液中是否存在SO42-来判断。检测的方法是.
-
(6) 步骤V可用pH试纸检测来判断Cl-是否洗净,其理由是.
 ,该反应中还原产物和氧化产物的物质的量之比是( )
,该反应中还原产物和氧化产物的物质的量之比是( )
-
(1) K2FeO4的制备:

①i中反应的离子方程式是。
②将ii中反应的离子方程式补充完整:Fe3++OH-+ClO-=FeO42-++
③iii中反应说明溶解度:Na2FeO4K2FeO4(填“>”或“<”)。
-
(2) K2FeO4的性质:
i.将K2FeO4固体溶于蒸馏水中,有少量无色气泡产生,经检验为O2 , 液体有丁达尔效应。
ii.将K2FeO4固体溶于浓KOH溶液中,放置2小时无明显变化。
iii.将K2FeO4固体溶于硫酸中,产生无色气泡的速率明显比i快。
①K2FeO4溶于蒸馏水的化学反应方程式是。
②K2FeO4的氧化性与溶液pH的关系是。
-
(3) K2FeO4的应用。K2FeO4可用于生活垃圾渗透液的脱氮(将含氮物质转化为N2)处理。K2FeO4对生活垃圾渗透液的脱氮效果随水体pH的变化结果如下:
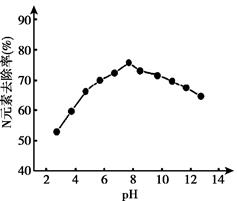
①K2FeO4脱氮的最佳pH是。
②根据图推测,pH=4时生活垃圾渗透液中含氮物质主要以形式存在。
③pH大于8时,脱氮效果随pH的升高而减弱,分析可能的原因:。
-
(1) 下列微粒:①S②SO
 ③Fe2+④Al3+⑤Na⑥HCl⑦Na2O2。在化学反应中只能被氧化的是(填序号),只能表现出氧化性的是(填序号)。
③Fe2+④Al3+⑤Na⑥HCl⑦Na2O2。在化学反应中只能被氧化的是(填序号),只能表现出氧化性的是(填序号)。
-
(2) 高铁酸钠(Na2FeO4)(其中氧元素是-2价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O。
①用双线桥法在化学方程式中标出电子转移的情况。
②当反应中有5个FeO
 离子生成时,转移的电子数是个。
离子生成时,转移的电子数是个。 -
(3) 请完成方程式的配平。Al+NO
 +OH-=AlO
+OH-=AlO  +N2↑+H2O
+N2↑+H2O
-
(4) 在一定条件下,2个X2O
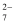 离子恰好能把6个SO
离子恰好能把6个SO  离子氧化成SO
离子氧化成SO  ,则还原产物中X元素的化合价为。
,则还原产物中X元素的化合价为。
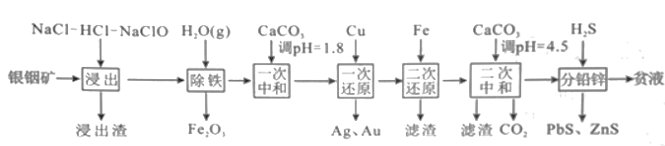
该工艺条件下,金属离子开始沉淀和完全沉淀的pH如表:
金属离子 | Fe3+ | In3+ | Ga3+ | Cu2+ | Zn2+ | Pb2+ |
开始沉淀的pH | 2.2 | 2.1 | 2.6 | 4.6 | 6.24 | 7.1 |
完全沉淀(c=1.0×10-5mol·L-1)的pH | 3.2 | 3.4 | 4.3 | 6.6 | 8.24 | 9.1 |
-
(1) “浸出”过程中金、银分别转化为AuCl
 、AgCl
、AgCl 进入溶液,同时生成硫,写出Ag2S发生反应的离子方程式。
进入溶液,同时生成硫,写出Ag2S发生反应的离子方程式。
-
(2) 高温水蒸气除铁利用了FeCl3易水解的性质,写出该反应的化学方程式。
-
(3) “二次还原”得到的滤液中主要的阳离子有H+、Na+、Ca2+、Zn2+、Pb3+、In3+、。
-
(4) “二次中和”得到的滤渣除少量Fe(OH)3外,主要成分还有(写化学式)。
-
(5) “分铅锌”步骤中,维持H2S饱和水溶液的浓度为0.1mol·L-1 , 为使Zn2+沉淀完全,需控制溶液的pH不小于已知:lg3≈0.48;Ksp(ZnS)=3.0×10-25 , Ka1(H2S)=1.0×10-7 , Ka2(H2S)=1.0×10-13]。
-
(6) 已知:氧化还原反应可看成由两个半反应组成,每个半反应具有一定的电极电势(用“φ”表示),φ越大则该物质的氧化性越强,φ越低则该物质的还原性越强。浸出步骤中金反应的两个半反应如下:
HClO+H++2e-=Cl-+H2O φ=1.49+
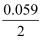 lg
lg
AuCl4-+3e-=4Cl-+Au φ=0.994+
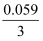 lg
lg
(φ与半反应式的系数无关,仅与浓度有关,cθ=1mol·L-1)
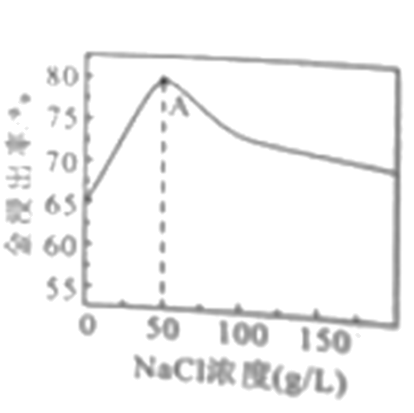
如图是Au的浸出率与NaCl溶液浓度的关系,请解释A点以后,金浸出率减小的原因是。
已知: ;
;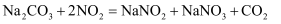
-
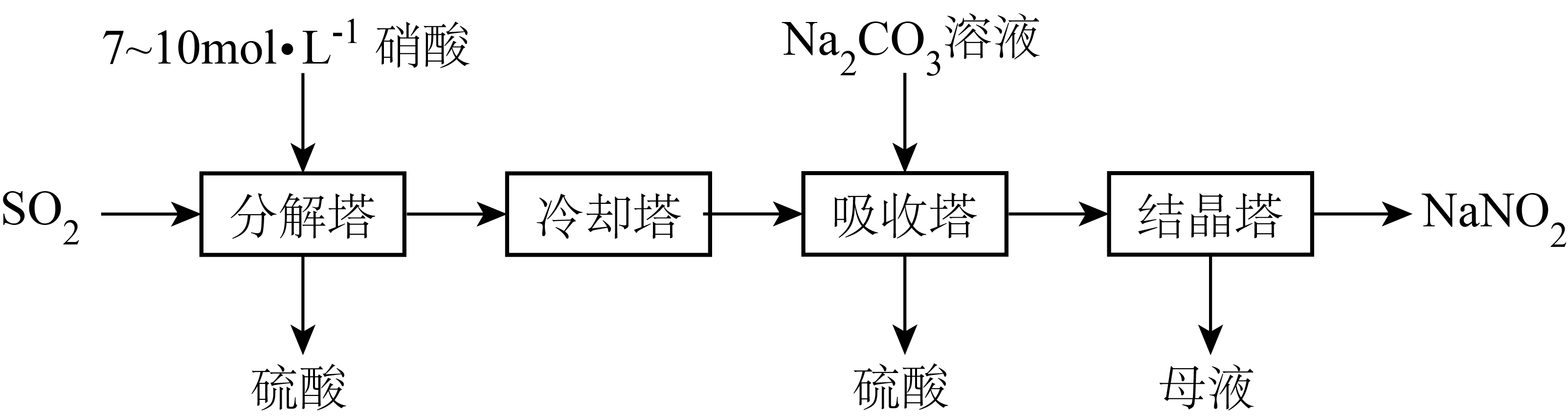
(1) 分解塔中填有大量的瓷环,其目的是:。分解塔中的温度不宜过高,其原因是:。
-
(2) 按一定计量比在分解塔中通
 和喷入硝酸,若反应后生成的
和喷入硝酸,若反应后生成的 与
与 物质的量之比恰好
物质的量之比恰好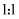 , 则分解塔中发生反应的化学方程式为。
, 则分解塔中发生反应的化学方程式为。
-
(3) 下列关于吸收塔中变化,说法正确的是。
a.升高吸收塔的温度,有利于氮氧化物的吸收
b.加快通入吸收塔中气体的流速,有利于提高氮氧化物的利用率
c.可向尾气中通入一定量的
 , 再通入吸收塔中,实现循环吸收
, 再通入吸收塔中,实现循环吸收 -
(4) 酸性条件下
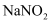 具有还原性。取
具有还原性。取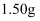 样品,配成
样品,配成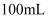 溶液。分别取出
溶液。分别取出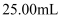 , 用
, 用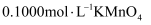 酸性标准溶液滴定三次,测得平均消耗
酸性标准溶液滴定三次,测得平均消耗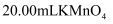 溶液。其离子方程式为:
溶液。其离子方程式为: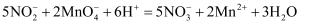 。计算样品中
。计算样品中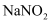 的纯度。(请写出计算过程)
的纯度。(请写出计算过程)
-
(5) 设计实验验证酸性条件下
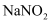 具有氧化性:取一定量
具有氧化性:取一定量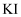 溶液,__。补充实验方案。(必须使用的试剂:
溶液,__。补充实验方案。(必须使用的试剂: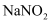 溶液、稀硫酸、淀粉溶液。)
溶液、稀硫酸、淀粉溶液。)
- 物价被称作是国民经济运行与发展的“晴雨表”。下列对图表的解读不正确的是 ( )A.
- 战国时期的著名战役不包括 A.城濮之战 B.桂陵之战 C.马陵之战 D.
- 有个部门组织了主题为:“重走北伐路”的学生夏令营活动。活动的 主要内容是:全体营员分为三组,从广州出发,分别按照当年北伐
- 表明物体做匀速直线运动的图象是( )
- 阅读下面这首宋词,完成8-9题。 贺圣朝·留别 (宋)清 臣 满斟绿醑①留君住,莫匆匆归去。三分春色二分愁,更一分风雨。
- ---Why do you look so upset? ---I broke up with my girlfr
- 密度为的氨水,其溶质的质量分数为0.25,该氨水用等体积的水稀释后,所得氨水的质量分数为A.等于12.5% B.大于12
- 由草木灰提取钾盐并检验钾元素存在的下列实验操作中,错误的是A.溶解 B.过滤 C.蒸发
- 有学者指出:“从一定意义上说,赫鲁晓夫既是斯大林模式的掘墓人,但最终还是扮演了守墓人的角色。”该学者的观点主要是指赫鲁晓
- 下列说法中正确的是( ) A.对于一定质量的理想气体,当温度升高时,分子的平均动能增大,则气体的压强一定增大B.
- 美国内战爆发前是“一国两制”的经济格局,此处的“两制”是指①北方资本主义工商业经济②南方封建主义经济③北方奴隶制经济④南
- 直接参与第二次中东战争的国家有:⑴英国 ⑵法国 ⑶埃及 ⑷美国 ⑸ 以色列 A.⑴⑵⑶⑷ B.⑴⑵⑶
- 有关氢氧化钠的叙述不正确的是() A.露置在空气中易变质 B.溶于水时放出热量 C.能使紫色石蕊试液变蓝色 D.
- 下列所述的情况,哪一种情况可以肯定钢棒没有磁性( ) A.将钢棒的一端接近磁针的N极时,则两者互相吸引,再将钢
- 阿根廷的牛肉在国际市场上竞争力很强的自然原因是 A.潘帕斯草原为温带海洋性气候区,牧草高而密 B.
- 阅读下列文言文,完成下面题目 召公谏厉王弭谤 厉王虐,国人谤王。召公告曰:“民不堪命矣!”王怒,得卫巫,使监谤者。以告,
- 新航路开辟后,世界各民族的历史逐渐融合为一部统一的人类历史。这种“融合”和“统一”实现的主要方式是 () A.西方的殖民
- 下列关于惯性的说法中正确的是( ) A.物体只有静止或做匀速直线运动时才有惯性 B.物体只有受外力作用时才有惯性
- 某气球内充满了一定质量的气体,当温度不变时,气球内气体的气压与气体体积之间是反比例函数关系,其函数图象如图所示.当气球内
- 28.下列对当今世界政治格局变化的概括,最为准确的是( ) A.多极化格局已经确立



