常见离子的检验 知识点题库
①Ag+、Fe3+、Na+ ②Ag+、Al3+、K+ ③Ag+、Ba2+、NO ④SiO、AlO、K+ ⑤Ag+、NH、H+ ⑥AlO、K+、Ba2+
 、Mg2+、Al3+、SO
、Mg2+、Al3+、SO  、NO3﹣、Cl﹣ . 某同学收集了该地区的雾霾,经必要的预处理后的试样溶液,设计并完成了如下实验:
、NO3﹣、Cl﹣ . 某同学收集了该地区的雾霾,经必要的预处理后的试样溶液,设计并完成了如下实验: 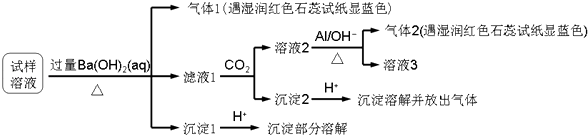
已知:3NO  +8Al+5OH﹣+2H2O
+8Al+5OH﹣+2H2O  3NH3↑+8AlO
3NH3↑+8AlO 
根据以上的实验操作和现象,该同学得出的结论不正确的是( )
操作 | 现象 | 结论 | |
A | 先滴加BaCl2溶液再滴加HCl溶液 | 生成白色沉淀 | 原溶液中有SO42﹣ |
B | 先滴加稀盐酸再滴加AgNO3溶液 | 生成白色沉淀 | 原溶液中有Cl﹣ |
C | 用洁净铁丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有K+ |
D | 滴加NaOH溶液加热,将湿润红色石蕊试纸置于试管口 | 试纸变蓝 | 原溶液中有NH4+ |
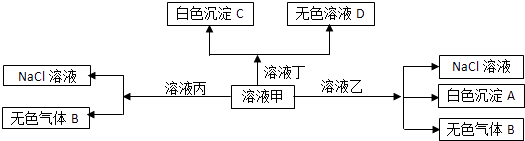
(I)取一定量的溶液于试管中,加入过量的Ba(NO3)2溶液有白色沉淀生成,过滤出的沉淀部分溶于稀HNO3 , 并放出5.6L(标况下)无色无味的气体,剩余沉淀4.66g.
(II)取部分滤液,加入过量的NaOH溶液并加热,产生13.6g无色有刺激性气味的气体,该气体能使湿润的红色石蕊试纸变蓝.
(III)另取部分滤液,加入AgNO3溶液,无明显现象.
根据以上现象,试判断:
①溶液中肯定存在的离子是 ;
②溶液中肯定不存在的离子是 ;
③溶液中可能存在的离子是 ;
④写出实验(I)中沉淀部分溶于稀HNO3并放出无色无味气体的离子方程式:
⑤实验(II)中产生气体的离子方程式为 .
-
(1) 为了进一步确认,对该溶液进行实验检测:
实验操作与现象
实验结论
判断理由
步骤一
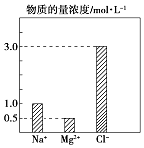
仔细观察坐标图
肯定无
肯定无该离子的理由
步骤二
该溶液呈无色、透明、均一状态
肯定无
肯定无该离子的理由
步骤三
加入足量BaCl2溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失
肯定有SO42﹣、H+;肯定无Ba2+
肯定有H+的理由
-
(2) 实验操作的步骤三中称量沉淀前的实验操作步骤有:过滤、、灼烧、在干燥器中冷却.
-
(3) 原溶液中H+物质的量浓度为 mol/L.
-
(4) 向溶液中加入NaHCO3溶液,反应的离子方程式为:.
-
(5) 若向 100mL 该溶液中加入 1mol/L 的 Ba(OH)2溶液,恰好沉淀完全时加入的Ba(OH)2溶液体积为 L.
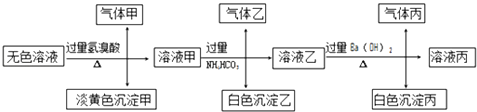
回答下列问题:
-
(1) 生成沉淀甲的离子方程式:;
-
(2) 已知气体甲由两种氧化物组成(不包括水蒸汽和HBr),请你设计实验逐一鉴别这两种成分,将所需试剂以及现象填入下表中(可不填满,表中每一行对应正确方可得分)
步骤
实验目的
试剂
现象
1
2
3
-
(3) 由溶液甲生成沉淀乙的离子方程式:;
-
(4) 综上所述,该溶液中肯定存在的离子有:.
-
(5) 针对溶液中可能存在的离子,用实验验证其是否存在的方法是.
可能大量含有的阳离子 | H+、K+、Mg2+、Al3+、NH4+、Fe2+、Fe3+ |
可能大量含有的阴离子 | Cl﹣、Br﹣、I﹣、CO32﹣、AlO2﹣ |
-
(1) 往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示.则该溶液中一定不含有的离子是.
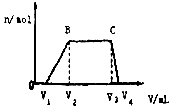
-
(2) BC段离子方程式为.
-
(3) 经检测,该溶液中还含有大量的Cl﹣、Br﹣、I﹣ , 若向1L该混合溶液中通入一定量的Cl2 , 溶液中Cl﹣、Br﹣、I﹣的物质的量与通入Cl2的体积(标准状况)的关系如表所示,分析后回答下列问题:
Cl2的体积(标准状况)
2.8L
5.6L
11.2L
n(Cl﹣)
1.25mol
1.5mol
2mol
n(Br﹣)
1.5mol
1.4mol
0.9mol
N(I﹣)
a mol
0
0
①a=.
②当通入Cl2的体积为2.8L时,溶液中发生反应的离子方程式为.
③原溶液中Cl﹣、Br﹣、I﹣的物质的量浓度之比为.
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据①②实验事实可推断:
-
(1) A的化学式,B的化学式。
-
(2) 写出过量盐酸与D反应的离子方程式:。
-
(3) 写出C与Ba(OH)2溶液反应的离子方程式:。
-
(4) C溶液中阴离子的检验方法: 。
-
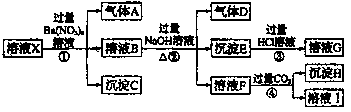
(1) 由题给信息可知,溶液X中确定不存在的阴离子有。
-
(2) 气体A是(填化学式),产生气体A的离子方程式为。
-
(3) 步骤④中发生反应的离子方程式为。
-
(4) 根据题给信息和图中转化关系,可以确定溶液X中肯定存在的离子有,可能存在的离子有。检验可能存在的离子是否存在的方法是。
 、Al3+、SO
、Al3+、SO  、Fe2+、Cl-等若干种离子,某同学设计并完成了如下实验:
、Fe2+、Cl-等若干种离子,某同学设计并完成了如下实验: 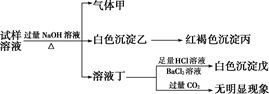
根据以上的实验操作与现象,该同学得出的结论错误的是( )
 、SO
、SO  和Fe2+
B . 试样溶液中一定没有Al3+
C . 若气体甲在标准状况下体积为0.448 L,沉淀丙和沉淀戊分别为1.07 g和4.66 g,则可判断试样溶液中还有Cl-
D . 该盐在工业上可以用作净水剂
和Fe2+
B . 试样溶液中一定没有Al3+
C . 若气体甲在标准状况下体积为0.448 L,沉淀丙和沉淀戊分别为1.07 g和4.66 g,则可判断试样溶液中还有Cl-
D . 该盐在工业上可以用作净水剂
 、
、  、
、  、
、  、
、  、
、 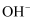 ,现进行如下实验:
,现进行如下实验: ①取适量该溶液,加入过量的  溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
②过滤出①中沉淀,向滤液中通入过量的  ,又生成白色沉淀。
,又生成白色沉淀。
③另取原溶液于试管中,加入足量氯水,再加入  溶液,振荡静置,下层为橙红色。
溶液,振荡静置,下层为橙红色。
根据上述实验回答:
-
(1) 溶液中一定大量存在的离子有 。
-
(2) 写出②中生成沉淀的离子方程式 。
-
(3) 如何检验未确定的离子是否存在? 。
 。某学习小组对该溶液进行探究以确定溶液组成。
。某学习小组对该溶液进行探究以确定溶液组成。 步骤1:取100mL溶液,加足量稀盐酸和足量BaCl2溶液,有白色沉淀产生,然后将溶液过滤,洗涤、干燥、用电子天平称量所得固体为6.99g。
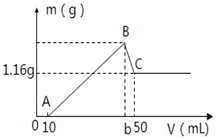
步骤2:另取100mL溶液,加入2.00mol/L的NaOH溶液,有白色沉淀产生。该小组同学依据相关现象和有关数据绘出NaOH溶液体积与沉淀质量的关系图象(如图所示)。请你协助小组同学通过计算确定溶液组成:
-
(1) c(SO
 )=mol/L
)=mol/L
-
(2) 请写出BC段发生反应的离子方程式。
-
(3) b=mL。
| 选项 | 实验操作和现象 | 结论 |
| A | 室温下,向溶液X中滴加少量双氧水,再加入KSCN溶液,变红 | 溶液X中一定含Fe2+ |
| B | 用洁净铂丝蘸取溶液Y在火焰上灼烧,火焰呈黄色 | 溶液Y中含Na+不含K+ |
| C | 室温下,向0.1mol·L−1Na2C2O4溶液中加入等体积0.1mol·L−1CaCl2溶液,产生白色沉淀 | Ksp(CaC2O4)=2.5×10−3 |
| D | 室温测定浓度均为0.1mol·L-1的CH3COONa溶液和NaNO2溶液的pH,CH3COONa溶液的pH大 | HNO2电离出H+的能力比CH3COOH强 |
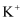 、
、  、
、 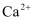 、
、  、
、  、
、  、
、  、
、  八种离子中的若干种,为确定其组成,进行如下实验。
八种离子中的若干种,为确定其组成,进行如下实验。 ①观察溶液颜色,溶液呈无色,做焰色实验,直接观察时发现焰色为黄色。
②取5mLX溶液,向其中加入  溶液,当沉淀量达到最大时
溶液,当沉淀量达到最大时  也恰好反应完,过滤后将滤渣置于足量盐酸中,充分搅拌后还剩余4.66g干燥固体(Y),将生成的气体全部导入澄清石灰水中,最终得到2g干燥沉淀(Z)。
也恰好反应完,过滤后将滤渣置于足量盐酸中,充分搅拌后还剩余4.66g干燥固体(Y),将生成的气体全部导入澄清石灰水中,最终得到2g干燥沉淀(Z)。
③向步骤②的滤液中加入 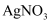 溶液得到mg白色沉淀(W)。
溶液得到mg白色沉淀(W)。
-
(1) 由步骤①知,溶液中一定含有的离子是,一定不存在的离子是。
-
(2) 由②知,X中含有的离子是,其中形成Y的源于X溶液的离子物质的量浓度是。
-
(3) 形成Z的离子方程式为。
-
(4) 则m的取值范围是:。
选项 | 实验操作 | 现象 | 结论 |
A | 某溶液中加入氯化钡溶液 | 生成白色沉淀 | 该溶液一定含有 |
B | 某溶液中加入无色酚酞试液 | 溶液变红色 | 该溶液一定是NaOH溶液 |
C | 蘸取某溶液做焰色试验 | 焰色呈黄色 | 该溶液一定含钠元素 |
D | 某溶液中加入硝酸银溶液 | 生成白色沉淀 | 该溶液一定含有 |
- 仿照下面诗歌的拟人手法,选取新的事物,另写一组意思完整、句式相近的句子。(不要求与原句字数相同) 眼睛很宽容
- (3分) 用如图甲所示的电路可以测量一个未知电阻的阻值,其中Rx为待测电阻,R为电阻箱(符号为≠),S为单刀双掷开关,R
- 下列化学用语或模型表示正确的是A.Cl-离子的结构示意图: B.CH4分子的球棍模型:C
- 将0.1mol的镁、铝混合物溶于100mL 2mol/LH2SO4溶液中,然后再滴加1mol/L NaOH溶液.若在滴加
- 图4示意东欧城市的典型空间结构。读图回答7-8题。 7.图中、、代表的依次是 A.工业区、别墅区、绿化区 B.绿化区、工
- 下列各组词语中,有两个错别字的一组是 () A.连袂 鞠躬尽粹 妄费 以逸代劳 B.
- 为了美化环境,某市加大对绿化的投资.2010年用于绿化投资20万元,2011年用于绿化投资25万元,求这两年绿化投资的年
- 下面短文中有10处语言错误。请在有错误的地方增加、删除或修改某个单词。 增加:在缺词处加一个漏字符号(/\),并在其下面
- 已知函数,则不等式的 解集是
- 对下列现象或做法的解释不正确的是 ( ) A.洒到地面上的酒会使房间充满酒味——分子在不断运动 B.在钢铁制品表面
- 将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量见下表:物质 a
- I don't like ______ as you read.A. the novels B. the such no
- 随着经济社会的发展和城市化进程的加快,和谐理念越来越为人们所接受。尤其是“三大和谐”的理念,即“人与人的和谐,人与自然的
- 估计介于( ) A.0.4与0.5之间 B.0.5与0.6
- 80年前美国经济学家泰罗提出“裙摆定律”,即裙子越短,经济越活跃;裙子越长,经济越萎靡。以19世纪中期英国为例,此时英国
- 在当今上海,“宁要浦西一张床,不要浦东一问房”的状况已经一去不复返。这主要是由于 A.长江三角洲的开放
- 已知△ABC的三个内角A,B,C满足:A+C=2B,,求的值
- 关于活鲫鱼的鳃的描述,错误的一项是() A.鳃盖在外面,起保护作用,是呼吸的主要结构 B.鳃丝既多又细 C.鳃是鲜红色的
- 下列图象关系合理的是
- 23.根据语境,在横线处填入适当的语句,使整个语段语意完整连贯。 语文是什么?语文是眩目的先秦繁星, ;是





