常见离子的检验 知识点题库
①取少量的溶液用硝酸酸化后,加Ba(NO3)2溶液,无沉淀生成.
②另取少量溶液加入盐酸,其现象是:一段时间保持原样后,开始产生沉淀并逐渐增多,沉淀量基本不变后产生一种气体,最后沉淀逐渐减少至消失.
-
(1) 肯定不存在的离子是.
-
(2) 写出步骤②中生成沉淀和气体的反应的离子方程式;
-
(3) 已知一定量的原溶液中加入5mL 0.2mol/L盐酸时,沉淀会完全消失,加入足量的硝酸银溶液可得到沉淀0.187g,则原溶液中是否含有Cl﹣?(填“有”或“无”).
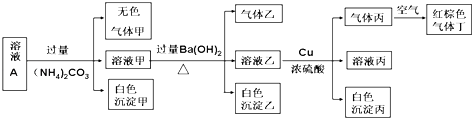
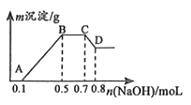
则:
-
(1) 溶液中一定含有的阳离子有,一定不含有的离子有.
-
(2) C→D的离子方程式为.
-
(3) 由A→B及C→D段有关数据可计算出的某两种离子的物质的量浓度分别为mol•L﹣1和mol•L﹣1 .
① (NH4)2SO4、KCl、MgCl2、Al2(SO4)3、FeSO4六种溶液
②Na2S、NaHSO3、NaAlO2、Na2SiO3、Na2SO4六种溶液
③FeO、CuO、MnO2、C四种黑色固体
④NaCl、Na2CO3、NaHSO4三种溶液
⑤Na2SO4、KSCN、KOH、AgNO3四种溶液
-
(1) 我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示:
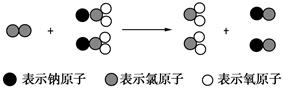
该反应的化学方程式为。
ClO2是一种优良的消毒剂,浓度过高时易发生分解,为了运输和贮存便利常将其制成NaClO2固体,模拟工业上用过氧化氢法制备NaClO2固体的实验装置如图所示。
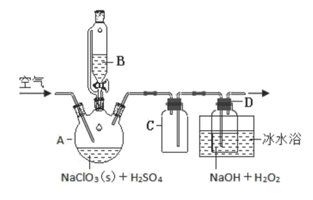
已知:H2O2沸点150℃,ClO2熔点为-59℃,沸点为11.0℃
A中的化学方程式:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
-
(2) 如果仪器B改成分液漏斗,实验过程中可能会出现的实验问题。
-
(3) 向A装置中通入空气,其作用是赶出ClO2 , 然后通过C再到D中反应。通空气不能过快,空气流速过快时ClO2不能被充分吸收;通空气也不能过慢,其原因是。
-
(4) 冰水浴冷却的目的是(双选)。
a.降低NaClO2的溶解度 b.使ClO2变为液态 c.加快反应速率
-
(5) 为证实产物中含有钠离子,方法是: 。
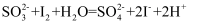 。某无色溶液中可能含有
。某无色溶液中可能含有  、
、  、
、  、
、 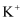 、
、 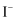 、
、  、
、  ,且所有离子的物质的量浓度相等。向该溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是( )
,且所有离子的物质的量浓度相等。向该溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是( )
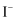 B . 可能含有
B . 可能含有  C . 肯定含有
C . 肯定含有  D . 肯定含有
D . 肯定含有 
资料:①CH3COONH4溶液呈中性。
②Cl-对该反应几乎无影响。
|
实验 |
实验试剂 |
实验现象 |
|
1 |
5mL蒸馏水 |
反应缓慢,有少量气泡产生(经检验为H2) |
|
2 |
5mL 1.0 mol/L NH4Cl溶液(pH=4.6) |
剧烈反应,产生刺激性气味气体和灰白色难溶固体 |
-
(1) 经检验实验2中刺激性气味气体为NH3 , 检验方法是。用排水法收集一小试管产生的气体,经检验小试管中气体为H2。
-
(2) 已知灰白色沉淀中含有Mg2+、OH-。为研究固体成分,进行实验:将生成的灰白色固体洗涤数次,至洗涤液中滴加AgNO3溶液后无明显浑浊。将洗涤后固体溶于稀HNO3 , 再滴加AgNO3溶液,出现白色沉淀。推测沉淀中含有,灰白色固体可能是(填化学式)。
-
(3) 甲同学认为实验2比实验1反应剧烈的原因是NH4Cl溶液中c(H+)大,与Mg反应快。用化学用语解释NH4Cl溶液显酸性的原因是。
-
(4) 乙同学通过实验3证明甲同学的说法不合理。
实验
实验装置
3
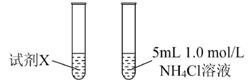
①试剂X是 。
②由实验3获取的证据为 。
-
(5) 为进一步探究实验2反应剧烈的原因,进行实验4。
实验
实验试剂
实验现象
4
5 mL NH4Cl乙醇溶液
有无色无味气体产生(经检验为H2)
依据上述实验,可以得出Mg能与
 反应生成H2。乙同学认为该方案不严谨,需要补充的实验方案是。
反应生成H2。乙同学认为该方案不严谨,需要补充的实验方案是。 -
(6) 由以上实验可以得出的结论是。
 B . 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO
B . 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO  C . 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液
D . 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH
C . 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液
D . 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH 
-
(1) 在表格空白处填写符合条件物质的序号
条件
序号
能导电
属于碱性氧化物
属于电解质
-
(2) 从上述物质中选择试剂,证明氧化性Fe3+>Cu2+:(用离子方程式表示)。
-
(3) ⑥中混有少量的①,除杂过程中选用的试剂和操作方法为。
-
(4) 将1.12g铁粉加入25mL2 mol•L-1的①中,充分反应后溶液中n(Fe3+)∶n(Fe2+)=。
-
(5) 设计实验证明某溶液含有①、⑥中的两种阳离子。
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向某溶液中滴加少量酚酞 | 溶液变红 | 该溶液一定是碱溶液 |
| B | 向某溶液中滴加少量盐酸 | 产生白色沉淀 | 原溶液中一定含有Ag+ |
| C | 将某气体通入品红溶液中 | 溶液褪色 | 该气体一定是SO2 |
| D | 向饱和AgCl溶液中加入NaCl固体 | 产生白色沉淀 | AgCl溶液中存在沉淀溶解平衡 |
| 实验目的 | 实验操作 | |
| A | 称取2.0gNaOH固体 | 右盘上加2g砝码,左盘上放NaOH固体 |
| B | 除去FeCl3溶液中含有少量的FeCl2杂质 | 向溶液中加入铁粉 |
| C | 检验溶液中是否含有Fe3+ | 取少量试液于试管中,加入KSCN溶液,观察溶液是否呈红色 |
| D | 向某溶液中滴加氯水后再加入KSCN溶液,溶液呈红色 | 溶液中一定含有Fe2+ |
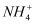 、Cl-、Mg2+、Ba2+、
、Cl-、Mg2+、Ba2+、  、
、  。现取三份各100mL溶液进行如下实验:第一份加入AgNO3溶液有沉淀产生;第二份加足量NaOH溶液加热后,收集到0.08mol气体;第三份加足量BaCl2溶液后,得到干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。正确的是( )
。现取三份各100mL溶液进行如下实验:第一份加入AgNO3溶液有沉淀产生;第二份加足量NaOH溶液加热后,收集到0.08mol气体;第三份加足量BaCl2溶液后,得到干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。正确的是( )
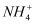 、
、  、
、  ,可能含Cl- , 且c(K+)≥0.4mol/L
B . 该混合液中一定含有:
,可能含Cl- , 且c(K+)≥0.4mol/L
B . 该混合液中一定含有: 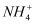 、
、  、
、  ,可能含K+、Cl-
C . 该混合液中一定含有:
,可能含K+、Cl-
C . 该混合液中一定含有: 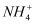 、
、  、
、  ,可能含Mg2+、K+、Cl-
D . 该混合液中一定含有:
,可能含Mg2+、K+、Cl-
D . 该混合液中一定含有: 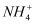 、
、  ,可能含Mg2+、Cl-
,可能含Mg2+、Cl-
 、H+、AlO
、H+、AlO  、CO
、CO  、NO
、NO  、Cl-十种离子中的几种,向该溶液中逐滴加入一定量1mol/LNaOH溶液,开始产生沉淀并逐渐增多,随后又逐渐减少,整个过程始终无气体放出。则下列判断正确的是( )
、Cl-十种离子中的几种,向该溶液中逐滴加入一定量1mol/LNaOH溶液,开始产生沉淀并逐渐增多,随后又逐渐减少,整个过程始终无气体放出。则下列判断正确的是( )
 B . 一定不含Cl- ,可能含有NO
B . 一定不含Cl- ,可能含有NO  C . 一定不含NH
C . 一定不含NH  、AlO
、AlO  、CO
、CO  D . 可能含有Fe3+、Fe2+ ,一定不含AlO
D . 可能含有Fe3+、Fe2+ ,一定不含AlO  、CO
、CO 
- 中国古代许多朝代出现“富者田连阡陌,贫者无立锥之地”的现象,根源在于 A.封建专制下的政治腐败 B.商品经济的
- 赵华同学体育中考时测了三次肺活量,三次测量的值为:2800ml、3000ml和3500ml,请问小明的肺活量是多少(
- 化合物Z由如下反应得到:,Z的结构简式不可能是() A.CH3CH2CHBrCH2Br B.CH3CH(CH2Br)2
- 作为中国公民,我们政治生活的基本内容是 A.依法行使政治权利,履行政治义务 B.参加社会主义政治文明建设 C.参与社会公
- 历史上,贝壳、粮食、皮革都曾充当过商品交换的媒介,但伴随着商品交换的发展,“贵金属”长期占有了货币的宝座。这是由于“贵金
- 小流域综合治理生态工程运用的原理主要包括( ) ①物质循环再生原理 ②协调与平衡原理 ③整体性原理 ④系统
- 在△ABC中,角A、B、C所对的边分别为a、b、c,且cosA=.(1)求sin2+cos2A的值;(2)若a=,求bc
- 在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混
- 化学学习小组做实验时记录了下列实验现象,其中正确的是 A.硫在空气中燃烧,发出蓝紫色火焰,产生有刺激性气味的气体 B.加
- of the two skirts satisfied Mary, so she asked _
- 可用于鉴别乙酸和乙醇的是()A. NaCl溶液 B. KNO3溶液 C. Na2CO3溶液 D. 紫色石蕊试液
- 由n个碱基组成的基因,控制合成由1条多肽链组成的蛋白质,氨基酸的平均分子量为a,则该蛋白质的分子量最大为()
- - In a textmessage, 88 means Bye-bye. - And anotherexample
- 汽车从甲地由静止出发,沿平直的公路开到乙地刚好停止运动,其速度图象如图所示,在0-t1和t1-3 t1两段时间内,汽车的
- 氨水有下列平衡:NH3·H2O NH4+ + OH– 当其它条件不变时,改变下列条件,平衡向左移动,且c(NH4+)增
- One day I took a bus with mygirlfriend. It was so 41 that we
- 语法与情景会话 Last Sunday we didn’t go out __________ the rain.
- 阅读下文,完成1—4题 鲍君 昔有人设罝以捕獐,得而未觉。有行人窃取之,犹念不仁,乃以鲍鱼置罝中而去。本主来,于罝中得鲍
- 下列各组稀溶液不用其他试剂和试纸,就可以将它们区别开的是 ( )A.硝
- 焦亚硫酸钠(Na2S2O5)常用作食品漂白剂。其制备工艺流程如下:已知:反应Ⅱ包含2NaHSO3Na2S2O5+H2O等



