电解质在水溶液中的电离 知识点题库
-
(1) 常温下,pH=5的NaHSO4溶液中水的电离程度pH=9的NH3•H2O中水的电离程度.(填“>”、“=”或“<”)
-
(2) 等体积等物质的量浓度的NaHSO4与氨水混合后,溶液呈酸性的原因为 . (用离子方程式表示);若一定量的NaHSO4溶液与氨水混合后,溶液pH=7,则c(Na+)+c(NH4+)
2C(SO42﹣)(填“>”、“=”或“<”);用硫酸氢钠与氢氧化钡溶液制取硫酸钡,若溶液中SO42﹣完全沉淀,则反应后溶液的pH7(填“>”、“=”或“<”).
阳离子 | K+、Na+、Ba2+、NH4+ |
阴离子 | CH3COO﹣、Cl﹣、OH﹣、SO42﹣ |
已知:
①A、C溶液的pH均大于7,B溶液的pH小于7,A、B的溶液中水的电离程度相同;D溶液焰色反应显黄色.
②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无明显现象.
(1)A的名称是 .
(2)写出C溶液和D溶液反应的离子方程式 .
(3)25℃时pH=9的A 溶液和pH=9的C溶液中水的电离程度小的是 (填写A或C的化学式).
(4)25℃时用惰性电极电解D的水溶液,一段时间后溶液的pH 7;(填>、<或=)
(5)B溶液中各种离子浓度由大到小的顺序为 .
0.01mol/L的溶液 | X | Y | Z | W |
PH | 12 | 2 | 8.5 | 4.5 |
(1)X、W的化学式分别为 、 .
(2)W的电离方程式为 .
(3)25℃时,Z溶液的pH>7的原因是 (用离子方程式表示).
(4)将X、Y、Z各1mol•L﹣1同时溶于水中制得混合溶液,则混合溶液中各离子的浓度由大到小的顺序为 .
(5)Z溶液与W溶液混合加热,可产生一种无色无味的单质气体,该反应的化学方程式为 .
①HA是 (填“强电解质”或“弱电解质”);
②在加水稀释HA溶液的过程中,随着水量的增加而减小的是 (填字母).
A.c(H+)/c(HA) B.c(HA)/(A﹣) C.c(H+)与c(OH﹣)的乘积 D.c(OH﹣)
③若M溶液是由上述HA溶液V1mL与pH=12的NaOH溶液V2mL混合充分反应而得,则下列说法中正确的是
A.若溶液M呈中性,则溶液M中c(H+)+c(OH﹣)=2.0×10﹣7 mol•L﹣1
B.若V1=V2 , 则溶液M的pH一定等于7
C.若溶液M呈酸性,V1一定大于V2
D.若溶液M呈碱性,V1一定小于V2 .
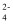 的物质的量为( )
的物质的量为( )
KCl | K2SO4 | ZnCl2 | ZnSO4 | |
甲 | 0.3mol•L﹣1 | 0.2mol•L﹣1 | 0 | 0.1mol•L﹣1 |
乙 | 0.1mol•L﹣1 | 0.3mol•L﹣1 | 0.1mol•L﹣1 | 0 |
下列对两份营养液成分的分析中,正确的是( )
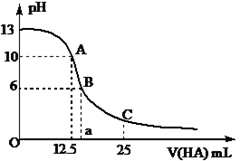
-
(1) 该氢氧化钠溶液的物质的量浓度为mol·L-1。
-
(2) A点对应酸的体积为12.5ml,则所得混合溶液中由水电离出的c(OH-)= mol·L-1。
-
(3) B点所示溶液中,c(CH3COO-)-c(Na+)= mol·L-1(填精确值),c(CH3COO-)/c(CH3COOH)=。
-
(4) C点所示溶液中,c(CH3COOH)c(CH3COO-)。(填“>”、“<”或“=”)
-
(5) 向300 mL上述NaOH溶液中通入448 mL CO2(标准状况)气体,充分反应后,溶液中粒子浓度关系正确的是________.A . c(Na+)+ c(H+)= c(OH-)+ c(HCO3-)+ c(CO32-) B . 2/3c(Na+)= c(HCO3-)+ c(CO32-)+ c(H2CO3) C . c(Na+)> c(CO32-)> c(HCO3-)> c(OH-)> c(H+) D . c(Na+)> c(HCO3-)> c(CO32-)> c(OH-)> c(H+)
 的盐酸中
的盐酸中 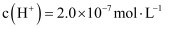 B . 将
B . 将 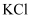 溶液从常温加热至
溶液从常温加热至 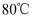 ,溶液的
,溶液的  变小但仍保持中性
C . 常温下,
变小但仍保持中性
C . 常温下, 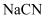 溶液呈碱性,说明
溶液呈碱性,说明 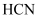 是弱电解质
D . 常温下,
是弱电解质
D . 常温下,  为3的醋酸溶液中加入醋酸钠固体,溶液
为3的醋酸溶液中加入醋酸钠固体,溶液  增大
增大
-
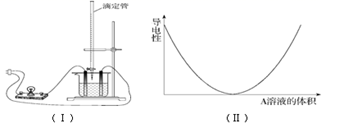
(1) 滴加溶液A至图(Ⅱ)中曲线最低点时,灯泡可能熄灭,溶液A中含有的溶质可能是。(填序号)
①HCl ②H2SO4 ③NaHSO4 ④NaHCO3
关于图(Ⅱ)下列说法中错误的是()
A 反应前一段导电能力不断减弱,说明生成的BaSO4是非电解质
B 图(Ⅱ)中最低点导电能力约为零说明溶液中几乎没有自由移动的离子
C 图(Ⅱ)中最低点导电能力约为零时,Ba(OH)2溶液与稀硫酸恰好完全中和
D Ba(OH)2 、H2SO4 和BaSO4都是电解质
-
(2) 请回答下列问题:
①写出NaHSO4在水溶液中的电离方程式。
②NaHSO4属于(填“酸”“碱”或“盐”)。
③将NaHSO4溶液中逐滴加入Ba(OH)2溶液中能否出现如图(Ⅱ)的导电性曲线()
A 能 B 否
-
(3) 用一种试剂除去下列各物质中的杂质(括号内的物质),写出所用的试剂及反应的离子方程式。
①CaCl2(CaCO3):试剂,离子方程式为;
②O2 (CO2):试剂,离子方程式为。
-
(4) 已知某温度下氯化钠的溶解度为a克,列式表达该温度下饱和氯化钠溶液的质量分数
①食盐 ②食醋 ③氯化钠固体 ④BaSO4固体 ⑤纯CH3COOH ⑥KHSO4 ⑦Ba(OH)2⑧Na2O ⑨CO2 ⑩次氯酸HClO ⑪乙醇 ⑫HNO3 ⑬CuSO4•5H2O ⑭Cu2(OH)2CO3 ⑮Cu ⑯Fe(OH)3胶体
-
(1) 以上物质能导电的有(填序号)。
-
(2) 以上物质属于电解质的正盐的有(填序号)。
-
(3) 属于一元弱酸的有(填序号)。
-
(4) 写出⑥在熔融状态的电离方程式:。
-
(5) 写出NaHCO3在水溶液条件下的电离方程式:。
-
(6) 不定相选择:下列有关分散系的表述错误的是_______A . 分散系是多组分混合而成的一种稳定体系。 B . 分散质和分散剂是相对的概念,如75%的酒精,分散质既可以是酒精也可以是水。 C . 按照物质所处的状态划分(气、液、固三态),分散系可以分为9种。 D . 按照分散质粒子的直径大小,分散系可以分为溶液、胶体、浊液。 E . 胶体是一种特殊的分散系,如氯化钠无论溶解在水中还是溶解在酒精中都不可形成胶体。
 样品(杂质为
样品(杂质为 )的纯度。步骤如下:
)的纯度。步骤如下:①称取m g样品,配制成100mL溶液;
②取出25mL溶液置于锥形瓶中,加入2滴酚酞溶液,用浓度为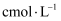 的盐酸滴定至溶液恰好褪色(溶质为
的盐酸滴定至溶液恰好褪色(溶质为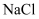 和
和 ),消耗盐酸体积为
),消耗盐酸体积为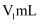 ;
;
③滴入2滴甲基橙溶液,继续滴定至终点,消耗盐酸体积为 。
。
下列说法正确的是( )
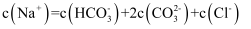 C .
C .  样品纯度为
样品纯度为 D . 配制溶液时放置时间过长,会导致最终测定结果偏高
D . 配制溶液时放置时间过长,会导致最终测定结果偏高
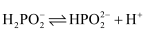 D . 0.01mol/L
D . 0.01mol/L 溶液中存在:
溶液中存在: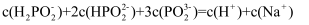
①2SO2(g)+CH4(g) 
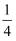 S8(g)+CO2(g)+2H2O(g)+Q1(Q1>0)
S8(g)+CO2(g)+2H2O(g)+Q1(Q1>0)
②2SO2(g)+CH4(g)  S2(g)+CO2(g)+2H2O(g)+Q2(Q2>0)
S2(g)+CO2(g)+2H2O(g)+Q2(Q2>0)
在容积固定的2 L密闭容器中,通入2 mol SO2和1 mol CH4 , 一定条件下发生上述反应。完成下列填空:
-
(1) Q1Q2(选填“>”或“<”)。能说明反应已达平衡状态的是。(选填编号)
A.CO2物质的量浓度不变 B.气体密度不变
C.容器内压强不变 D.容器内SO2与CH4的物质的量之比不变
-
(2) 如图为相同时间内测得SO2的转化率随温度变化情况。
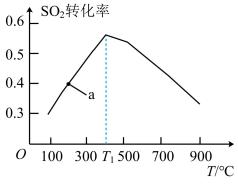
a点是否已达到化学平衡状态?(选填“是”或“否”)。随着温度升高,SO2转化率先升后降的原因是。
-
(3) 如图为某温度时,SO2和CH4的物质的量随时间变化情况。
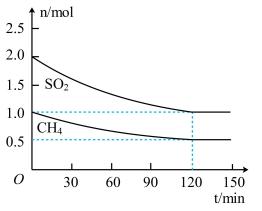
0~2 h内,v(CH4)=。温度不变,若要提高SO2的平衡转化率可采取的措施是(任写一条)。
-
(4) 烟气中的SO2常用氨水吸收。向氨水中通入SO2 , 测得溶液的pH与各含硫组分物质的量分数的关系如图所示。溶液的pH=7时,n(SO
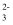 )∶n(HSO
)∶n(HSO )≈。氨水吸收烟气中SO2后,经O2催化氧化可得到硫酸盐。控制合适的温度,随着氧化的进行,溶液的pH(选填“增大” 或“减小”)。
)≈。氨水吸收烟气中SO2后,经O2催化氧化可得到硫酸盐。控制合适的温度,随着氧化的进行,溶液的pH(选填“增大” 或“减小”)。 
- 阅读下面这首诗,完成14~15题。 房兵曹胡马 杜甫 胡马大宛名,锋棱瘦骨成。 竹批双耳峻,风入四蹄轻。 所向无空阔,真
- 关于稳态的实现,下列叙述有误的是 A.血液中的缓冲物质可以调节PH B.肾脏不时地排出内环境中多余的水、尿素、无机
- 如图是某细胞的部分结构,下列有关叙述正确的是() A. 结构①中的磷元素主要分布于DNA中 B.
- (4分)用热水配制Al2(SO4)3溶液,出现浑浊现象,原因是
- 同圆中的两条弦长为和,圆心到两条弦的距离分别为和,且,那么,的大小关系是( ) A.B.C. D.
- 西汉学者贾谊在其《治安策》中宣称:“天下之势,方病大肿。一胫之大几如腰,一指(脚趾)之大几如股,平居不可屈信(伸),一
- 阅读下列材料,回答问题。 农奴制度是历史上出现过的残暴、野蛮的政治经济制度,对农奴制度的改革是历史的必然。 材料一
- 16.下列基因中,能产生4种配子的是 A.EeFF B.Aabb C.CcDdGg
- 两个氨基酸缩合成二肽,产生1分子水,这个水分子中的氢元素来自( ) A .氨基 B .羧
- 下列事例中表明光子不但具有能量,而且象实物粒子一样具有动量的是 ( )A.康普顿
- 下列关于生物体基本特征的叙述,正确的是 A.不管生物体的结构如何,生命活动都离不开细胞结构 B.发生在生物体内和环境中的
- 宋代“收乡长、镇将之权悉归于县,收县之权悉归于州,收州之权悉归于监司,收监司之权悉归于朝廷”,这一做法 A.实现了
- 下列各组离子在溶液中能大量共存的是 A. B.
- 双曲线C:-=1(a>0,b>0)的右焦点为F(c,0),以原点为圆心,c为半径的圆与双曲线在第二象限的交点
- 如图所示,在正的点电荷Q的电场中有a、b两点,它们到点电荷Q的距离r1<r2. (1)a、b两点哪点电势高? (2)将一
- 迷津欲有问, 。(孟浩然《早寒江上有怀》)
- 贝多芬于1804年创作完成《英雄交响曲》时,他在总谱的扉页上写下了“献给拿破仑·波拿巴”的字样。后来当他听到拿破仑称帝的
- He sighed again and the failure in physics seemed to have
- 56. It is interested tovisit another country.
- (08年康杰中学理)若函数,则与的大小关系是( ) (A) (B) (C



