电解质在水溶液中的电离 知识点题库
如图是在一定温度下向不同电解质溶液中加入新物质时溶液的导电性能发生变化,其电流(I)随新物质加入量(m)的变化曲线,以下四个导电性实验,其中与A图变化趋势一致的是 ,与B图变化趋势一致的是 ,与C图变化趋势一致的是 .
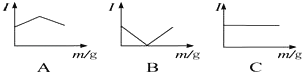
A.Ba(OH)2溶液中滴入H2SO4溶液至过量
B.醋酸溶液中滴入NH3•H2O至过量
C.澄清石灰水中通入CO2至过量
D.NH4Cl溶液中逐渐加入适量NaOH固体.
①石墨;②铝;③酒精;④氨水;⑤二氧化碳;⑥碳酸氢钠固体;
⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩氯化氢气体.
-
(1) 其中能导电的是;属于非电解质的是;属于强电解质的是;属于弱电解质的是.
-
(2) 写出物质⑥溶于水的电离方程式:.
-
(3) 写出物质⑥和⑧在水中反应的离子方程式:.
-
(4) 将物质⑥配制成溶液,逐滴加入⑦溶液中至沉淀量最大,写出离子方程式:.
A.KI固体 B.乙醇 C.Cl2 D.CaCO3固体 E.H2SO4 F.Mg(OH)2 G.石墨 H.CH3COOH
-
(1) 属于非电解质的是(填字母代号,下同),属于强电解质的是,属于弱电解质的是.它们的电离方程式是
-
(2) 能直接导电的是,水溶液能导电的是.
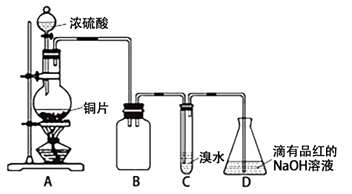
请回答下列问题:
-
(1) 装置B的作用是。
-
(2) 设计装置C的目的是验证SO2的性,装置C中发生反应的离子方程式是。装置D中NaOH全部转化为NaHSO3的标志是。
-
(3) 向NaHSO3溶液中加入NaClO溶液时,反应有三种可能的情况:
I.HSO3-与ClO-恰好反应
Ⅱ.NaClO不足
Ⅲ.NaClO过量

甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请完成下表:(已知酸性:H2SO3>H2CO3>HClO)
-
(4) 请设计简单实验证明:室温下HSO3-的电离平衡常数Ka与水解平衡常数Kb的相对大小:。
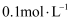 的
的  溶液呈酸性,下列关系错误的是( )
溶液呈酸性,下列关系错误的是( )
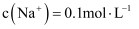 B .
B . 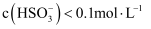 C .
C .  D .
D . 
| 选项 | 传统文化 | 化学角度解读 |
| A | | 利用物理方法可以检验钠盐和钾盐 |
| B | “司南之杓 | 司南中“杓”的材质为Fe3O4 |
| C | | 因为绿矾能电离出H+,所以“味酸” |
| D | 兰陵美酒郁金香,玉碗盛来琥珀光 | “香”主要因为美酒含有酯类物质 |
| 实验操作 | 现象 | 结论 | |
| A | 向某溶液中滴加稀HNO3 , 再加入过量的BaCl2溶液 | 产生白色沉淀 | 原溶液中一定含有SO |
| B | 25℃时分别测定等物质的量浓度的NaHCO3溶液和NaHC2O4溶液的pH值 | NaHCO3溶液的pH更大 | 酸性:H2CO3<H2C2O4 |
| C | 其他条件不变,将H2(g) + I2(g) | 气体颜色变浅 | 减小压强,平衡正向移动 |
| D | 将氯气和甲烷在光照下反应后的混合气体通入紫色石蕊试液 | 紫色石蕊试液变红 | 甲烷的氯代产物具有酸性 |
 )由大到小的顺序为:③>②>①
B . 0.1mol⋅L-1 的 Na2CO3 溶液:c(OH-)=c(H+)+c(
)由大到小的顺序为:③>②>①
B . 0.1mol⋅L-1 的 Na2CO3 溶液:c(OH-)=c(H+)+c(  )+c(H2CO3)
C . 0.1mol⋅L-1 的 CH3COOH 与 0.05mol⋅L-1 的 NaOH 溶液等体积混合(pH<7): c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)
D . 0.1mol⋅L-1 的 Na2CO3 与 0.05mol⋅L-1 的 NaHCO3 溶液等体积混合:5c(Na+)= 3c(
)+c(H2CO3)
C . 0.1mol⋅L-1 的 CH3COOH 与 0.05mol⋅L-1 的 NaOH 溶液等体积混合(pH<7): c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)
D . 0.1mol⋅L-1 的 Na2CO3 与 0.05mol⋅L-1 的 NaHCO3 溶液等体积混合:5c(Na+)= 3c(  )+3c(
)+3c(  )+3c(H2CO3)
)+3c(H2CO3)
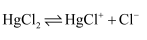 B . HgCl2的水溶液几乎不导电,说明其难溶于水
C . HgCl2中含有金属Hg,一定不是共价化合物
D . HgCl2是强电解质
B . HgCl2的水溶液几乎不导电,说明其难溶于水
C . HgCl2中含有金属Hg,一定不是共价化合物
D . HgCl2是强电解质
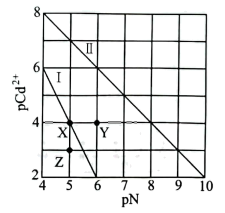
 (aq)平衡体系中,平衡常数K=102
(aq)平衡体系中,平衡常数K=102
酸 | HClO4 | H2SO4 | HCl | HNO3 |
电离平衡常数 | Ka=1.6×10-5 | Ka1=6.3×10-9 | Ka=1.6×10-9 | Ka=4.2×10-10 |
根据表格信息判断下列说法正确的是( )
 B . 这四种酸在冰醋酸中都能完全电离
C . 在冰醋酸中盐酸是这四种酸中最强的酸
D . 冰醋酸较水更能区分这四种酸的强弱
B . 这四种酸在冰醋酸中都能完全电离
C . 在冰醋酸中盐酸是这四种酸中最强的酸
D . 冰醋酸较水更能区分这四种酸的强弱
- 阅读下面短文,从短文后各题所给的四个选项(A、B、C和D)中,选出可以填入空白处的最佳选项。 For most,ge
- 要解决“山寨”苹果现象,政府应该( ) A.诚信经营,树立良好信誉和形象 B.不断提高企业自主创新能力 C
- 国务院决定从2008年到2010年启动4万亿投资计划。对4万亿元巨额投资的认识,正确的是( )学 ①它属于财政支出
- “Tell mewhat you were like when you were my age,” I asked m
- 下面各句的“莫”字全是副词的一项是 ( ) ①东西南北,莫可奔走 ②楚妃且勿叹,齐蛾且莫讴 ③
- 从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是 [来 A. 海带灼烧成灰 B. 过滤得含I—溶液 C.
- 下列各句中,语气最委婉的一句是 A.只关注孩子的学习成绩而忽视他们的心理健康,这是不是应该引起我们认真思考呢? B.只关
- 对物质进行分类学习是研究化学的重要方法.下列有关物质的分类错误的是() A.硝酸钾﹣盐 B.硫酸﹣酸C.纯碱﹣碱
- Hi! I’m Harry. Life used to be kind of difficult for me. Th
- 如图所示,用两条同样的绝缘细线悬挂两个带电小球,已知m甲=m乙,Q甲>Q乙,平衡时两细线与竖直线的夹角分别为α和β,则:
- 人体的某种免疫反应过程图如下,其中a~e代表不同免疫细胞,①~④代表生理过程。该过程最终能产生抗体与抗原结合。下列表述错
- 阅读材料,回答问题。(1 3分) 材料一:图14为某两区域示意图。 材料二:A地区和B地区均为著名的茉莉花产地。茉
- 北魏孝文帝从小就接受汉族文化的教育,不仅“五经之义”能拿过来就讲,史书传记、诸子百家涉猎颇多;对汉族的诗文也很有研究,他
- 函数y=lg(3-4x+x2)的定义域为M,当x∈M时,求f(x)=2x+2-3×4x的最值.
- PM2.5是指大气中直径小于或等于2.5微米的颗粒物,PM2.5粒径小,富含大量的有毒、有害物质,下列情况通常不可能引起
- 调节人体成为一个复杂、协调、统一的整体,使各种生命活动能够有序进行的系统是( )A.循环系统和神经系统B.呼吸
- 计算: (-2x3y4)3= ; (-0.125)8×88= .
- 下列叙述中,说法不正确的是A.复分解反应一定都不属于氧化还原反应B.在氧化还原反应中,金属单质一定不是氧化剂C.在氧化还
- 下列有关细胞分化的说法错误的是( ) A.细胞分化与生物发育有密切关系 B.细胞分化是生物界普遍存在的一种生命现象
- 2016年1月,中国第十八届中央纪委第六次全会强调,坚持全面从严治党依规治党,严格执行准则和条例,推动全面从严治党向基层
 本草经集注
本草经集注  记载“如握盐雪不冰,强烧之,紫青烟起
记载“如握盐雪不冰,强烧之,紫青烟起  云是真硝石也
云是真硝石也 勺
勺  ,投之于地,其柢
,投之于地,其柢  ”
”
 2HI(g)的平衡体系的容器体积增大为原来的10倍
2HI(g)的平衡体系的容器体积增大为原来的10倍


