电解质在水溶液中的电离 知识点题库
把下列四种物质分别加入到盛有100 mL蒸馏水的烧杯中,不能使蒸馏水导电性发生明显变化的是( )
A . 10 g NaCl固体
B . 10 g NaOH固体
C . 10 g BaSO4固体
D . 10 g Cu(NO3)2固体
将0.5mol的下列物质溶于500ml水中,含阴离子数目最多的是( )
A . CaCO3
B . CH3COONa
C . NH3
D . Na2SO3
下列物质的分类依据、类别、性质三者之间对应关系完全正确的是( )
物质 | 分类依据 | 类别 | 性质 | |
A | FeCl2 | 铁元素化合价 | 还原剂 | 可与O2、Zn等发生反应 |
B | FeCl2 | 电离产生的微粒 | 盐 | 可发生水解反应,溶液显碱性 |
C | HNO3 | 在水中能电离出H+ | 酸 | 可与CuO反应生成NO |
D | HNO3 | 氮元素的化合价 | 氧化剂 | 可与Al、I﹣等发生反应 |
A . A
B . B
C . C
D . D
下列各组均为两种化合物溶于水时电离出的离子,其中由酸电离的是( )
A . Na+、OH﹣、SO42﹣
B . H+、Cl﹣、SO42﹣
C . Na+、K+、OH﹣
D . Na+、K+、NO3﹣
体积相同的某植物营养液两份,其配方分别如下.两溶液成分
第一份:0.3mol KCl、0.2mol K2SO4、0.2mol ZnSO4
第二份:0.1mol KCl、0.3mol K2SO4、0.1mol ZnCl2( )
A . 完全不同
B . 仅n(Cl﹣)相同
C . 完全相同
D . 仅n(K+)、n(Cl﹣)相同
某兴趣小组用白云石(主要含CaCO3 和MgCO3)和废铝屑制备一种化合物12CaO·7Al2O3。
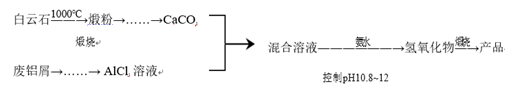
相关信息如下:
①MgCO3 分解温度低于 CaCO3;
②金属离子形成氢氧化物沉淀的 pH 范围:
| 金属离子 | pH | |
| 开始沉淀 | 完全沉淀 | |
| Ca2+ | 11.3 | - |
| Mg2+ | 8.4 | 10.9 |
③AlCl3 易水解,易升华。请回答:
-
(1) 从煅粉经一系列操作可制备纯净的CaCO3。请给出合理的操作排序(从下列操作中选取,按先后次序列出字母) :
煅粉→加入适量 NH4NO3 溶液→( )→()→()→通入 NH3 和 CO2 , 控制pH<11.0→过滤→洗涤→CaCO3
a.过滤 b.控制 pH=11.0 c.控制 pH=8.0 d.取滤渣加水形成悬浊液 e.取滤液
-
(2) 煅粉加入 NH4NO3 溶液发生反应的离子方程式是。
-
(3) 通入 NH3 和 CO2 时,需控制 pH<11.0 的原因是。
-
(4) 下列说法正确的是_________。A . 煅烧时,需用玻璃棒不断搅拌坩埚中固体,使其受热均匀 B . 煅烧时产生 CO2 的体积恰好等于制备 CaCO3 时需要通入 CO2 的体积(已换算为相同状况) C . NH4NO3 溶液还可用(NH4)2SO4、NH4HCO3 等溶液代替 D . 过滤时,应选用玻璃砂漏斗,以免滤纸被溶液腐蚀
-
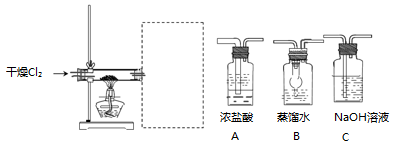
(5) 废铝屑需要先放在乙醇和丙酮混合溶液中,放入超声波清洗器中清洗 30 分钟,目的是。取出晾干,用以下装置制备 AlCl3 溶液。请为虚线框中补充必须的装置,并按连接顺序排列 (填写代表装置的字母,不考虑橡皮管连接)。
下列说法不正确的是( )
A . 0.1 mol •Lˉ1CH3COOH 溶液加水稀释,CH3COO- 数目增多,c(OH-)增大
B . 室温下,NaHSO3 溶液的 pH<7,说明HSO3-的电离程度大于其水解程度
C . 酸碱质子理论认为,凡能给出质子(H+)的物质都是酸,凡能接受质子的物质都是碱。由该理论可知:NaHCO3、H2O、Al(OH)3 均可称为酸碱两性物质
D . 25℃时 0.1mol•L-1 的H2S 水溶液中,加入一定量的NaOH 溶液,当溶液中存在: c(Na+)=c(S2-)+c(HS-)+c(H2S)时,溶液的主要溶质为Na2S
常温下,用0.1 mol·L-1 KOH溶液滴定10 mL 0.1 mol·L-1 HA(Ka=1.0×10-5)溶液的滴定曲线如图所示。下列说法错误的是( )
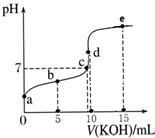
A . a点溶液的pH约为3
B . 水的电离程度:d点>c点
C . b点溶液中粒子浓度大小:c(A-)>c(K+)>c(HA)>c(H+)>c(OH-)
D . e点溶液中:c(K+)=2c(A-)+2c(HA)
下列叙述中正确的是( )
A . 金属氧化物一定是碱性氧化物
B . 溶于水后能电离出氢离子的化合物都是酸
C . 硫酸钡难溶于水,但硫酸钡属于强电解质
D . 氯化钠溶液在电流作用下电离成钠离子和氯离子
25℃时,有c(HA)+c(A-)=0.1mol/L 的一组HA、KA 混合溶液,溶液中c(HA)、c(A-)与pH 的关系如下图所示。下列叙述错误的是( )
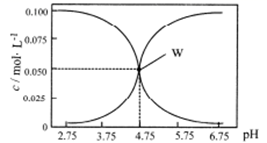
A . pH= 5.75 的溶液中: c(K+)>c(A- )>c(HA)> c (H+)>c(OH- )
B . 欲得W 点所示溶液,起始所加溶液应符合c(HA)+c(A-)=0.1mol/L 且c(KA)<c(HA)
C . pH=3.75的溶液中:c(K+)+c(H+)-c(OH-)+c(HA)=0.1mol/L
D . 若A-的水解常数为Kh ,则lgKh=-9.25
下列说法正确的是( )
A . HCl溶于水后形成水合氢离子和水合氯离子
B . HCl属于电解质,故溶于水或融熔状态下均能导电
C . 氨气属于电解质,因为氨气的水溶液能导电
D . Cl2属于电解质,因为其水溶液能导电
室温时,下列有关电解质的说法正确的是( )
A . pH相等的HNO3和HCN两种酸溶液中,c(  )>c(CN-)
B . NaHB溶液呈酸性,可推知H2B在水中不能完全电离
C . 往NH4Cl溶液中加入镁粉,可生成两种气体
D . Na2CO3溶液中通入CO2所得的中性溶液中:c(Na+)=2(
)>c(CN-)
B . NaHB溶液呈酸性,可推知H2B在水中不能完全电离
C . 往NH4Cl溶液中加入镁粉,可生成两种气体
D . Na2CO3溶液中通入CO2所得的中性溶液中:c(Na+)=2(  )
)
 )>c(CN-)
B . NaHB溶液呈酸性,可推知H2B在水中不能完全电离
C . 往NH4Cl溶液中加入镁粉,可生成两种气体
D . Na2CO3溶液中通入CO2所得的中性溶液中:c(Na+)=2(
)>c(CN-)
B . NaHB溶液呈酸性,可推知H2B在水中不能完全电离
C . 往NH4Cl溶液中加入镁粉,可生成两种气体
D . Na2CO3溶液中通入CO2所得的中性溶液中:c(Na+)=2(  )
)
下列关于电解质溶液的说法正确的是( )
A . 0.1mol/L的KA溶液 pH=6.5,则 HA一定为弱酸
B . 等 pH的盐酸和醋酸溶液加水稀释10倍后,c(Cl-)<c(CH3COO-)
C . 将 pH=3的醋酸溶液稀释后,溶液中所有离子的浓度均降低
D . 常温下,pH相同的盐酸和醋酸,将两溶液升温至 80℃后溶液的 pH仍然相同
下列关于电解质溶液的叙述错误的是( )
A . 常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)=c(NH  )
B . pH=12的溶液中,Na+、Cl-、AlO
)
B . pH=12的溶液中,Na+、Cl-、AlO  、ClO-可以大量共存
C . pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴人石蕊溶液呈红色
D . 向0.1 mol·L-1的氨水中加入少量硫酸铵固体,溶液中
、ClO-可以大量共存
C . pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴人石蕊溶液呈红色
D . 向0.1 mol·L-1的氨水中加入少量硫酸铵固体,溶液中  增大
增大
 )
B . pH=12的溶液中,Na+、Cl-、AlO
)
B . pH=12的溶液中,Na+、Cl-、AlO  、ClO-可以大量共存
C . pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴人石蕊溶液呈红色
D . 向0.1 mol·L-1的氨水中加入少量硫酸铵固体,溶液中
、ClO-可以大量共存
C . pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴人石蕊溶液呈红色
D . 向0.1 mol·L-1的氨水中加入少量硫酸铵固体,溶液中  增大
增大
水溶液因水解呈酸性的是( )
A . NaHSO4
B . BaCl2
C . CH3COONa
D . NH4Cl
常温下,已知Ka1(H2CO3)=4.3×10-7 , Ka2(H2CO3)=5.6×10-11。某二元酸H2R及其钠盐的溶液中,H2R、HR-、R2-三者的物质的量分数随溶液pH变化关系如图所示,下列叙述正确的是( )
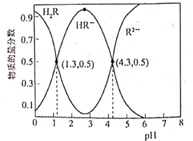
A . H2R的二级电离常数Ka2的数量级为10-5
B . 在pH=4的溶液中:3c(R2-)<c(Na+)+c(H+)-c(OH-)
C . 等体积、等浓度的NaOH浴液与H2R溶液混合后,溶液中:(R2-)<c(H2R)
D . 向Na2CO3溶液中加入过量H2R溶液,发生的反应是: CO3- +H2R=CO2↑+H2O+R2-
下列说法正确的是( )
A . NaCl在熔融条件能导电
B . NaCl固体不导电,因为NaCl固体中无阴阳离子
C .  在熔融态电离:
在熔融态电离: 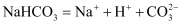 D . 盐酸能导电,盐酸是电解质
D . 盐酸能导电,盐酸是电解质
 在熔融态电离:
在熔融态电离: 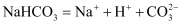 D . 盐酸能导电,盐酸是电解质
D . 盐酸能导电,盐酸是电解质
已知有下列物质:盐酸、稀硫酸、硫代硫酸钠、氨水、二氧化硫、铜、碳酸、醋酸、碳酸钡、硫化氢。请回答问题:
-
(1) 上述物质中属于强电解质且其水溶液能导电的是。填化学式
-
(2) 硫化氢的水溶液称为氢硫酸,写出氢硫酸第二步电离的方程式。
-
(3) 硫代硫酸钠在酸性溶液中不能存在的原因是。(用离子方程式表示)
-
(4) 氨水中存在个平衡,向氨水中加入少量CH3COONH4固体,一水合氨的电离平衡向移动。(填“右”“左”或“不移动”)
-
(5) 一定温度下冰醋酸稀释过程中溶液的导电能力变化如图所示,A、B、C三点中
 浓度最大的是点,电离程度最大的是点,如果对C点的溶液进行长时间加热,其导电能力会。(填“增强”“不变”或“减弱”)
浓度最大的是点,电离程度最大的是点,如果对C点的溶液进行长时间加热,其导电能力会。(填“增强”“不变”或“减弱”) 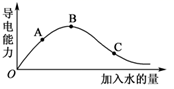
常温下,下列有关电解质溶液的叙述正确的是( )
A . 在  溶液中
溶液中  B . 在
B . 在  溶液中
溶液中  C . 在
C . 在  溶液中
溶液中 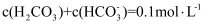 D . 氨水和NH4Cl溶液混合,形成pH=9的溶液中
D . 氨水和NH4Cl溶液混合,形成pH=9的溶液中 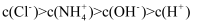
 溶液中
溶液中  B . 在
B . 在  溶液中
溶液中  C . 在
C . 在  溶液中
溶液中 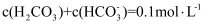 D . 氨水和NH4Cl溶液混合,形成pH=9的溶液中
D . 氨水和NH4Cl溶液混合,形成pH=9的溶液中 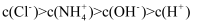
室温下,向10mL氨水中加入蒸馏水,将其稀释到1L后,下列说法中错误的是( )
A .  的数目增多
B . 除水分子之外所有粒子浓度都会减小
C . 含氮粒子数目之和不变
D .
的数目增多
B . 除水分子之外所有粒子浓度都会减小
C . 含氮粒子数目之和不变
D .  的电离常数不变
的电离常数不变
 的数目增多
B . 除水分子之外所有粒子浓度都会减小
C . 含氮粒子数目之和不变
D .
的数目增多
B . 除水分子之外所有粒子浓度都会减小
C . 含氮粒子数目之和不变
D .  的电离常数不变
的电离常数不变
最近更新
- 与被子植物相比,裸子植物特有的特征是( ) A.受精作用离开水 B.靠种子进行繁殖 C.种子没有果皮包被着 D.
- Everywhere man has cut down forests in order to grow_____ cr
- 下列关于细胞结构和生物体内化合物的叙述正确的是( ) A.抗体、激素、神经递质、酶发挥一次作用后都将失去生物活
- 下列关于我国所面临的困难,正确的是A.粮食需求增加,粮食增产举步维艰 B.人口继续膨胀与迅速年轻化C.农业资源日益
- 依次填入下列各句中横线处的词,最恰当的一组是() ①世博会是________创造精神最集中的空间,在家门口举办的世博会能
- They prepared manmade rubberas a(n) ________ for the natura
- —There is still a copy of the book in the library. Wall you
- 在下列叙述中,正确的是 A.摩尔是个基本物理量 B.物质的量是衡量微观粒子数量的物理量
- 关于各元素相对含量说法正确的是()A. 地壳中含量最高的元素是氧 B. 海洋中含量最高的元素是氯 C. 空气中含量最高的
- 目前城市生态环境恶化的根本原因是() A.与城市地域结构模式不合理有关 B.城市人口、工业的膨胀产生大量废弃物,超过了环
- 欲使0.2 mol·L-1 Na2SO3溶液和0.4 mol·L-1 NaCl溶液中Na+的物质的量相等,应取两种溶液的
- 下列实验操作中错误的是() A. 点燃酒精灯 B. 滴加溶液 C. 量筒读数 D. 放置滴管
- 银杏俗称白果,它属于裸子植物的主要原因是() A. 种子外无果皮包被 B. 种子外有果皮包被 C. 体内有输导
- 在△中, ,,则 ;的最小值是 .
- 读图。漫画告诫我们,国家机关工作人员应该坚持 A. 调查研究 B. 决策为民 C. 求真务实
- 一竖直弹簧下端固定于水平地面上,小球从弹簧的正上方高为h的地方自由落下到弹簧上端,如图5-5-4所示,经几次反弹以后小球
- Hi! My name is Jenny. I am a student in PEP Middle School in
- 写出求过已知三点的圆的方程的一个算法.
- “Are there any post offices ________ around here?”asked the
- The news got around the world; people came from___________to



