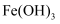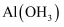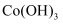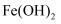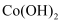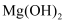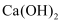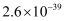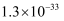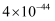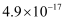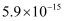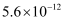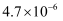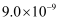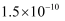蒸发和结晶、重结晶 知识点题库
在粗盐提纯的实验中,蒸发时正确的操作是( )
A . 把浑浊的液体倒入蒸发皿内加热
B . 开始析出晶体后用玻璃棒搅拌
C . 待水分完全蒸干后停止加热
D . 蒸发皿中出现大量固体时即停止加热
下列有关实验操作的说法正确的是( )
A . 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
B . 用pH试纸测定溶液的pH时,需先用蒸馏水润湿pH试纸
C . 用稀硝酸溶液洗涤并灼烧铂丝后,再进行焰色反应
D . 用CCl4萃取溴水中的溴,分液时有机层从分液漏斗的下端流出
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( )
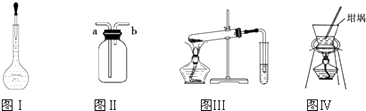
A . 图Ⅰ配制1mol/L NaCl溶液定容操作
B . 图Ⅱa口进气可收集Cl2、CO2等气体
C . 图Ⅲ探究NaHCO3的热稳定性
D . 图Ⅳ蒸发结晶获得氯化钠晶体
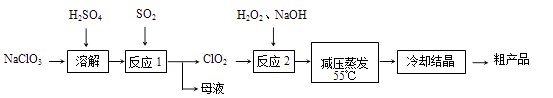
亚氯酸钠(NaClO2)主要用于棉纺、造纸业的漂白剂,也用于食品消毒、水处理等,亚氯酸钠受热易分解。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下:
-
(1) “反应2”的还原剂是,写出它的电子式,该反应的化学方程式为,原因是。
-
(2) 采取“减压蒸发”而不用“常压蒸发”,原因是。
-
(3) 从“母液”中可回收的主要物质是。
-
(4) “冷却结晶”后经(填操作名称)即可获得粗产品。
下列叙述正确的是( )
A . 乙醇能够使酸性KMnO4溶液和酸性K2Cr2O7溶液褪色均被氧化成乙酸
B . 向酸性高锰酸钾中加入草酸溶液,随着反应的进行,反应速率逐渐减小
C . 向某溶液中滴加BaCl2溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该溶液中存在SO42-或SO32-
D . 实验室提纯混有少里氯化钠的硝酸钾,通常采用重结晶的方法
下列物质分离提纯的方法错误的是( )
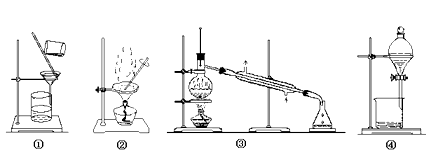
A . 提纯含杂质的工业酒精选择装置③
B . 提纯含杂质的粗苯甲酸选择装置①②
C . 从溴水中提纯溴选择装置④
D . 苯中混有少量苯酚选择装置④
用下列实验装置进行相应实验,能达到实验目的是( )
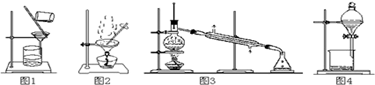
①用图1所示装置从Fe(OH)3胶体中过滤出Fe(OH)3胶粒
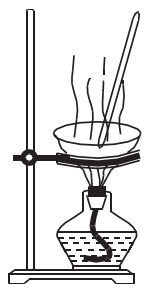
②用图2所示装置从氯化钠溶液中得到氯化钠晶体
③用图3所示装置从碘的四氯化碳溶液中分离出四氯化碳
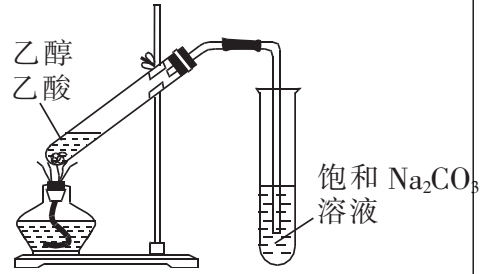
④用图4所示装置从乙醇与苯的混合物中分离出苯
A . ①②
B . ②③
C . ②③④
D . ①③④
孔雀石主要含Cu2(OH)2CO3 , 还含少量Fe、Si的化合物。某工厂以孔雀石为主要原料制备CuSO4·5H2O,主要步骤如下:
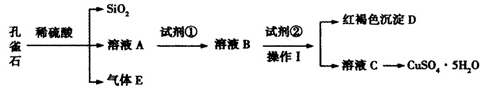
已知该条件下,通过调节溶液的酸碱性而使 Fe3+、Fe2+、Cu2+生成沉淀的 pH 分别如下:
|
物质 |
开始沉淀时的pH |
完全沉淀时的pH |
|
Fe(OH)3 |
2.2 |
3.2 |
|
Fe(OH)2 |
7.6 |
9.6 |
|
Cu(OH)2 |
4.7 |
6.4 |
请回答下列问题:
-
(1) 为了提高孔雀石酸浸时的速率,除适当增加浓硫酸浓度外,还可以采取的措施有:(写一种)。
-
(2) 试剂①是双氧水,把 Fe2+氧化成 Fe3+的目的是。根据如图有关数据,你认为工业上氧化操作时应采取的条件是。
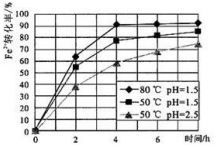
-
(3) 试剂②为CuO,其目的是调节溶液的 pH 保持在范围。操作Ⅰ的名称是。
-
(4) 溶液 C 得到CuSO4·5H2O的主要步骤是、、过滤、洗涤、干燥。
下列实验操作中错误的是( )
A . 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
B . 蒸馏操作时,应使冷凝管中的冷却水从下口进上口出
C . 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D . 称量NaOH固体时,将NaOH固体放在托盘天平的左盘的小烧杯中并盖上玻璃片
规范操作是实验的基本要求。下列操作规范的是( )
A .  转移溶液
B .
转移溶液
B .  搅拌溶液
C .
搅拌溶液
C .  熄灭酒精灯
D .
熄灭酒精灯
D .  取蒸发皿
取蒸发皿
 转移溶液
B .
转移溶液
B .  搅拌溶液
C .
搅拌溶液
C .  熄灭酒精灯
D .
熄灭酒精灯
D .  取蒸发皿
取蒸发皿
-
(1) Ⅰ.我国的青海省有许多盐湖盛产食盐,人类与食盐关系密切,食盐在老百姓生活和现代社会的工农业生产中均有重要作用。粗盐中含Ca2+、Mg2+、SO42-以及泥沙等杂质,为了除去可溶性杂质,有以下实验步骤进行提纯:
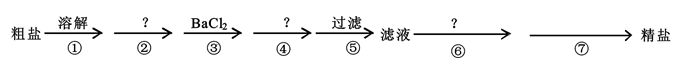
④步所加试剂是。
-
(2) 第⑥步发生反应的离子方程式为、。
-
(3) 第⑦步的操作名称,需要的玻璃仪器有、。
-
(4) 通过步骤⑤中过滤后的滤液,检验SO42-已除尽的操作方法是。
-
(5) Ⅱ.设阿伏加德罗常数为NA , 标准状况下,某O2和N2的混合气体m g含有b个分子,则n g该混合气体在相同状况下所占的体积是L。
-
(6) 在xR2++yH++O2═mR3++nH2O的离子方程式中,对化学计量数m和R2+、R3+判断正确的是____。A . m=y,R3+是氧化产物 B . m=2y,R2+被氧化 C . m=2,R3+是氧化剂 D . m=4,R2+是还原剂
-
(7) 用双线桥法标出下列反应的电子转移方向和数目。2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
下列相关实验的叙述中正确的是( )
A . 在胆矾溶液中滴入少许烧碱溶液,再加入有机物加热可验证含醛基类物质
B . 实验室测定硫酸铜晶体中结晶水含量时,需要进行的称量操作一定为4次
C . 为验证氯乙烷中含氯,将其与氢氧化钠溶液混合加热后再滴入硝酸银溶液
D . 需要约480mL0.100mol/L的NaOH溶液,配制时可准确称量NaOH2.000g
工业制取皮革加工中的鞣化剂硝酸铝,是用铝灰与烧碱、硝酸反应制得的。铝灰是铝、氧化铝和氧化铁的混合物。产品硝酸铝晶体为Al(NO3)3·nH2O。
已知偏铝酸盐能与一般的酸反应,如:NaAlO2+HNO3+H2O→NaNO3+Al(OH)3↓
生产流程如图:

完成下列填空:
-
(1) 用氢氧化钠固体配制30%的氢氧化钠溶液,除烧杯、玻璃棒外还需(选填编号)。
A.
 B.
B.  C.
C.  D.
D. 
说出流程中产生的滤渣的一种用途是。制作一个过滤器需要。流程中操作x的名称是。
-
(2) 反应Ⅱ加入的硝酸必须适量,原因是。反应Ⅲ加入的硝酸要稍过量,原因是。
-
(3) 从反应Ⅲ所得的溶液制成产品的步骤依次为减压蒸发,,过滤,,低温烘干。
-
(4) 为测定所得的产品的纯度,质检人员称取产品Wg,溶于水配成500mL溶液,从中取出25.00mL,加入过量已知浓度的氨水充分反应后,剩余的氨水用已知浓度的盐酸溶液进行测定。通过计算便可得出产品的纯度。
①上述过程属于定量实验。其中除配制一定物质的量浓度的溶液外,还有一个是,该实验过程中要进行多次读数,读数的方法是读出与的刻度值。
②任意写出一个该测定过程中所涉及的化学反应的离子方程式:。
下列实验操作中错误的是( )
A . 蒸发操作时,将蒸发皿中固体完全蒸干停止加热
B . 过滤操作时,要沿着玻璃棒慢慢向漏斗中倾倒过滤液
C . 蒸馏操作时,冷凝水应从冷凝管下口进,上口出
D . 分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出
下列实验装置能达到相应实验目的的是( )
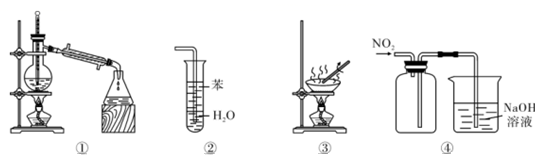
A . 用装置①分离沸点不同的液体混合物
B . 用装置②于吸收 HCl气体,能够防止倒吸
C . 用装置③加热硫酸铜溶液制得硫酸铜固体
D . 用装置④收集 NO2气体
溴、碘主要存在于海水中,有“海洋元素”的美称。海水中的碘主要富集在海带中,我国海带产量居世界第一位,除供食用外,大量用于制碘。提取碘的途径和装置如下图所示,下列有关叙述正确的是( )
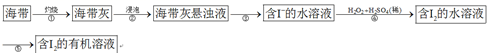
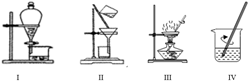
A . 完成步骤①需要装置Ⅲ
B . 完成步骤③需要装置Ⅰ
C . 步骤⑤中溶剂可选用酒精或苯
D . 完成步骤②和④需要装置Ⅳ
下列说法错误的是( )
A . 将CoCl2•6H2O晶体溶于95%乙醇,加水稀释,溶液颜色由蓝色逐渐转变为粉红色
B . 从海带中提取碘的实验可用CCl4溶解海带灰,增大碘的浸出率
C . 用蒸馏法提纯物质时,如果温度计水银球位于蒸馏烧瓶的支管口以下,会使收集的产品中混有低沸点的杂质
D . 硝酸钾在制备过程中应趁热过滤,在过滤过程中应加入2mL水,目的是避免固体中NaCl等杂质因温度较低而冷却析出,影响硝酸钾的纯度
实验室中下列灼烧、过滤、蒸馏、分液使用的装置错误的是( )
A . 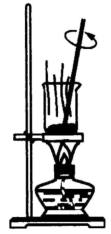 B .
B . 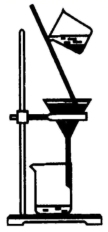 C .
C .  D .
D . 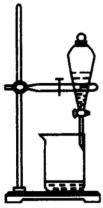
 B .
B .  C .
C .  D .
D . 
下列实验方案能达到实验目的的是( )
选项 | A | B | C | D |
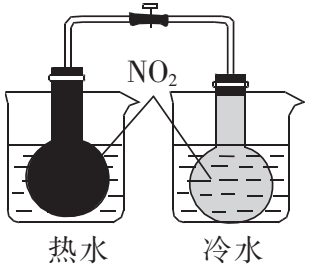
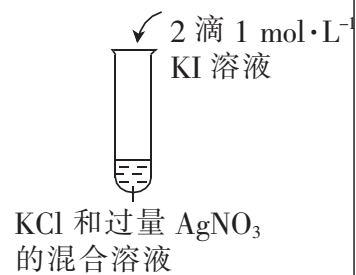
目的 | 制备并收集乙酸乙酯 | 证明温度对平衡的影响 | 证明AgI的溶解度小于AgCl | 蒸干氯化锰溶液制 |
实验方案 |
|
|
|
|
A . A
B . B
C . C
D . D
某化工厂利用废旧锂离子电池的正极材料(含有 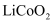 以及少量Ca、Mg、Fe、Al等)制备
以及少量Ca、Mg、Fe、Al等)制备  和
和 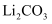 的工。艺流程如下:
的工。艺流程如下:
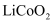 以及少量Ca、Mg、Fe、Al等)制备
以及少量Ca、Mg、Fe、Al等)制备  和
和 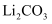 的工。艺流程如下:
的工。艺流程如下: 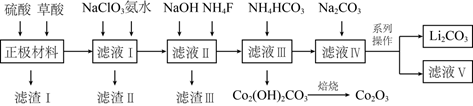
已知:①草酸(  )是一种二元弱酸,不稳定易分解,具有还原性。
)是一种二元弱酸,不稳定易分解,具有还原性。
②常温时,有关物质  如下表(单位已略):
如下表(单位已略):
| | | | | | | | | |
| | | | | | | | | |
③当离子浓度  ,可认为沉淀完全。
,可认为沉淀完全。
④常温下 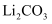 的溶解度为
的溶解度为 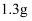 ,
, 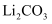 的溶解度随温度的升高而逐渐减小。
的溶解度随温度的升高而逐渐减小。
回答下列问题:
-
(1) 拆解后的“正极材料”需按先后顺序加酸,最后加入的是(填“硫酸”或“草酸”),溶解
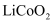 的反应的离子方程式为。
的反应的离子方程式为。
-
(2) “滤液Ⅰ”中加入氨水调
 为5,则“滤渣Ⅱ”的主要成分是(填化学式)。若先调节
为5,则“滤渣Ⅱ”的主要成分是(填化学式)。若先调节  并控制到5,再加入
并控制到5,再加入 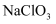 ,则
,则 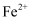 被氧化时的离子方程式为。
被氧化时的离子方程式为。
-
(3) 若取
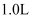 “滤液Ⅱ”,测得
“滤液Ⅱ”,测得  、
、  浓度均为
浓度均为 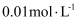 ,则至少需加入g(保留到小数点后1位)
,则至少需加入g(保留到小数点后1位) 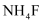 固体才能使
固体才能使  沉淀完全。
沉淀完全。
-
(4) 在空气中“焙烧”
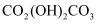 的化学方程式为。
的化学方程式为。
-
(5) 为了获得更多更纯的
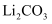 固体,“系列操作”依次为和干燥。
固体,“系列操作”依次为和干燥。
最近更新
- 某单质能与足量浓硝酸反应,若参加反应的单质与硝酸的物质的量之比为1∶4,则该元素在反应中所显示的化合价可能为( )
- 枕下的零食 罗兰 ①在我幼年的时候,每天晚上临睡之前,父亲必在床前陪我们,讲故事给我们听,讲到我们睡意蒙胧的时候,我们就
- 秦皇岛将承办2008年北京奥运会的部分足球比赛,请拟一条手机短信邀请朋友届时观看比赛。不超过60字。(4分)
- There was one thought that air pollutionaffected only the ar
- 为探究物质对草履虫的刺激是有利还是有害,某中学生物兴趣小组的同学做了以下实验:⑴取两片载玻片,分别编号1和2。
- 在做“用单摆测定重力加速度”的实验时测得g值偏大,其原因可能是( ) A.小球质量太小
- 已知数列{an}满足a1=,an+1=. (1)证明数列是等差数列,并求{an}的通项公式; (2)若数列{bn}满足b
- “起来,饥寒交迫的奴隶;起来,全世界受苦的人,满腔热血已经沸腾,要为真理而斗争…” 这首《国际歌》一直激励着一代又一代的
- 精子和卵细胞经过受精作用形成受精卵,在受精卵细胞中() A.细胞核的遗传物质完全来自卵细胞 B.细胞
- .阅读下面一段文字,回答问题(4分) 2003年前后,“山寨产品”在南方城市“崭露头角”,但当时还没被统称为“山寨机”,
- 在下列学校生活中,属于不自信的行为是( ) A.当老师为挑选800米跑运动员为难时,小强挺身而出说“我能行” B.
- 已知四种物质在水中、液氨中的溶解度〔g(溶质)/100 g(溶剂)〕如下表,这几种化合物在两溶剂中能发生复分解反应的为_
- 下表是前20号元素中的部分元素的一些数据: A B C D E F G H I J 原子半径(10-10m) 1.02
- 某班在讨论“挫折”这个话题时,同学们各抒己见。你认为正确的是A.挫折只会给人带来损失和痛苦B.挫折是成长的障碍,应当绕过
- 关于诉讼调解,下列说法中正确的是( ) ①目的是使当事人达成调解协议②目的是惩罚违法当事人③法院制作的调解书在当事人签
- 下列词语中加点字字义不同的是 A.相宜 因地制宜 B.谋生 栩栩如生 C. 振作
- — What can I do for you, sir? — I want _____. A. a dollar’s
- 我国有文字可考的历史始于商朝。你认为商朝用来记事的文字应该是 A.楔形文字 B.甲骨文
- 补写出下列名篇名句中的空缺部分。 (1)______________,烟光凝而暮山紫。(王勃《滕王阁序》) (2)峨嵋山
- 如图 3-7-5甲所示为电热毯电路示意图,交流电压 μ=311 sin100πt(V),当开关 S 接通时,电热丝的电功